3aula potencial padrão e k ELETROQUÍMICA
-
Upload
clauberdalmas -
Category
Documents
-
view
575 -
download
3
description
Transcript of 3aula potencial padrão e k ELETROQUÍMICA
03/09/2011
Prof Clauber
Uma das aplicaes mais teis dos potenciais padro no clculo das constantes de equilbrio a partir de dados eletroqumicos. As tcnicas que desenvolvemos aqui pode ser aplicado a qualquer tipo de reao, incluindo a neutralizao e reaes de precipitao , bem como reaes redox, desde que pode ser expressa como a diferena de duas semi-reaes de reduo.
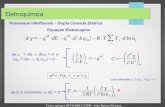
A energia livre de Gibbs padro, Gr, est relacionada com a constante de equilbrio da reao por Gr = - RT ln K. Sendo que Gr est relacionada a fem padro de uma clula galvnica por Gr= - nFEo , ento:
nFEo = RT ln K
(eq.4)
1
03/09/2011
Rearranjando:
ln K
nFE RT
o
Por causa da magnitude de K que aumenta exponencialmente com Eo, uma reao com um Eo com um valor muito grande e positivo tem K >>1.
O fato de que podemos calcular E a partir de potenciais padro nos permite calcular constantes de equilbrio para qualquer reao que pode ser expresso em duas semi-reaes. A reao no precisa ser espontnea nem tem de ser uma reao redox.
Exemplo
Exemplo
Calcular a constante de equilbrio 25,00 oC de:
Encontrando Eo:E o 0,22V 0,8V 0,58V
AgCl(s) Ag+(aq) + Cl-(aq)
E o E o reduo E ooxidao
Para esta reao, Kps =
[Ag+]
[Cl-]ln K
AgCl(s) + e- Ag(S) + Cl-(aq) Ag(s) Ag+(aq) + e-
Eo = + 0,22V Eo = -0,80 V
nFE o RT
ln K
nE o RT / F
ln K ps
1 ( 0,58V ) 0,58V 0,025693V 0,0256930 ,58V
Para esta reao, note que o nmero de e- envolvido 1.
V K ps e 0,025693 1,6 1010
2
03/09/2011
Utilizando uma tabela de potenciais padro, calcule o Kps do Hg2Cl2. Cd(OH)2
Como uma reao acontece em direo ao equilbrio, as concentraes de reagentes e seus produtos e G aproxima zero. Portanto, como reagentes so consumidos em uma clula eletroqumica de trabalho, o potencial das clulas tambm diminui at que finalmente chega a zero (ddp=0).
Uma bateria morta aquela em que a reao de clula atingiu o equilbrio. No equilbrio, uma clula de zero gera diferena de potencial entre os eletrodos ea reao no pode mais fazer o trabalho. Para descrever este comportamento quantitativamente, precisamos descobrir como a fem clula varia de acordo com as concentraes de espcies na clula.
3
03/09/2011
Como fazer isto?Para estabelecer como a fem de uma clula depende da concentrao, primeiro note que a fem proporcional reao de energia livre de Gibbs (Eq. 2). Ns j sabemos como Gr varia com a composio:
Como fazer isto?Como Gr=-nFE e Gro=-nFEo , permite que:
nFE nFE o R T ln Q
Dividindo por nF, tem-se a expresso;
Gr Gr R T ln Qo
E Eo
RT ln Q nF
Q quociente da reao
Equao de Nersnt
chamado de equao de Nernst devido o alemo eletroqumico Walther Nernst, que foi o primeiro derivado dele. Em 298,15 K, RT / F = 0,025 693 V de modo na temperatura da equao de Nernst toma a forma:
s vezes conveniente usar esta equao com logaritmos comum, caso em que fazemos uso da relao: ln x = 2,303 log x. 298,15 K:
E Eo
2,303 RT 0,05917 V ln Q E o ln Q n n
E Eo
0,025 693 V ln Q n
4
03/09/2011
Aplicaes da Equao de NersntA equao de Nernst amplamente utilizado para estimar a fora eletromotriz de clulas sob condies no padro. Em biologia utilizado, entre outras coisas, para estimar a diferena de potencial atravs das membranas celulares biolgicas, tais como os de neurnios.
Zn(s) | Zn2+(aq) || Cu2+(aq) | Cu(s) Cu2+(aq) + Zn(s) Zn2+(aq) + Cu(s)Q aZn2 aCu2 o
[ Zn2 ] 0,10 M 2 [Cu ] 0,0010 M
n=2
E o ER EP 0,34 ( 0,76)V 1,10Vo
Usando a equao de Nersnt para predizer uma fem
Calcule a fem 25oC de uma clula de Daniel na qual a [ Zn2+(aq)] = 0,10 mol/L e [ cu2+(aq)] = 0,0010 mol/L e
E Eo
0,025693V 0,1 RT ln ln Q 1,10 V 2 0,0010 nF 1,10V 0,059V 1,04 V
Primeiro, escreva a equao balanceada para a reao das clulas e da expresso correspondente para Q, e observe o valor de n. Ento determine Eo a partir dos potenciais padro na tabela 12.1 ou 2B apndice. Determinar o valor de Q para as condies estabelecidas. Calcule a fem, substituindo esses valores na equao de Nernst, Eq. 6 25,0C, RT / F = 0,025 693 V.
5
03/09/2011
Calcule a fem das clulas: Zn(s) | Zn2+(aq, 1,5mol/L) || Fe2+(aq, 0,10 mol/L) | Fe(s)
Ag(s) | Ag+(aq, 0,0010mol/L) || Ag+(aq, 0,010mol/L) | Ag(s)
Uma aplicao importante da equao de Nernst a medida de concentrao. Em uma clula de concentrao, os dois eletrodos so idnticos, exceto para as suas concentraes. Para este tipo de clula, a E= 0, e 25 C o potencial para esta reao da clula est relacionado com Q por E = - (0,025693 V / n) ln Q.
Por exemplo, uma clula de concentrao, tendo dois Ag / Ag eletrodos Ag(s) | Ag+(aq, Esq) || Ag+(aq, dir) | Ag(s)
Se Ag+(aq, dir) = 1mol/L
Ag+(aq, Esq) Ag+(aq, dir)
Portanto, medindo-se E, pode-se inferir a concentrao de Ag no compartimento do eletrodo esquerdo. Se a concentrao de ons Ag+ no eletrodo da esquerda menor do que na direita, ento E>0 para a clula, conforme especificado eo eletrodo mo direita ser encontrado para ser o catodo.
6
03/09/2011
Usando a Equao de Nersnt para encontrar uma concentrao
Cada compartimento do eletrodo de uma clula galvnica contm um eletrodo de prata e 10,0 mL de 0,10 M AgNO3 (aq), que so conectadas por uma ponte de sal. Voc agora adicionar 10,0 mL de 0,10 M NaCl(aq) para o compartimento do eletrodo esquerdo. Quase toda a prata precipita como o cloreto de prata, mas fica um pouco na soluo como uma soluo saturada de AgCl. A fem medida E = + 0,42 V. Qual a concentrao de Ag+ na soluo saturada?
Esta clula uma clula de concentrao em que a concentrao de Ag+ em um compartimento determinada pela solubilidade do AgCl. Use a equao de Nernst, Eq. 6, para encontrar a concentrao de Ag+ no compartimento com o precipitado. A fem padro da clula 0 (em seus estados padro dos eletrodos so idnticos). 25,00 C, RT / F = 0,025 693 V.
Ag(s) | Ag+(aq, Esq) || Ag+(aq, dir) | Ag(s) Ag+(aq, Esq) Ag+(aq, dir)Q [ Ag ]esquerdo [ Ag ]direito
ln Q
0,42V 16,34 0,025693V
[ Ag ]esquerdo 0,010
Q e16,34 n=1 Como [Ag+]esquerdo = Q [Ag+]direito [Ag+]esquerdo = e-16,34 0,1 = 8,0 10-9
E RT E Eo ln Q ln Q R T nF nF
Ou seja, a concentrao de ons Ag+ presentes na soluo saturada de 8,0 nmol.L-1.
7
03/09/2011
Calcule a concentrao molar de Y3+ em uma soluo saturada de YF3 pelo uso de uma clula construda com dois eletrodos de trium. O eletrlito no compartimento 0,1M Y(NO3)2(aq) . No outro compartimento tem preparado uma soluo saturada de Y(NO3)2(aq) . A medida do potencial da clula +0,34V 298K.
Calcule a fem de uma clula construda com dois eletrodos de cobre. O eletrlito em um dos compartimentos 1,0M de AgNO3(aq). No outro compartimento, NaOH tem sido adicionado a uma soluo de AgNO3(aq) at que o pH atinja 12,5 298K.
Uma aplicao importante da equao de Nernst a medio do pH (e, atravs de pH, constantes de acidez). O pH de uma soluo pode ser medido eletroquimicamente com um aparelho chamado de pHmetro.
8
03/09/2011
A tcnica faz uso de uma clula na qual um eletrodo sensvel concentrao de H3O+ e outro eletrodo serve como referncia. Um eletrodo sensvel concentrao de um on em particular chamado de `eletrodo de on-seletivo.
Uma combinao de eletrodos que poderia ser usado para determinar o pH um eletrodo de hidrognio ligados por uma ponte de sal para um eletrodo de calomelano. A reduo semi-reao para o eletrodo de calomelano Hg2Cl2(s) + 2 e- 2 Hg(l) + 2 Cl-(aq) E =+0,27 V
Figura: eletrodo de calomelano
A reao global da clula Hg2Cl2(s) + H2(g) 2 Hg(l) + 2 Cl-(aq)Q [ H ]2 [Cl ]2 PH 2
Desde que a presso do hidrognio um bar, podemos escrever o quociente de reao como Q = [H+]2 [Cl-]2.
9
03/09/2011
Para encontrar a concentrao de ons de hidrognio, escrevemos a equao de Nernst:Como:
A concentrao de Cl- de um eletrodo de calomelano fixado no momento da fabricao de soluo com a saturao do KCl, e assim [Cl-] uma constante. Podemos, portanto, combinar os dois primeiros termos do lado direito em uma nica constante, E = E (0,0257 V) ln [Cl-]. Ento, porque ln x = 2,303 log x
O eletrodo de vidro para medir pHPortanto, medindo-se a clula fem E, podemos determinar o pH. O valor de E estabelecido pela calibrao da clula, o que exige a medio E para uma soluo de pH conhecido.
Um eletrodo de vidro, um bulbo de vidro de paredes finascontendo um eletrlito, muito mais fcil de usar do que um eletrodo de hidrognio e tem um potencial que varia linearmente com o pH da soluo fora do bulbo de vidro.
10
03/09/2011
Eletrodo de vidro para medida de pH medida de pH medida da diferena de potencial atravs de uma membrana de vidro que separa a soluo desconhecida de uma soluo de referencia cuja [H+] conhecidapH-metro
Eletrodo de vidro para medida de pHH+ + Na+VdNa+ + H+Vd-
Sol.
Vidro
sol.
vidro
ESC
eletrodo de vidro
fio de prata soluo de pH desconhecido HCl O,1 M saturado c/ AgClFina membrana de vidro (responsvel pela resposta ao pH)
agitador magntico
11
03/09/2011
Muitas vezes h um eletrodo de calomelano incorporado a sonda que faz contato com a soluo de teste atravs de uma ponte salina em miniatura. Um pHmetro , portanto, normalmente tem apenas uma sonda, que forma uma clula eletroqumica completa, uma vez que mergulhado em um soluo. O pHmetro calibrado com um tampo de concentrao conhecida, e a fem da clula de medio ento automaticamente convertida para o pH da soluo, que exibido.
Eletrodos disponveis comercialmente, usados em pXmetros, so sensveis a outros ons, tais como Na+, Ca2+, NH4+, CN- e S2-. So usados para monitoiar processos industriais e para controIe da poluio. O pH ou o concentrao de ons podem ser medidos pelo uso de um eletrodo que responde seletivamente a somente uma espcie de on.
Eletrodos on Seletivo Amnia - Brometo - Cadmio
http://www.splabor.com.br/eletrodos/eletrod o-on-seletivo/eletrodos-on-seletivoamonia-brometo-cadmio.html
12