1.b Sedimentacijske Metode
-
Upload
aleksandra-radonjic -
Category
Documents
-
view
88 -
download
3
description
Transcript of 1.b Sedimentacijske Metode
• centrifugiranje– razdvajanje molekula na temelju razlika u taloženju pri povećanoj gravitacijskoj sili
• precipitacija (taloženje)
Sedimentacijske metode
• precipitacija (taloženje)– razdvajanje molekula na osnovi različite topljivosti pri promjeni uvjeta u otopini
Teorijske osnove centrifugiranja
centrifugalno polje (G) = ϖϖϖϖ2rϖϖϖϖ = kutna brzina rotora (radian/s)
r = polumjer rotora (u cm)
preračunato u okretaje u minuti
ili kao višekratnik gravitacijskog polja Zemlje (xg)
ϖπ
2 okret min
-1
=
60G
4 (okret min )-1 2
=π
2
3600
r
RCS 4 (okret min )
(1.11 10 )(okret min )
-1 2
-5 -1 2
=
×
= ×
π2
3600 980
r
r
Podjela centrifugiranja prema namjeni
• analitičko centrifugiranje– mjeri fizikalna svojstva tvari koje sedimentiraju
• koeficijent sedimentacije S– jedinica je Svedberg (S) = 10-13 sec
– omjer brzine sedimentacije (v ; dr/dt) i centrifugalne – omjer brzine sedimentacije (v ; dr/dt) i centrifugalne sile (ω2r)
• preparativno centrifugiranje
rSv2
ω×=r
vS
2ω
=
Podjela centrifugiranja prema brzini
• ultracentrifuguranje– više od 20.000 okretaja/min
• centrifugiranje niske brzine– manje od 10.000 okretaja/min
•centrifugiranje visoke brzine
–10.000 do 20.000 okretaja/min
Diferencijalno centrifugiranje
• uzorak pravilno raspoređen u cijeloj epruveti– nakon centrifugiranja razdvajamo supernatant i talog
• sastav taloga ovisi o brzini i vremenu centrifugiranja– uvijek kontaminiran česticama koje su se nalazile u – uvijek kontaminiran česticama koje su se nalazile u dnu epruvete prije početka centrifugiranja
mala brzina
veća brzina
velikabrzina
najvećabrzina
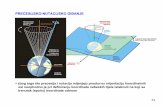
Zonalno centrifugiranje
• uzorak se nanosi u tankom sloju na vrh epruvete ispunjene gradijentom gustoće
• pod djelovanjem centrifugalne sile čestice sedimentiraju ovisno o svom obliku i gustoći
• centrifugiranje prekidamo prije no što čestice • centrifugiranje prekidamo prije no što čestice stignu do dna epruvete
Izopikničko centrifugiranje
• gradijent obuhvaća cijeli raspon gustoća čestica koje želimo razdvojiti
• uzorak je jednoobrazno raspoređen u epruveti
• gradijent nastaje pod djelovanjem centrifugalne sile na čestice u mediju (npr. CsCl)sile na čestice u mediju (npr. CsCl)
• čestice se zaustavljaju na mjestu gdje je njihova gustoća jednaka gustoći medija
Osnovni tipovi rotora za centrifugiranje
• sa stalnim kutem
– fixed angle
• ljuljajuće košarice
– swinging bucket– swinging bucket
• uspravni
– vertical tube
Precipitacija (taloženje)
• razdvajanje molekula na osnovi različite topljivosti pri promjeni uvjeta u otopini
• usoljavanje (salting in)– povećanje topljivosti proteina dodatkom soli
– talože se pri maloj ionskoj jakosti
• isoljavanje (salting out)• isoljavanje (salting out)– taloženje povišenjem ionske jakosti
• taloženje organskim otapalima
• taloženje selektivnom denaturacijom– temperatura
• afinitetno taloženje– umrežavanje specifičnim reagensima (protutijela, lektini)
Isoljavanje (salting out)
• uklanjanje proteina iz otopine povišenjem koncentracije soli
• razmjerno kompleksna teorija– uređenje molekula vode oko hidrofobnih područja
– kompeticija za slobodne molekule vode
– agregacija i precipitacija proteina– agregacija i precipitacija proteina
hidrofobno područje na
proteinu
molekule vode
Svaki protein se taloži u uskom rasponu koncentracije soli.
Taloženje amonij-sulfatom
• prednosti amonij-sulfata– dobra topljivost (4 mol/l)– prihvatljiva gustoća zasićene otopine (1.235 g/ml)– prihvatljiva cijena– koncentrira proteine u uzorku– stabilizira većinu proteina– stabilizira većinu proteina
• nedostaci amonij-sulfata– neprikladan iznad pH 8
• natrij-citrat
– prisutnost teških metala (ppm) • EDTA u otopini
– potrebno ga je naknadno ukloniti • dijaliza, gel filtracija
Primjer taloženja amonij-sulfatom
raspon %
zasićenja
% istalož.
enzima
% istalož.
proteina
obogaćenje
prvi
pokušaj
0-40
40-60
60-80
80 supern.
4
62
32
2
25
22
32
21
2.8
1.0
Zaključak: enzim se većinom istaložio u rasponu 40-60% Zaključak: enzim se većinom istaložio u rasponu 40-60%
drugi
pokušaj
0-45
45-70
70 supern.
6
90
4
32
38
30
2.4
Zaključak: dobro iskorištenje (prinos); slabije obogaćenje
Treći
pokušaj
0-48
48-65
65 supern.
10
75
15
35
25
40
3.0
Nakon taloženja amonij-sulfatom potrebno je ukloniti višak iona
dijaliza gel-filtracija
Ione amonij-sulfata nije potrebno uklanjati ako nakon taloženja planiramo kromatografiju hidrofobnih interakcija.
Taloženje organskim otapalima
• složena teorija– smanjenje aktivnosti vode– slično izoelektričnom taloženju– hidrofobne interakcije manje važne– veće molekule se talože ranije
• svojstva otapala– moraju se potpuno miješati s vodom– moraju se potpuno miješati s vodom– moraju biti nereaktivna i neotrovna – uglavnom etanol i aceton
• pri niskim temperaturama– efikasnije taloženje– manja denaturacija proteina
• oprez pri izražavanju postotaka– 50 ml H2O + 50 ml aceton = 95 ml
Afinitetno taloženje (imunoprecipitacija)Protein G i protein A
• protein G – 6,5 kD aprotein iz soja Streptococcus• protein A – 40-60 kDa protein iz soja Staphylococcus
• površinski proteini bakterija
• velik afinitet vezanja imunoglobulina (Fc regiju)
Table 1. Relative Affinity of Immobilized Protein A for Various Antibody Species and Subclasses1-4. Note: These conditions may vary somewhat based on the salt concentration of the same sample and/or buffer.
Species/Subclass Protein A Protein G
Human IgG1 High High
Human IgG2 High High
Human IgG3 Mod. High High
Human IgG4 Mod. High High
Rabbit IgG High High
Mouse IgG1 Low High
Mouse IgG2a Moderate High
Mouse IgG2b Mod. High High
Mouse IgG3 High High
Rat IgG1 Low Moderate
Table 2. Recommended Column Volumes for Different Antibody Sources
Antibody SourceRecommended bed volume
per ml starting material
Immune Serum 2 ml
Tissue Culture Supernatant (with 10% fetal bovine serum) 0.2 ml
Tissue Culture Supernatant (serum-free) 0.01 ml
Ascites Fluid 2 ml
Rat IgG2a Low High
Rat IgG2b Low Low
Rat IgG2c High High
Goat IgG Low High