Versuchsprotokoll: Fehling: reduzierende und nicht ... · PDF filesaccharid, so wird der...
Click here to load reader
Transcript of Versuchsprotokoll: Fehling: reduzierende und nicht ... · PDF filesaccharid, so wird der...

Versuchsprotokoll: Fehling-Disaccharide
Zeitaufwand:
Vorbereitung: 5 Minuten
Durchführung: 10 Minuten
Abbau/Entsorgung: 5 Minuten
Chemikalien:
Chemikalie Menge R-Sätze S-Sätze Gefahrensymbol Schul-
einsatz
Kupfersulfat-
Pentahydrat
CuSO4*5H2O
3,5 g 22-36/38-
50/53 22-60-61
SI + SII
Kalium-Natrium-
Tartrat
K+/Na+ [C4H4O6]2-
17,5 g - 22-24/25 - SI + SII
Natriumhydroxid
NaOH 6 g 35 26-37/39-45
SI + SII
Saccharose
C12H22O11
Spatel-
spitze - - - SI + SII
Lactose
C12H22O11
Spatel-
spitze - - - SI + SII
Maltose
C12H22O11
Spatel-
spitze - - - SI + SII
Trehalose
C12H22O11
Spatel-
spitze - - - SI + SII

Versuchsprotokoll: Fehling: reduzierende und nicht-reduzierende Zucker
2
Herstellen der Fehling-Lösungen:
Fehling-1-Lösung :
3,5 g CuSO4*5 H2O in 50 mL Wasser lösen
Fehling-2-Lösung:
17,5 g K- Na- Tartrat und 6,0 g NaOH in 50 mL Wasser lösen
Unmittelbar vor der Durchführung des Versuchs müssen Fehling-1-Lösung und Fehling-2-
Lösung im Verhältnis 1:1 gemischt werden.
Materialien:
- Heizplatte
- Becherglas (2x)
- Reagenzgläser (4x)
- Schliffflaschen (2x) (für die Fehling-Lösungen)
- Reagenzglasgestell
Versuchsaufbau:
Durchführung:
Verschiedene Zucker heißes Wasser
Fehling-Lösung (1+2 gemischt)
1. Lösen in heißem Wasser 2. Zugabe von Fehling-Lösung
Blindprobe
Abb.1 Versuchsaufbau

Versuchsprotokoll: Fehling: reduzierende und nicht-reduzierende Zucker
3
1. In die Reagenzgläser wird je eine Spatelspitze eines Disaccharids gegeben.
2. Die verschiedenen Zucker werden nun in heißem, nicht kochendem Wasser gelöst.
3. In die heißen Zuckerlösungen werden etwa 5-10 mL der zuvor gemischten Fehling-
Lösung gegeben.
Sicherer ist das Arbeiten mit kalten Zuckerlösungen, die dann in ein warmes Wasserbad ge-
stellt werden! (Die angewandte Variante eignete sich besser zum Filmen von Videos.)
Beobachtung:
Die Lösungen von Maltose und Lactose verfärben sich nach der Zugabe von Fehling-Lösung
von blau über gelblich-braun nach orange-rot, während bei der Saccharose-Lösung, wie
auch bei der Trehalose-Lösung, keine Farbveränderung zu erkennen ist und die Lösung blau
bleibt.
Entsorgung:
Die mit Fehling-Lösung untersuchten Zucker-Lösungen werden neutral in den anorganischen
Abfall entsorgt.
Auswertung:
Abb.2 Versuchsbeobachtung

Versuchsprotokoll: Fehling: reduzierende und nicht-reduzierende Zucker
4
Disaccharide sind die einfachsten Polysaccharide, die aus zwei Monosacchariden bestehen.
Die beiden Monosaccharide sind dabei über eine glykosidische Bindung von einer Hydroxy-
Gruppe des einen Monosaccharids mit der Hydroxy-Gruppe des anomeren Kohlenstoffatoms
eines anderen Monosaccharids verknüpft.1 Diese Verknüpfung findet über den Mechanismus
einer Acetalbildung statt, welcher in Abb.3 beispielhaft an der Bildung von Fructose aus den
beiden Monosacchariden α-D-Glucose und β-D-Fructose gezeigt wird.2
1 Streitwieser, A. & Heathcock, C.H. & Kosower, E.M. (1994) S.946
2 Mechanismus: Vgl. Vollhardt, K.P.C. & Schore N. E. (2005) S.875
Abb.3 Acetalbildung am Beispiel der Bildung von Saccharose
O
O
HH
H
OH
OH
H OH
H
OH
H
H+
O
O+
HH
H
OH
OH
H OH
H
OH
H
H
- H2O O
C+
HH
H
OH
OH
H OH
H
OH
O+
HH
H
OH
OH
H OH
H
OH
+
H+
-
-D-Glucose
-D-Fructose
Saccharose
O
HH
H
OH
OH
H OH
H
OH
O+
O H
H
OH
OH
H
OH
OHH
O
HH
H
OH
OH
H OH
H
OH
O
O H
H
OH
OH
H
OH
OH
H
O
O
OH
H
H
OH
H
OH
OH

Versuchsprotokoll: Fehling: reduzierende und nicht-reduzierende Zucker
5
Die systematische Benennung der Disaccharide ist durch die beteiligten Monosaccharide,
deren Ringform (α oder β bzw. Fünf- oder Sechsring) sowie die Art der Verknüpfung zwi-
schen den beiden Monosacchariden charakterisiert.3
Konventionsgemäß wird der Name der Di- und auch Oligosaccharide ausgehend von dem
linken, nicht reduzierenden Ende beschrieben und dann folgendermaßen aufgebaut:4
1. Zuerst wird die Konfiguration (α oder β) des anomeren Kohlenstoffatoms angegeben,
das die erste (linke) Monosaccharid-Einheit mit der zweiten verbindet.
2. Nun wird der nicht-reduzierende (linke) Zucker benannt und dabei auch zwischen
Sechs- und Fünfring durch die Endung „-pyranosyl“ bzw. „-furanosyl“ unterschieden.
3. Danach werden in Klammern die beiden durch die glycosidische Bindung miteinander
verbundenen Kohlenstoffatome angegeben. (1,4) bedeutet also, dass das Kohlens-
toffatom C1 des zuerst genannten Zuckerrestes mit dem Kohlenstoffatom C4 des
zweiten Zuckerrestes verbunden ist.
4. Zuletzt wird der zweite Rest genannt. Handelt es sich dabei um ein reduzierendes Di-
saccharid, so wird der Zucker mit der Endung „-ose“ ausgeschrieben und es muss
keine Konfiguration (α- oder β-) vorangestellt werden. Im Falle eines nicht-
reduzierenden Disaccharids muss die Konfiguration angegeben werden und der Zu-
cker erhält anstatt der Endung „-ose“ die Endung „-id“.
Um erklären zu können, warum manche Disaccharide eine positive Fehling-Probe aufweisen
und andere nicht, muss die Art der Verknüpfung zwischen den beiden Monosacchariden
betrachtet werden. Sind die beiden Monosaccharide über ihre jeweiligen anomeren Kohlens-
toffatome verknüpft, so ist die Fehling-Probe negativ und im Versuch fällt kein rotes Kupfer-
oxid aus. Diese Zucker werden auch nicht reduzierende Zucker genannt, da sie keine re-
duzierenden Eigenschaften aufweisen. Des Weiteren ist bei diesen nicht reduzierenden Zu-
ckern keine Mutarotation festzustellen. Ist bei einem der beiden Monosaccharid-Einheiten
eines Disaccharids das anomere Kohlenstoffatom nicht an der glykosidischen Bindung betei-
ligt, so hat dieser Zucker reduzierende Eigenschaften und wird als reduzierender Zucker
bezeichnet (im Versuch reduziert er die Kupferionen). Zusätzlich ist bei diesen reduzieren-
den Zuckern eine Mutarotation zu beobachten.
Zum besseren Verständnis werden im Folgenden die im Versuch verwendeten Disaccharide
vorgestellt und die reduzierenden- bzw. nicht reduzierenden Eigenschaften erläutert:
3 Voet, D. & Voet, J. G. & Pratt, C. W. (2002) S. 218
4 Nelson, D. & Cox, M. (2009) S.322

Versuchsprotokoll: Fehling: reduzierende und nicht-reduzierende Zucker
6
Abb.5 Saccharose: -D-Glucopyranosyl-(1,2)--DFructofuranosid
1
2
3
4
5
6
OH
O
H OH
OH H
H OH
H OH
-D-GlucopyranoseD-Glucose
5 O
1
23
4
OH
H
HH
OH
OH
H OH
H
6OH
* 3
4
5
6
OH
OH H
H OH
H OH
2
1OH
O
4 3
2O
5
OH
1
H
OH
OH
H
6
H
OH
OH
*
D-FructofuranoseD-Fructose
* = anomeres Zentrum
1. Saccharose:
Die Saccharose ist das am häufigsten vorkommende Disaccharid und ist die Haupttransport-
form von Kohlenhydraten in Pflanzen.5 Für uns Menschen ist die Saccharose als der ge-
wöhnliche Haushaltszucker bekannt. Kommerziell wird die Saccharose aus Rohrzucker oder
Zuckerrüben gewonnen.
Die systematische Bezeichnung der Saccharose lautet α-D-Glucopyranosyl-(1,2)-β-D-
Fructofuranosid. Dies bedeutet, dass sich die Saccharose aus einem Molekül α-D-Gluco-
pyranose und einem Molekül β-D-Fructofuranose zusammensetzt (Abb.4).
Wie man in Abb.4 erkennen kann, befindet sich das anomere Kohlenstoffatom der Glucopy-
ranose an Kohlenstoffatom C1, während sich im Falle der Fructose das anomere Kohlens-
toffatom an Position C2 befindet. Anhand der systematischen Bezeichnung kann man erken-
nen, dass die Saccharose gerade über diese beiden anomeren Kohlenstoffatome verknüpft
ist (Abb.5).
5 Voet, D. & Voet, J. G. & Pratt, C.W. (2002) S.219
5 O
1
23
4 HH
H
OH
OH
H OH
H
6OH
O 3 4
5
O
2
H
6
H
OH
OH
H
1
OH
OH
Abb.4 Ringschluss von Glucose und Fructose

Versuchsprotokoll: Fehling: reduzierende und nicht-reduzierende Zucker
7
Aufgrund der Beteiligung der beiden anomeren Kohlenstoffatome an der glykosidischen Bin-
dung schützen die beiden cyclischen Acetalgruppen sich gegenseitig und eine Ringöffnung
wird verhindert.6 Da jedoch die offenkettige Form die Voraussetzung für reduzierende Eigen-
schaften der Zucker ist und auch die Mutarotation über die offenkettige Form stattfindet, ge-
hört die Saccharose zu den nicht reduzierenden Zuckern.
2. Lactose:
Das in der Natur am zweithäufigsten vorkommende Disaccharid ist die Lactose. In der Natur
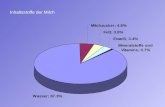
kommt die Lactose nur in Milch vor, weshalb Lactose auch „Milchzucker“ genannt wird. Da-
bei beträgt der Anteil der Lactose in der Muttermilch der meisten Säugetiere etwa fünf Ge-
wichtsprozente der flüssigen Milch. Bei den Trockensubstanzen der Milch beträgt der Lacto-
se-Anteil etwa ein Drittel.7 Kommerziell wird die Lactose aus Molke, einem Nebenprodukt der
Käseherstellung, gewonnen. Dabei fällt beim Evaporieren der Molke bei Temperaturen unter
95 °C das weniger lösliche α-Anomer aus.8
Die systematische Benennung der Lactose lautet β-D-Galactopyranosyl-(1,4)-D-Gluco-
pyranose. Dies bedeutet, dass die Lactose aus einer β-D-Galactopyranose- und einer D-
Glucopyranose-Einheit besteht (Abb.6).
Glucose: s. oben
6 Vollhardt, K.P.C. & Schore, N.E. (2005) S.1287
7 Vollhardt, K.P.C. & Schore, N.E. (2005) S.1290
8 Streitwieser, A. & Heathcock, C.H. & Kosower, E.M. (1994) S.947
1
2
3
4
5
6
OH
O
H OH
OH H
OH H
H OH
5 O
1
23
4
H
HH
OH
H
OH
H OH
OH
6
OH
*
Galactose -D-Galactopyranose
Abb.6 Ringschluss Galactose

Versuchsprotokoll: Fehling: reduzierende und nicht-reduzierende Zucker
8
Man kann erkennen, dass sich das anomere Kohlenstoffatom der Galaktose an Kohlenstoff-
atom C1 befindet. Wie bereits bei der Saccharose beschrieben, ist das anomere Kohlens-
toffatom der Glucose ebenfalls am Kohlenstoffatom C1. Am systematischen Namen ist zu
erkennen, dass die Lactose über das Kohlenstoffatom C1 der Galactopyranose mit dem Koh-
lenstoffatom C4 der Glucopyranose verknüpft ist (Abb.7).
Abb.7 zeigt, dass das anomere Kohlenstoffatom der Glucopyranose nicht an der glykosi-
dischen Bindung beteiligt ist. Aus diesem Grund kann sich der Ring an dieser Stelle wieder
öffnen. Das bedeutet zum einen, dass dieser Zucker in Lösung auch in der offenkettigen
Form vorliegt. In dieser Form besitzt dieser Zucker eine Aldehydfunktion, die zur Carbonsäu-
re oxidiert werden kann. Aus diesem Grund weist die Lactose eine positive Fehling-Probe
auf, sie ist ein reduzierender Zucker. Des Weiteren steht die Glucopyranose der Lactose in
Lösung in einem Gleichgewicht zwischen offenkettiger-, α- und β- Form. Die Lactose weist
also Mutarotation auf. Es existiert sowohl eine α- als auch eine β- Form der Lactose (s.
oben).
Abb.7 Lactose: -D-Galactopyranosyl-(1,4)-D-Glucopyranose
O
14
OH
HH
H
O
OH
H OH
H
OH
O
1
H
HH
OH
H
OH
H OH
OH
*
*
O
14
H
HH
H
O
OH
H OH
OH
OH
O
1
H
HH
OH
H
OH
H OH
OH
*
*
-Lactose -Lactose
14
OH
HH
O
OH
H OH
H
OH
O
1
H
HH
OH
H
OH
H OH
OHOH

Versuchsprotokoll: Fehling: reduzierende und nicht-reduzierende Zucker
9
3. Maltose9
Nach der Saccharose und der Lactose ist die Maltose (oder auch Malzzucker) das am häu-
figsten vorkommende natürliche Disaccharid. Die Maltose entsteht aus Stärke und Glykogen,
die unter der Einwirkung des Enzyms Amylase mit einer Ausbeute von etwa 80% in das Di-
saccharid Maltose gespalten werden. So kommt die Maltose in Pflanzenwurzeln und Pflan-
zenknollen, Blättern, in keimenden Getreidesamen und Keimanlagen der Kartoffel vor.
Maltose ist ein Dimer der Glucose und trägt den systematischen Namen α-D-Gluco-
pyranosyl-(1,4)-D-Glucopyranose. Die Maltose besteht also aus zwei Glucose-Einheiten (s.
oben), die über die Kohlenstoffatome C1 und C2 verknüpft sind (Abb.8).
Ähnlich der Lactose ist auch bei der Maltose nur einer der beiden anomeren Kohlenstoffato-
me an der glycosidischen Bindung beteiligt. Das andere anomere Kohlenstoffatom ist nicht
an dieser Bindung beteiligt und kann, ebenso wie die Lactose, eine Ringöffnung vollziehen.
9 Nach: RÖMPP Online, Stichwort “Maltose“ (letzter Zugriff 14.03.10)
Abb.8 Maltose: -D-Glucopyranosyl-(1,4)-D-Glucopyranose
* *
O
1H
HH
OH
OH
H OH
H
OH
O
O
14
H
H
HH
OH
H OH
OH
OH
Maltose
* *
Maltose
O
1HH
H
OH
OH
H OH
H
OH
O
O
14
OH
HH
H
OH
H OH
H
OH
O
HH
H
OH
OH
H OH
H
OH
O O
HH
H
OH
H OH
H
OH
OH

Versuchsprotokoll: Fehling: reduzierende und nicht-reduzierende Zucker
10
4. Trehalose
Trehalose kommt mit einem Massenanteil von 7% an der Trockensubstanz einiger Pilze und
mit einem Anteil von 11% an der Oligosaccharidfraktion in Honig vor. Im Stoffwechsel von
Insekten und anderen wirbellosen Tieren spielt die Trehalose eine ähnliche Rolle wie die D-
Glucose im Organismus der Säugetiere. Des Weiteren ist die Trehalose bei Insektenlarven
und Hefen ein Reservekohlenhydrat.
Gewonnen wird die Trehalose durch die Isolierung aus Hefe, sowie durch enzymatische
Spaltung von Maltose.
Die Trehalose trägt den systematischen Namen α-D-Glucopyranosyl-(1,1)-α-D-Gluco-
pyranosid und ist somit ebenso ein Dimer der Glucose, wie auch die Lactose. Anders als die
Lactose sind die beiden Glucoseeinheiten jedoch über die jeweiligen Kohlenstoffatome C1
verknüpft (Abb.9)
Wie man an der Struktur der Trehalose erkennen kann, sind die beiden anomeren Kohlens-
toffatome an der glykosidischen Bindung beteiligt. Aus diesem Grund sind, wie bei der Sac-
charose, keine Ringöffnungen bei diesem Disaccharid möglich. Dadurch fällt auch die Feh-
ling-Probe negativ aus. Die Trehalose hat keine reduzierenden Eigenschaften und beim Lö-
sen in Wasser findet keine Mutarotation statt. Die Trehalose ist ein nicht reduzierender Zu-
cker und besitzt somit auch keine α- bzw. β-Form.
*O
1H
HH
OH
OH
H OH
H
OH
O
O
1
OH
OH
H
H
OH H
H
OH
*
Abb.9 Trehalose: -D-Glucopyranosyl-(1,1)--D-Glycopyranosid

Versuchsprotokoll: Fehling: reduzierende und nicht-reduzierende Zucker
11
Didaktische Analyse:
Einordnung in den Lehrplan:
s. Versuchsprotokoll: Fehling-Glucose
Einordnung dieses Versuchs:
Durch diesen Versuch können die Schüler anhand der verschiedenen chemischen Eigen-
schaften Rückschlüsse auf die Struktur bzw. die Verknüpfungsarten der verschiedenen Zu-
cker. Dabei kann auf das Vorwissen aus der Carbonyl- und Redoxchemie zurückgegriffen
werden. Der apparative wie auch der zeitliche Aufwand dieses Versuchs sind relativ gering
und die verwendeten Chemikalien dürfen laut „HessGiss“-Datenbank von Schülern der Se-
kundarstufe SI und SII uneingeschränkt verwendet werden. Somit eignet sich dieser Versuch
sowohl als Lehrer-Demonstrationsversuch als auch als Schülerversuch. Im Anschluss an
diesen Versuch könnte die Spaltung eines Disaccharids besprochen werden, was zu einem
besseren Verständnis zu Acetalbindungen führen kann.10
Literaturangaben:
Nelson D. & Cox M. (2009). Lehninger Biochemie (4. Auflage). Berlin Heidelberg: Springer-Verlag.
Streitweiser; A. & Heathcock C.H. & Kosower E.M. (1994). Organische Chemie (2. Auflage). Weinheim: VCH Verlagsgesellschaft mbH.
Voet, D. & Voet J.G. & Pratt C.W. (2002). Lehrbuch der Biochemie (X. Auflage). Weinheim: WILEY-VCH Verlag GmbH & Co. KGaA.
Vollhardt, K.P.C. & Schore N.E. (2005). Organische Chemie (4. Auflage). Weinheim: Wiley-VCH GmbH & Co KGaA.
Elektronische Quellen:
Hessisches Gefahrstoffinfomationssystem Schule „HessGISS“- 2008/2009, Version 13.0
„RÖMPP Online“, Version 3.2, verfügbar unter http://www.roempp.com/prod/index1.html (li-zenzpflichtig, zuletzt abgerufen am 14.03.2010)
Abbildungsverzeichnis:
Alle Abbildungen dieses Protokolls wurden selbst angefertigt.
10 Vgl. hierzu: Versuchsprotokoll Spaltung von Saccharose und Polarimeter: Spaltung von Saccharose