Reaksi Eliminasi t
-
Upload
annik-qurniawati -
Category
Documents
-
view
43 -
download
6
Transcript of Reaksi Eliminasi t

REAKSI ELIMINASI

Mekanisme Reaksi Eliminasi
1. Eliminasi (β) – 1,2
2. Mekanisme E1
3. Mekanisme E1cB
4. Mekanisme E2
5. Eliminasi (α)-1,1
6. Eliminasi Sin Pirolitik

Eliminasi (β) – 1,2

Jenis Mekanisme Reaksi Eliminasi
Mekanisme E2
Mekanisme E1
Mekanisme E1cB

Mekanisme E1
Pada mekanisme E1, zat antara karbonium (5) terbentuk cukup lambat sehingga berperan sebagai penetu laju reaksi (k2 > k1)
Laju = k[MeCH2CMe2Br]

Mekanisme E1 vs SN-1
Karbokation (8) identik dengan zat antara yang terbentuk pada reaksi solvolisis SN-1 menghasilkan produk (9) yang merupakan pesaing produk E1 (7)

Pengaruh Struktur Substrat
Gugus yang dapat memantapkan karbokation :
Laju E1 primer < sekunder < tersier Percabangan pada atom karbon β
mendukung eliminasi E1, sehingga :
eliminasi terhadap MeCH2CMe2Cl menghasilkan 34 % alkena, sedangkan terhadap Me2CHCMe2Cl menghasilkan 62 % alkena.

Regioselektivitas
Ada 2 kemungkinan lepasnya hidrogen β dari zat antara ion karbonium sehingga dapat menghasilkan lebih dari satu macam alkena. Pada reaksi di atas produk (7) lebih melimpah (82 %)

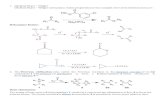
Mekanisme E1cB

Pengaruh Gugus pergi

Mekanisme E2
• Laju = k[CH2CH2Br][B]
• Karena sering kali B merupakan nukleufil selain basa, pada reaksi E2 sering disertai produk SN-2

Faktor yang Mempengaruhi Laju E2
• Pengaruh Kekuatan Basa
• -NH2 > -OR > -OH
• Pergantian pelarut protik polar menjadi aprotik polar meningkatkan kekuatan basa tertentu misalnya -OH dan –OR, karena menurunnya kekuatan solvasi terhadap basa.
• Laju relatif dengan -OEt/EtOH:
PhCH2CH2F PhCH2CH2Cl PhCH2CH2Br PhCH2CH2I
1 70 4,2 x 103 2,7 x 104

Stereoselektivitas Reaksi E2
Melalui konformasi anti-periplanar (24 a) atau sin-periplanar (24 b) ?

Pengaruh Gugus Y
Untuk Y = Br, Ts, atau +NMe3 praktis anti-periplanar, kecuali pada senyawa NR3 rantai panjang.

Eliminasi pada Senyawa Siklik

Pada substrat yang memiliki lebih dari 1 atom hidrogen B dapat diperoleh lebih dari satu alkena
Orientasi Saytzev vs Hofmann

Mengapa terjadi Orientasi Saytzev atau Hofmann?
Saytzef (1875)
Hofmann (1851)

Orientasi Hofmann
• Apabila Y adalah F cenderung produk Hofmann, misalnya pada eliminasi terhadap EtCH2CHFCH3 menghasilkan tidak kurang dari 85% EtCH2CH=CH2
• Meningkatnya kekuatan basa juga meningkatkan produk Hofmann.
• Subtituen Ph, C=C, meningkatkan pembentukan alkena dengan ikatan rangkap terkonjugasi dengannya.


Pengaruh Gugus Y

Pengaruh Basa

Pengaruh Sterik

Zaitsev’s Rule for Elimination Reactions (1875)
• In the elimination of HX from an alkyl halide, the more highly substituted alkene product predominates

Mekanisme E1cB













![Crecimiento óptimo: El Modelo de Cass-Koopmans … · sin consumo y en el segundo sin capital) θ t [] t t c r c σ = −θ ... tt tt t t t t t t. c Hc v w r e w r nv c.](https://static.fdocument.org/doc/165x107/5ba66e0109d3f263508bae94/crecimiento-optimo-el-modelo-de-cass-koopmans-sin-consumo-y-en-el-segundo.jpg)




