Chap V. Le cycle de Krebs énergétique du cycle de Krebs isocitrate déshydrogénase...
-
Upload
nguyenthuy -
Category
Documents
-
view
217 -
download
1
Transcript of Chap V. Le cycle de Krebs énergétique du cycle de Krebs isocitrate déshydrogénase...

Le cycle de KrebsLe cycle de l’acide citriqueLe cycle tricarboxylique
dans les mitochondries conditions AÉROBIES
Acétyl-CoA
CO2
énergie
Voie finale, COMMUNE de l’oxydation des molécules énergétiques : acides aminés, acides gras, glucides
Figures tirées de
Copyright © 2004 by W. H. Freeman & Company
Lehninger Principles of BiochemistryFourth Edition
Chap V.

C6
C6
C5
C4
C4
C4
C4
C4
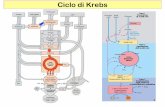
Vue générale du cycle de l’acide citrique

2 carbones entrent dans le cycle, 2 autres carbones en sortent sous forme de CO2
4 réactions d’oxydo réduction ont lieu
- 6 électrons sont transférés sur 3 NAD+
- 1 paire d’atomes d’hydrogène (2 électrons) sont transférés sur FAD
1 liaison phosphate, riche en énergie est formée à chaque tour (1 GTP)
Régénération de NAD+ et de FAD conduit à la formation de 3 ATP et de 2 ATP respectivement, dans la chaîne respiratoire
3×3 + 1×2 + 1×1 = 12 ATP

Vue détaillée du cycle de l’acide citrique

CCOO-
CH2
COO-
CH3C
O
S-CoA
C COO-HO
CH2
COO-
COO-
CH2
C COO-HO
CH2 COO-
CH2 S-CoAC
O
1. Condensation de l’oxaloacétate et de l’acétyl coenzyme A
Oxaloacétate
+
Acétyl-CoA
+ H2O
Citrate synthétase
Acide citrique
+ HS-CoA + H+
Intermédiaire = Citryl-CoA
I. Les 9 étapes en détail

2. + 3. Isomérisation du citrate
COO-
C
OH
CH2
-OOC
H H
C
COO-
COO-
C OH
CH2
-OOC
H
HC
COO-
COO-
C
CH2
-OOC
H
C
COO-
Citrate Cis-Aconitate Isocitrate
aconitase aconitase
H2O H2O

4. Oxydo-réduction I
isocitrate + NAD+ α-cétoglutarate + CO2 + NADH + H+
COO-
CH2
H C COO-
COO-
CH OH
COO-
CH2
H C COO-
COO-
C O
COO-
CH2
COO-
C O
CH2
Isocitrate Oxalosuccinate α-cétoglutarate
Isocitrate déshydrogénase
H+ CO2NAD+
NADH + H+

5. Décarboxylation oxydative
α-cétoglutarate + NAD+ + CoA succinyl-CoA + CO2 + NADH
COO-
CH2
COO-
C O
CH2
COO-
CH2
C O
CH2
S-CoA
+ NAD+ + HS-CoA + CO2 + NADH + H+
Enz = complexe α-cétoglutarate déshydrogénase
Cofacteurs = NAD+, CoA, TPP, lipoamide, FAD

6. Formation d’une liaison riche en énergie
succinyl~CoA + Pi + GDP succinate + GTP + CoASuccinyl CoA synthétase
Transfert sur ADP
GTP + ADP GDP + ATP
Nucléoside diphosphate kinase
7. Régénération de l’oxaloacétate
COO-
CH2
CH2
COO-
COO-
CH
HC
COO-
+ FAD + FADH2
fumaratesuccinate
succinate déshydrogénase

8. COO-
CH
HC
COO-
COO-
C
CH2
COO-
HO H
COO-
C
CH2
COO-
HO H
COO-
CH2
COO-
C O
fumarate L-malate
fumarase(trans addition
stéréospécifique)
9.
+ NAD+ + NADH + H+
L-malate oxaloacétate
malate déshydrogénas
e

Acétyl-CoA + 2 H2O + 3 NAD+ + FAD + GDP + Pi
2 CO2 + 3 NADH + FADH2 + GTP + 2 H+ + CoA
acétyl-CoA + oxaloacétate + H2O citrate + CoA + H+
citrate cis-aconitate + H2O
cis-aconitate + H2O isocitrate
isocitrate + NAD+ α-cétoglutarate + CO2 + NADH
α-cétoglutarate + NAD+ + CoA succinyl-CoA + CO2 + NADH
succinyl-CoA + Pi + GDP succinate + GTP + CoA
succinate + FAD (lié) fumarate + FADH2 (lié)
malate + NAD+ oxaloacétate + NADH + H+
fumarate +H2O malate
II. Bilan du cycle de l’acide citrique

Bilan énergétique du cycle de Krebsisocitrate déshydrogénase
α-cétoglutarate déshydrogénase
succinyl CoA synthétase
succinate déshydrogénase
malate déshydrogénase
1 NADH formé
1 NADH formé
1 GTP formé
1 FADH2 formé
1 NADH formé
3 liaisons ~
3 liaisons ~
3 liaisons ~
1 liaison ~
2 liaisons ~
12 liaisons ~

entrée du pyruvate dans la mitochondrie (cf. avant)
devenir des atomes de C :S-CoA
+CO2
CO2 α-cétoglutarate
isocitrate
citrate
succinyl-CoA
succinate
oxaloacétate
III. Particularités et mécanismes

complexe de l’α-cétoglutarate déshydrogénase
Très semblable au complexe pyruvate déshydrogénase
Mêmes cofacteurs : TPP, lipoamide, CoA, FAD, NAD+
3 enzymes :A’ : α-cétoglutarate déshydrogénaseB’ : transsuccinylaseC’ : dihydrolipoyl déshydrogénase
C’BA
CBA
CB’A’
C’B’A’
Complexes fonctionnels

La citrate synthétaseoxaloacétate + acétyl-CoA citrate + CoA
- enzyme = 2 monomères en interaction- (a) = enzyme sans substrat- (b) = enzyme avec substrats changement conformationnel, le site actif « se referme »- présence d’histidines dans le site actif qui stabilisent les différents intermédiaires

L’aconitase• Aspect structural :
COO-
C
HO
CH2
COO-
H2
C
COO-
COO-
C
CH2
COO-
H
C
COO-
COO-
C
CH2
COO-
H
C
COO-
COO-
CHO
CH2
COO-
H
HC
COO-
COO-
C OH
CH2
COO-
H
HC
COO-
ou
cis aconitate
isocitrate
ou
1
2
3
5
4
1
2
3
5
4
1
2
3
5
4
1
2
3
5
4
citrate
A B

Comment l’enzyme peut elle être spécifique sur une molécule symétrique
•
••
Molécule symétrique reconnue de manière asymétrique
Site OH
CH2COO-Site
Site COO-
CH2COO-

• Aspect fonctionnel : Dichapetelum cymosum
Aconitase inhibée par fluoroacétate
Site OH
Site
Site COO-
CH2COO-
COO-
C
HO
C
COO-
H2
C
COO-
HF
COO-
CH2 F F CH2
O
CS-CoA
CoA-SH
fluoroacétate fuoroacétyl CoAoxaloacétate
fluorocitrateAconitase
Fe2+
Fluor Blocage

IV. Régulation du cycle de Krebs

Régulation du cycle :
Complexe pyruvate déshydrogénase :• Acétyl-CoA inhibe la transacétylase
• NADH inh. Dihydrolipoyl déshydrogénase
P si élevés
• déphosphorylation si pyruvate élevé
ATP, NADH, Acétyl-CoAADP NAD+ CoA
• modification covalente : P de Ser
Citrate synthétase :
• inhibée allostériquement par ATP
(ATP baisse l’affinité de l’enzyme par l’Acétyl-CoA)

Isocitrate déshydrogénase :
• stimulation allostérique par ADP
(ADP augmente l’affinité pour les substrats)
• NADH inhibe l’enzyme car déplace le NAD+
α-cétoglutarate déshydrogénase :
• inhibition par succinyl-CoA et par NADH
Résumé : si taux énergétique cellulaire élevé, vitesse du cycle et vitesse d’incorporation de C2 réduites

V. Le cycle de l’acide citrique : source de précurseurs

Remarques :
• Dans situation alimentaire désespérée : voie néoglucogenèse : oxaloacétate glucides (glucose pour
le cerveau)
• Compensation par réactions anaplérotiques :
Ex : pyruvate + CO2 + ATP + H2O
oxaloacétate + ADP + Pi + 2 H+
pyruvate carboxylase

paralysie / tremblement mains + pieds, parfois tout le corps
provoqué par carence en vitamine B1 = thiamine
TPP = groupe prosthétique de 3 enzymes importants
• pyruvate déshydrogénase
• α-cétoglutarate déshydrogénaseCycle de Krebs
• transcétolasesVoie des pentoses
Activités enzymatiques faibles
Extrême Orient / riz, faible teneur en vit. B1
VI. Cycle de Krebs et Béribéri

VII. Le cycle glyoxylique
Bilan : 2 Acétyl-CoA + NAD+ + 2 H2O succinate + 2 CoA + NADH + H+
Remarque : Acétate + CoA + ATP Acétyl-CoA + AMP + PPi
Oxaloacétate
Citrate
Acétyl-CoA
CoASH
Isocitrate
CO2
α-cétoglutarate
Succinyl CoA
Succinate
Fumarate
Isocitrate lyase
Glyoxylate
Malate synthase
Acétyl-CoA
CoASH
MalateGlucose
NAD+
NADH + H+
Malate déshydrogénase
CO2