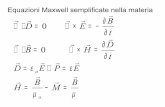Potenciales termodinámicos y relaciones de Maxwell - BUAPlilia/estad16/potenciales.pdf ·...
Transcript of Potenciales termodinámicos y relaciones de Maxwell - BUAPlilia/estad16/potenciales.pdf ·...

Potenciales termodinámicos y relaciones de Maxwell
Física Estadistica Lilia Meza Montes Primavera 2016

Procesos reversibles infinitesimales
dU = d 'Q+ d 'W
= d 'Q+ XidYii=1∑ + µ j
j=1
ν
∑ dN j
Primera Ley de la Termodinámica: Conservación de la energía
TQddS '
=
Segunda Ley función de punto S (entropía) Si no está aislado y proceso
cuasiestático infinitesimal en el cual se absorbe la cantidad de calor d’Q
T temperatura absoluta del
sistema.

Motivación
¡ En Mecánica, trabajo se almacena en energía potencial y se puede sustraer después.
¡ Similarmente en sistemas termodinámicos, en forma de energía libre
¡ Diferentes formas, según restricciones

Ecuación fundamental de la termodinámica
¡ Variables Xi,Yi ¡ Temperatura T ¡ Funciones de punto U y S ¡ Sistemas químicos
dU = TdS + XidYii=1∑ + µ j
j=1
ν
∑ dN j

Transfomación de Legendre
• f(x,y) à g(u,y) • g = f – ux
Primeras derivadas
Segundas derivadas: Respuesta
• Calor específico • Coeficientes κ,β
Relaciones de Maxwell
Teoremas
• Restricciones a proceso
• Condición de estabilidad ( ) ( ) dydudg
xduudxdfdgvdyudxdf
uyg
yug
∂∂
∂∂ +=
−−=
+=
yu uN
yM
NdyMdudg
⎟⎠
⎞⎜⎝
⎛∂∂
=⎟⎟⎠
⎞⎜⎜⎝
⎛
∂∂
+=
Transformaciones de Legendre

Ejemplo: U(S, X, {Nj})
dU ≤ TdS + XidYii=1∑ + µ j
j=1
ν
∑ dN j
¡ Igualdad para procesos reversibles ¡ Es un potencial para procesos reversibles,
sistema aislado y cerrado a X y {Nj} fijos. ¡ Cambio en U es el máximo trabajo que
puede ser hecho por o sobre el sistema
dU = TdS + XidYii=1∑ + µ j
j=1
ν
∑ dN j

¡ Si no se realiza trabajo (por o sobre el sistema), no hay intercambio de materia con alrededores y la entropía no cambia
¡ La energía interna no cambia
(reversible), disminuye (espontáneo)
(dU)S,X,{Nj} ≤ 0

Más consecuencias
∂T∂X"
#$
%
&'S,{Nj}
=∂Y∂S"
#$
%
&'X,{Nj}
, ∂T∂Nj"
#$
%
&'S,X,{Ni,i≠ j}
=∂µ j
∂S"
#$
%
&'X,{Nj}
¡ Primeras derivadas
¡ Función de punto (diferencial exacta)à derivadas cruzadas: Relaciones de Maxwell
T = ∂U∂S
"
#$
%
&'X,{Nj}
,Y = ∂U∂X"
#$
%
&'S,{Nj}
,µ j =∂U∂N j
"
#$$
%
&''S,X,{Ni,i≠ j}

Funciones de respuesta térmica
¡ Capacidad Calorífica
CX,{Nj} =∂U∂T"
#$
%
&'X,{Nj}
,CY ,{Nj} =∂U∂T"
#$
%
&'Y ,{Nj}
CY ,{Nj} =CX,{Nj} +∂U∂X"
#$
%
&'T ,{Nj}
−Y)
*+
,
-.∂X∂T"
#$
%
&'Y,{Nj}

Funciones de respuesta mecánica ¡ Compresibilidad
(Susceptibilidad) isotérmica
¡ Compresibilidad adiabática
¡ Coeficiente de dilatación o expansión térmica
κT ,{Nj} =∂X∂Y"
#$
%
&'T ,{Nj}
,
κS,{Nj} =∂X∂Y"
#$
%
&'S,{Nj}
,
βY ,{Nj} =∂X∂T"
#$
%
&'Y ,{Nj}
CY ,{Nj}
CX,{Nj}
=κT ,{Nj}
κS,{Nj}

Entalpía H= H(S,Y, {Nj}) (S, X, {Nj})à (S,Y, {Nj}) Transformación de U: agregar –XY
H =U − XY = ST + µ jj=1
ν
∑ dN j
dH ≤ TdS − XdY + µ jj=1
ν
∑ dN j
Si sistema térmicamente aislado y cerrado à S,Y, {Nj} constantes (Pero acoplado a alrededores mecánicamente)
dH ≤ 0 No hay cambio espontáneo, estado de equlibrio es el de entalpía mínima

Primeras derivadas
T = ∂H∂S
"
#$
%
&'Y ,{Nj}
,X = − ∂H∂Y"
#$
%
&'S,{Nj}
,µ j =∂H∂N j
"
#$$
%
&''S,Y ,{Ni,i≠ j}
∂T∂Y"
#$
%
&'S,{Nj}
= −∂X∂S"
#$
%
&'Y ,{Nj}
, ∂T∂Nj"
#$
%
&'S,Y ,{Ni,i≠ j}
=∂µ j
∂S"
#$
%
&'Y ,{Nj}
Relaciones de Maxwell

Funciones de respuesta mecánica ¡ Compresibilidad
adiabática
κS,{Nj} =∂X∂Y"
#$
%
&'S,{Nj}
= −∂2H∂Y 2"
#$
%
&'S,{Nj}

Funciones de respuesta mecánica ¡ Compresibilidad
(Susceptibilidad) isotérmica
¡ Compresibilidad adiabática
¡ Coeficiente de dilatación o expansión térmica
κT ,{Nj} =∂X∂Y"
#$
%
&'T ,{Nj}
,
κS,{Nj} =∂X∂Y"
#$
%
&'S,{Nj}
,
βY ,{Nj} =∂X∂T"
#$
%
&'Y ,{Nj}
CY ,{Nj}
CX,{Nj}
=κT ,{Nj}
κS,{Nj}

Funciones termodinámicas: sistema cerrado

Regla mnemoténica
p V
H S
G F T
E(=U)
Orden funciones : sentido contrario manecillas E, F, G, H Variables naturales: las que están a los lados Signos en diferencial: + si en dirección de flecha, - caso contrario Ejemplo: G= G( T,p) dG= -S dT + V dp
Thermodynamics, R. Kubo

Características
F = U-TS G =F +pV H = U +pV
H, U, S
U , S H, F, G F, G extensivas extensivas Funciones de estado
Funciones de estado
Unidades de energía
Unidades de energía
Criterio de cambio espontáneo. Medida de trabajo útil. Criterio de equilibrio

Criterio de equilibrio
¡ De la desigualdad de Clausius (d’Q/T <dS) y primera Ley
dU-d’W=d’Q à dU-d’W<TdS à dU – TdS – d’W < 0 Ejemplo: sistema hidrostático (realiza trabajo) dU – TdS + pdV < 0

Criterio de equilibrio
Para variaciones virtuales, el criterio de equilibrio para un sistema cerrado es
δS≤δQ/T o bien δU – TδS + pδV ≥ 0. Si δZ= δU – TδS + pδV à δZ≥0 criterio de equilibrio Igualdad para procesos reversibles. Depende de las restricciones. El criterio puede expresarse en términos de potenciales
termodinámicos

Condiciones de equilibrio de un sistema cerrado
Variables naturales
Función termodinámica
Proceso/característica/estabilidad (criterio de equilibrio)
E, V Entropía S Sistema aislado/S no puede disminuir/S máxima/ (δS)E,V ≤0
S,V Energía interna (U,E)
(δE)S,V ≥0
S,P Entalpía H Isobárico/ ΔH=QP/ (δH)S,P≥0
T,V Energía libre de Helmoltz (A,F)
Reversible, solo Q con alrededores, isocórico/ F no puede aumentar/F mínima/ (δF)T,V≥0
T,P Energía libre de Gibbs G
Isotérmico-isobárico/G no puede aumentar/G mínimo/ (δG)T,P≥0
Procesos reversibles obedecen el criterio. Una transformación espontánea (irreversible) puede ocurrir si la función cambia en forma contraria al criterio. Ejemplo, si G disminuye.

Ecuaciones de Gibbs-Helmholtz
Los potenciales termodinámicos no son indepedientes entre sí, existen relaciones entre ellos
F = F(V,T)
),(
),(
),(
TVUTGTG
TVHTGpG
TVUTFTF
p
p
V
=⎟⎠
⎞⎜⎝
⎛∂∂
−
=⎟⎠
⎞⎜⎝
⎛∂∂
−
=⎟⎠
⎞⎜⎝
⎛∂∂
−

EJEMPLOS

Entalpía y Entropía
Entalpía de Cd Entropía de Mg a 1 atm
o Estado estandar p=1 atm, estructura más estable, gases ideales

Energía libre de Gibbs
G=H-TS
El cambio en la pendiente de G correponde a ΔS de la transformacion
Zn (hcp) Continuas: estables Discontinuas : metaestables
0
0
2
2
<−=⎟⎠
⎞⎜⎝
⎛∂∂
−=⎟⎟⎠
⎞⎜⎜⎝
⎛
∂∂
<−=⎟⎠
⎞⎜⎝
⎛∂∂
TC
TS
TG
STG
p
pp
p
Curvatura negativa también

Dependencia de G de p
pendiente
Curvatura
Altas presiones: bajos volúmenes molares (alta densidad) Diamante más estable que grafito
∂G∂p
"
#$
%
&'T
=V
∂2G∂p2"
#$
%
&'T
=∂V∂p"
#$
%
&'T
= −Vβ

Diagrama pT de hierro
Fig. 15
Fases coexisten para Gα= Gβ
βα
βα
αβ
αβ
ββαα
βα
→
→
ΔΔ
=−−
=
+−=+−
=
SV
SSVV
dPdT
dPVdTSdPVdTSdGdG
Ecuación de Clausius-Clapeyron

Diagrama pT de CO2
fusión
sublimación
Pt debajo de presión atmosf -> la fusión se observa Excepciones CO2 Pt = 5.1 atm, Tt= -56.6 C à A presiones ordinarias Sublimación (hielo seco).