NUEVAS MOLÉCULAS TERAPÉUTICAS EN ENDOCRINOLOGÍA: …€¦ · S. insulina (dependiente de...
Transcript of NUEVAS MOLÉCULAS TERAPÉUTICAS EN ENDOCRINOLOGÍA: …€¦ · S. insulina (dependiente de...

NUEVAS MOLÉCULAS TERAPÉUTICAS EN
ENDOCRINOLOGÍA: DIABETES
Ana Cantón Blanco
H. Arquitecto Marcide
Endocrinología y Nutrición

Controlar la hiperglucemia
Mejorar el funcionamiento célula β
Actuar sobre otras comorbilidades: HTA,
dislipemia, obesidad,….
EL TRATAMIENTO “IDEAL” DE LA DIABETES DEBERÍA:

•FASE 1 •INTRODUCCIÓN EN HUMANOS•OBJETIVO: determinar metabolismo, farmacología y posiblesefectos secundarios•INDIVIDUOS: 20-80 VOLUNTARIOS SANOS
•FASE 2 ENSAYOS CONTROLADOSOBJETIVO: evaluar la eficacia en una indicación particular,establecer posibles efectos secundarios o riesgo a corto plazoINDIVIDUOS (en DM2): escasos cientosDURACIÓN (en DM2): MENOS DE 6 MESES
•FASE 3 ENSAYOS CONTROLADOS Y NO CONTROLADOSOBJETIVO: establecer riesgo-beneficio, tras aparente efectobeneficioso. Evaluar un fármaco en monoterapia o asociado aotros fármacos.INDIVIDUOS (en DM2): varios cientos (fase 2 + 3 unos 2500individuos)DURACIÓN (en DM2): 6 -12/18 MESES
Fases desarrollo de un fármaco en DM2
Code of Federal Regulations, April 2007

Rápido incremento de pacientes con DM
Disminución de la edad al diagnóstico
Tratamientos durante un período prolongado
Guidance for industry: diabetes mellitus. Developing drugs and therapeutic biologics for treatment and prevention. Food and Drug Administration. Center for Drug Evaluation and Research (CDER), Feb 2008
TRATAMIENTOS PARA LA DIABETES :Ensayos clínicos con un “mínimo” de
individuos durante un período “mínimo” de tiempo porque :
Se busca seguridad en el área cardiovascular ….

n: 6 voluntarios sanosGlucosa oralGlucosa endovenosa
* * *
Modificado de

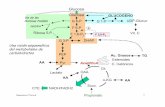
Páncreas:
síntesis de proinsulina
S. insulina (dependiente de glucosa)
S. glucagón (dependiente de glucosa)
+ proliferación célula beta
+ resistencia a la apoptosis
supervivencia de célula beta
Estómago
Vaciamiento gástrico
Secreción de ácido
SN
Apetito , ingesta
Saciedad
Captación glucosa
Síntesis de glucógeno
Secreción GLP-1
Ingesta
alimentos
+
Células L
Agonistas del GLP1

Agonistas del GLP1
• Utilización precoz, en fases tempranas de la diabetes
•Administración s.c.
•Bajo riesgo de hipoglucemia
• Efectos sobre la glucemia y otros factores de riesgo vascular:
•↓peso
• ↓TA
• Mejoría lípidos y marcadores de riesgo vascular
• Efectos adversos GI: náuseas, vómitos o diarrea
• No datos concluyentes que apoyen ↑pancreatitis aguda o
c. medular tiroides en humanos
•Contraindicados en FG <30 mL/min y enf GI grave

H G E G T F T S D L S K Q M E E E A V R L F I E W L K N G G P S S G A P P P S – NH2
H A E G T F T S D V S S Y L E G Q A A K E F I A W L V K G R – NH2
Exenatida
GLP-1Humano
G E G T F T S D K Q MK Q M E E E A V R L F I E W L K N G G P S S G A P P P S G P S S G A P P P S Exenatida
DPP-4
Molécula Dosis
Liraglutide 1,2-1,8 mg 1/d
Agonistas del receptor de GLP-1 (s.c.)
Segunda generación

7
36
9
Lys
His Ala Thr Thr SerPheGlu Gly AspVal
Ser
SerTyrLeuGluGlyAlaAla GlnLys
Phe
Glu
Ile Ala Trp Leu GlyVal Gly Arg
GLP-1 humano nativo
DPP-4 Ácido graso C-16 (palmitoyl)
His Ala Thr Thr SerPheGlu Gly AspVal
Ser
SerTyrLeuGluGlyAlaAla GlnLys
Phe
Glu
Ile Ala Trp Leu GlyVal Gly Arg
Glu
Arg
7 9
36
Liraglutida
Knudsen et al. J Med Chem 2000;43:1664–9; Degn et al. Diabetes 2004;53:1187–94
• Homología GLP-1: 97%
• Absorción lenta desde tej. subc.
• Menor susceptibilidad a DPP-4
• Larga vida media (T½=13 h)
• Administración una vez al día
• Independientemente horario ingesta

(n=110) (n=114) (n=97)
Garber A et al. Liraglutide, a human GLP-1 analogue maintains greater reductions in HA1c, FPG and weight than glimepiride over 2 years in patients vith type 2 diabetes:LEAD3 extension study.2009
P<0,0001
PESO

p=0,003
(n=896) (n=1363) (n=524)
p=0,0008
Fonseca V et al. A meta-analysis of six clinical trials demostrates that the once-daily human GLP-1 analogue liraglutide reduces systolic blood pressure.2009
PRESIÓN ARTERIAL SISTÓLICA

Molécula Dosis Ensayos
AVE0010 5-30 mcg 1-2/d Fase III
Exenatide LAR 2 mg 1 vez/semana
Taspoglutide 20-30 mg 1 vez/semana Fase III
Albiglutide 30-50 mg 1 vez/semana Fase III
CJC-1134-PC 1,5-3 mg 1-2/semana Fase II
NN9535 0,1-1,6 mg 1 vez/semana Fase II
LY2189265 0,25-3 mg 1 vez/semana Fase II
LY2428757 0,5-17,6 mg 1 vez/semana Fase II
Tercera generación
Agonistas del GLP1

HbA1c basal, cambio en HbA1c y diferencia vs tratamiento con exenatide
* **
Modificado de

* P=0,0003
Peso
HbA1c

Inhibidores de la DPP4
• ↓ actividad DPP4 en un 80% (↑GLP-1 y ↑GIP)
• Utilización precoz, en fases tempranas de la diabetes
•Administración oral (con o sin alimentos)
• Efecto fundamental sobre glucemia postprandial
• Bajo riesgo de hipoglucemia
• Efecto neutro peso y TA
• Buena tolerancia. No efectos adversos GI importantes
•No datos concluyentes que apoyen ↑pancreatitis aguda
•Contraindicados en general en insufiencia renal moderada-
grave y en insuficiencia hepática moderada-grave

Molécula Dosis Ensayos
Alogliptina 12,5-25 mg 1/d Fase III
Linagliptina 2,5-5 mg 1/d Fase III
Dutogliptina 200-400 mg 1/sem Fase III
........
Nuevos inhibidores de la DPP4
Moléculas comercializadas
Dosis
Sitagliptina 100 mg/d o 50 mg/12 h asoc
Vildagliptina 50 mg/12 h
Saxagliptina 5 mg/d
Inhibidores de la DPP4

El 99% de la glucosa plasmática filtrada en el riñón es reabsorbidaen el túbulo renal proximal. El 90% (SGLT2) principio túbuloproximal
Kidney International (2009);1272-1277
Inhibidores SLGT2 (sodium-D-glucose cotransporter-2)
Modificado de

Inhibidores SLGT2 (sodium-D-glucose cotransporter-2)en desarrollo clínico
Molécula Ensayo
Dapagliflozina Fase 3 (pub)
Canagliflozina Fase 3
•Múltiples moléculas :YM543, ASP-1941, R-7201,GSK189075, B110773, B144847,ISIS388626, DSP-3235, SAR7226,…
Fase 1Fase 2

* * *
* * *
Modificado de

Modificado de

• Stulnig TM, Waldhäusl W. Diabetologia. 2004; 47(1):1-11.
Inhibidores de la 11β-HSD1

• n: 302 pac
• 12 sem tto
-0,47%,p<0,05 -0,56%,p<0,01
p<0,1
* *
Modificado de

**
***
*
*
Modificado de

* * *
*
*
*
Modificado de

AGONISTAS DE LOS PPAR (peroxisome proliferator-activated receptors)
Modificado de

AGONISTAS DE LOS PPAR
Modificado de

PPAR α: (+ por fibratos, FFA)
• Metabolismo lipídico ( ↑ HDL,↓TGS)
• Síntesis de lipoproteínas
• Respuesta inflamatoria
PPAR γ :
• Aumento sensibilidad a In
• Respuesta inflamatoria
PPAR β/δ :
•Agonistas panPPARs
•Agonistas duales PPAR α - PPAR γ
•Agonistas PPAR γ selectivos:
•< adipogénesis,
•< ↑peso, < expansión volumen, < retención fluídos (< edema)
Skin,….

Agonistas duales PPAR α - PPAR γ (glitazares)
•Diferentes tipos de toxicidad : no > fase III
• Ragaglitazar/farglitazar: toxicidad hepática en animales
•Tesaglitazar : alteración función renal
• Muraglitazar:aumento eventos cardiovasculares

• n: 332 pac
• 16 sem tto
*

TGS* colHDL*
colLDL*
•↓m. inflamatorias •↓TA

=

PRAMLINTIDE
Análogos de
la amilina
Modificado de

cierre
Secretagogos de insulina
Modificado de

Activadores glucokinasa
- Problema principal: glucokinasa en múltiples tejidos
- Múltiples moléculas (2007-2009),ej:
•In vitro/in vivo•Administración oral
•Derivados de la dicicloalkilurea In vitro
•Compuestos del benzoil aminoheterociclil
In vitro
•Derivados tiazólicos •In vivo (animal)•Reducción glucemia 22%
•Compuestos heterocíclicos •In vivo (animal)•Reducción glucemia 21,6%•Incremento actividad 178%
•Derivados del ácido propiónico •In vivo (animal)•Reducción glucemia 35%
Secretagogos de insulina: activadores de la glucokinasa

•Glinidas / sulfonilureas•Riesgo de hipoglucemia •El desarrollo de nuevos fármacos a través de este mecanismo es escaso
Secretagogos de insulina: Moduladores canales de K

• In administración tópica (parche)
• Insulina inhalada
• Insulina oral •Evitar degradación enzimáticaen el tracto GI•Escasa permeabilidad de lainsulina a través del sistemagastrointestinal• Fase II
• Insulina s.c de mayor duración •Insulinas de acción ultralarga (1 /d, 3/semana) Ej. degludec
•Asociaciones de Insulina -análogos GLP-1•asociaciones de análogos de In
Insulina

Monocitos, cél. natural killer, cél. B autoreactivas,…
cél. beta
DIABETES TIPO 1
Modificado de

INMUNOTERAPIA EN DIABETES TIPO I(AG ESPECÍFICA Y NO ESPECÍFICA)
OBJETIVO: MEJORÍA FUNCIÓN RESIDUAL CÉLULA BETA
Modificado de

•Acs monoclonales anti-CD3: teplizimab, otelixizumab
• pép C durante 2 a
• preservación de las c. Treg
•Acs monoclonales anti-CD20: rituximab
•Intervención antígeno específica: GAD65
• Pendiente inicio ensayos clínicos en DM1:
• Aralast NP (α 1 antitripsina)
• Imatinib (Gleevec) – tirosinkinasa
INMUNOTERAPIA EN DIABETES TIPO 1
• ¿Tratamiento combinado?

• Ac monoclonal anti-CD20
• Estudio Fase 2 (depleción de linfocitos B)
• n: 81 (8-40 a) con DM1 diagnosticada 81-91 d
antes de la primera infusión (rituximab/placebo)
• infusión rituximab/placebo i.v. días 1, 8, 15, 22
• evaluación al cabo de un año
• No incremento de neutropenia ni de infecciones

*P=0,03
* P<0,001
* P<0,001

• Autoantígeno GAD
• n: 70 [pépt C> 0,1 nm/L y antiGAD+ ]con DM1
diagnosticada en los 18 m previos
• Dosis s.c 1 y 30 d
• Evaluación a los 30 m

Preservación función célula beta si reciente diagnóstico

• Existen diferentes líneas de trabajo
• Líneas más prometedoras:
• análogos del GLP-1: acción fisiológica, efecto
sobre riesgo cardiovascular (peso)
• -SLGT2: potencial utilidad en cualquier fase de la
enfermedad, en monoterapia o asociación, efecto
sobre riesgo cardiovascular (peso)
• Análogos de la insulina: asociaciones entre
análogos, asociación con análogos del GLP-1,…
Conclusiones
![Metabolismo de los lipidos [Modo de compatibilidad] · PDF fileLos restos de acetil-CoA provenientes de la β-oxidación y de la degradación de glucosa o de las cadenas carbonadas](https://static.fdocument.org/doc/165x107/5a943a8b7f8b9aba4a8bd427/metabolismo-de-los-lipidos-modo-de-compatibilidad-restos-de-acetil-coa-provenientes.jpg)










![Propiedades y características - [DePa] Departamento de …depa.fquim.unam.mx/amyd/archivero/Radiacion... · 2014-04-21 · dependiente de la fuente de radiación. Velocidad de propagación,](https://static.fdocument.org/doc/165x107/5bab31e709d3f2e74b8b9c8d/propiedades-y-caracteristicas-depa-departamento-de-depafquimunammxamydarchiveroradiacion.jpg)



