Mecanismos de sinalização endotelial envolvidos na atividade ...
Transcript of Mecanismos de sinalização endotelial envolvidos na atividade ...

2
UNIVERSIDADE FEDERAL DA PARAÍBA
CENTRO DE CIÊNCIAS DA SAÚDE
PROGRAMA DE PÓS-GRADUAÇÃO EM PRODUTOS NATURAIS E
SINTÉTICOS BIOATIVOS
THAÍS PORTO RIBEIRO
Mecanismos de sinalização endotelial envolvidos na
atividade cardiovascular do α-terpineol
JOÃO PESSOA – PB
2012

3
THAÍS PORTO RIBEIRO
Mecanismos de sinalização endotelial envolvidos na atividade cardiovascular do α-terpineol
Tese apresentada ao Programa de Pós-Graduação em Produtos Naturais e Sintéticos Bioativos/UFPB como requisito parcial para obtenção do título de Doutor em Produtos Naturais e Sintéticos Bioativos - Farmacologia.
Orientador:
Prof. Dr. Isac Almeida de Medeiros
Coorientador:
Prof. Dr. Valdir de Andrade Braga
JOÃO PESSOA – PB
2012

4
THAÍS PORTO RIBEIRO
Mecanismos de sinalização endotelial envolvidos na atividade cardiovascular do α-terpineol
Aprovado em 27 de Fevereiro de 2012.
COMISSÃO EXAMINADORA
__________________________________________________ Prof. Dr. Isac Almeida de Medeiros
Orientador
__________________________________________________ Prof. Dr. Demétrius Antônio Machado de Araújo
Examinador Interno
__________________________________________________ Prof. Dr. Celso José Bruno de Oliveira
Examinador Externo
__________________________________________________ Profa. Dra. Patricia Emilia Naves Givisiez
Examinador Externo
__________________________________________________ Prof. Dr. José Eduardo Krieger
Examinador Externo
JOÃO PESSOA – PB
2012

5
R484m Ribeiro, Thaís Porto. Mecanismos de sinalização endotelial envolvidos na atividade
cardiovascular do -terpineol / Thaís Porto Ribeiro. - - João Pessoa:
[s.n.], 2012.
210f. : il.
Orientador: Isac Almeida de Medeiros.
Co-orientador: Valdir de Andrade Braga.
Tese (Doutorado) – UFPB/CCS.
1. Produtos naturais. 2. Óxido nítrico. 3. Artéria mesentérica
superior. 4. Canais para potássio. 5. Hipotensão.
UFPB/BC CDU: 547.9(043)

6
A minha família, minha base, minha felicidade...
A todos aqueles que necessitam do contínuo estudo
de desenvolvimento de fármacos para amenizar seus sofrimentos frente às
doenças.

7
Agradecimentos
Ao finalizar esta tese de doutorado gostaria de registrar meus sinceros agradecimentos
às individualidades de cada pessoa que contribuiu com este trabalho e foi capaz de amenizar o
processo solitário ao qual qualquer investigador está destinado a seguir.
Inicialmente, ao meu orientador Prof. Isac, eu agradeço por me formar uma pesquisadora e
por me ensinar nestes 10 anos como ser profissional. Ainda, por compartilhar comigo o seu
tema de pesquisa, sendo um exemplo de pesquisador e ser humano, mostrando que
devemos levar não só na pesquisa, mas para toda a vida os valores éticos de honestidade e
humildade. Obrigada pela amizade, desde a iniciação científica, pela confiança depositada na
construção desse trabalho, sou grata pelo incentivo e oportunidade de poder realizar e
conquistar esse grande sonho.
Ao meu coorientador Prof. Valdir toda minha gratidão por encarar o desafio de trabalhar
em um projeto em andamento. Por ser um pesquisador dinâmico e disposto a oferecer
estímulos e, principalmente, a percorrer novos caminhos, ouvir com atenção as questões,
dúvidas e problemas que surgiam durante o processo. Obrigada pelos ensinamentos e
contribuição durante a execução desse trabalho e acima de tudo por sua amizade.
Je remercie chaleureusement la Madame Pr. Valérie B. Schini-Kert, la diretrice du
Laboratoire de Pharmacologie et Physiopalotologie Cardiovasculares pour m’avoir accueille au
sein de sa unité, pour son acessabilité et sa disponibilité. Je la remercie de m’avoir accordé sa
confiance, ses competénces scientifique et ses précieux conseils durant mon séjour au
laboratoire.
Aos membros da banca examinadora, os professores José Eduardo Krieger, Celso de
Oliveira, Patrícia Naves, Demétrius Araujo (membro da qualificação) e aos membros da
banca de qualificação os professores Amilton Cruz e Sandra Mascarenhas, expresso meus
agradecimentos pelo interesse em compartilhar seus conhecimentos para aprimorar este
trabalho. Agradeço a ajuda e as contribuições concedidas e por me dar a honra de aceitar
julgar este trabalho.
Faço um agradecimento especial ao aluno de mestrado Leônidas, e aos alunos de doutorado
- Aurylene, Bruna, George, Maria do Socorro (Corrinha) e Melissa- eu não tenho palavras
para expressar minha gratidão, agradeço a sincera amizade e por ter depositado em mim a
confiança de aprender junto. Obrigada pelo auxílio na execução deste trabalho, tenho
orgulho de ter compartilhado todos os árduos momentos com vocês, lembrando que este
trabalho é nosso.

8
Aos amigos do laboratório de Farmacologia Cardiovascular: Abraão, Ana Letícia, Angélica,
Fabíola, Islânia, Jaci, Juliane, Kivia, Lays, Maria do Carmo (Carminha), Marney, Mônica,
Natália, Priscila, Priscila, Valéria, Robson, Tays, Thaís Josy, Thyago, Walma, agradeço o
coleguismo e companheirismo em compartilhar com discussões sobre os diversos temas
relacionados e pela eficiência exercida sempre.
A TODOS os alunos do Laboratório de Neurobiologia, do Departamento de Patologia da
Universidade Federal do Paraná - Curitiba/PR. Em especial a professora Lia Nakao e as alunas
Alessandra Antunes e Karime França pelo acolhimento, interesse compartilhar seus
conhecimentos que ajudaram ao desenvolvimento deste trabalho e o compromisso com a
execução de experimentos. Agradeço toda a ajuda e as contribuições concedidas.
J’exprime toute ma reconnaissance et remercie viventent à ensemble des membres du
Laboratoire de Pharmacologie et Physiopalotologie Cardiovascular, du Laboratoire de
Biophotonique et Pharmacologie, de la Faculté de Pharmacie de l’Université de Strasbourg qui
ont tous participé à realisation de ce travail.
Mes remerciements très particuliers vont à Chuc, Evelyne, Israa, Lazare et Quentin pour son
amitié chaleureuse, son disponibilité et pour son aide à mon travail. Je remercie également
les colègues Cyril, Faraj, Grégory, Guy, Mahmoud, Mohammad, Nelly, Nourddinne,
Philipe et Thierry pour leur sympathie, leur soutien et leur bonne humeur quotidienne. Et je
remercie à le Messieur Cristhian Müller pour sa disponibilité.
Agradeço as primeiras pessoas que me ajudaram na iniciação científica; os professores
Horacinna, Katy Lísias, Márcio Roberto e Renildo que me ensinaram a dar os primeiros
passos no caminho da pesquisa e a amar tudo isso.
Aos professores Damião Piergentino e Diego Nunes, e as alunas de iniciação científica
Dayane Porto e Camilla Pinheiro eu agradeço as contribuições concedidas, principalmente
na fase inicial deste trabalho.
Impossível não ressaltar a importância que teve a convivência fraterna e a cumplicidade que
encontrei meus amigos de pós-graduação. Ter tido a oportunidade de conviver e dividir
ansiedades, alegrias e amizade sem a qual não saberia ter sido diferente, em especial a
Ionaldo, José Alves, Juan, Kiriaki, Micheline e Nilson por mostrar que os amigos são a
família que escolhemos.
Deixo também meus agradecimentos à Coordenação, em especial a professora Fátima
Agra, e a todos os professores do programa de pós-graduação, pela ajuda na construção
do conhecimento e enriquecimento durante esses anos de pós-graduação, pela dedicação e
pelo emprenho com que conduzem este programa.

9
Indispensável também citar a importante função que exerceram os dirigentes e funcionários
do CBiotec na minha formação. Em especial a Mônica Rodrigues por passar a alegria todos
os dias com um sorriso e incentivo, às secretárias da pós-graduação Tânia e Carol e os
funcionários do Biotério George Thomas, os ilustres: Crispim, Sr. Luiz e Adriano.
Agradeço ao CBIOTEC, CCS e à Universidade Federal da Paraíba e à Faculté de Pharmacie
e à Université de Strasbourg por possibilitar e pelo suporte técnico a essa pesquisa. Ao
CNPq e a Capes pelo apoio financeiro de custeio de todo doutorado, além da contribuição
com a disponibilidade do portal de periódicos CAPES.
Agradeço ainda aos alunos de graduação (que me foram emprestados no estágio docência)
que me motivavam a buscar sempre mais conhecimento, depositando em mim suas
expectativas e seus questionamentos e me dando a certeza de que este é caminho certo a
seguir.
As palavras são pequenas ao expressar o tamanho da gratidão para a minha família que está
sempre presente em períodos de escolhas e decisões, pela compreensão e força em todos os
momentos da minha vida. Em especial a minha linda mãe Maria Luísa, por ser fonte de
inspiração e aos meus queridos irmãos Arthur e Rafael, os quais amo tanto! Obrigada não é
o bastante para minhas queridas avós Maria José e Severina pelo apoio concedido durante
toda minha existência, creditando toda a paciência, carinho e amor.
Aos meus eternos amigos: Andréia, Juliana, Naiana, Roxana, Suênia, Wagner. Eu não
poderia deixar de agradecer a todo o carinho e amizade dedicada durante os anos que se
fizeram antes deste momento. Desde o período de graduação e que me acompanham até
hoje. E apesar da distância e das atividades do dia-a-dia estão sempre na torcida para que
sempre dê tudo certo.
Aos amigos especiais Adriana, Benito, Fabíola, Isabella, Luciana, Renata, Vanessa e
Thiago Ianatoni que estão comigo em diversos momentos, sempre me trazendo para o
mundo real e mostrando que existem outras experiências, além da pesquisa.
A todos os meus grandes amigos que colaboraram de maneira direta ou indiretamente com
esse trabalho e que em vários momentos serviram de norte nesta caminhada. E aqueles que
de uma simples conversa, aprendemos sem mistérios, a conhecermos as pessoas com suas
limitações e vocações. A todos, minha eterna gratidão.
Thaís Porto Ribeiro Fevereiro 2012

10
Só sabemos com exatidão quando sabemos pouco;
Com o saber, cresce a dúvida.
.
Johann Wolfgang von Goethe (1749-1832)

11
Os óleos essenciais são componentes voláteis orgânicos encontrados em plantas aromáticas, que apresentam vários monoterpenos, como o α-terpineol. Estudos têm demonstrado algumas atividades biológicas, tais como hipotensivas e vasorelaxantes (Guedes et al., 2004). No presente trabalho, estudaram-se os efeitos cardiovasculares do α-terpineol e caracterizou-se a farmacodinâmica destes efeitos. Para isso foram utilizados ratos normotensos Wistar (WKY) e espontaneamente hipertensos (SHR), empregando técnicas combinadas in vivo, in vitro, e cultivo de células endoteliais. Para determinar a medida direta da pressão arterial, foram implantados cateteres na artéria aorta e veia cava inferior para administração de drogas em ratos WKY e SHR. Adicionalmente, foram realizados estudos para avaliar a reatividade vascular, assim, animais foram sacrificados e a artéria mesentérica superior foi isolada. Os anéis foram mantidos em cubas com solução de Tyrode, e gaseificada com carbogênio. Os anéis foram fixados a um transdutor de força, o qual estava acoplado a um sistema de aquisição de dados (Miobath-4, WPI, Sarasota, EUA) a uma tensão de 0,75 g por 1h. Após este período as preparações, foram pré-contraídas com 10 µM de fenilefrina (FEN) e, em seguida, concentrações crescentes
de -terpineol (10-12-10-5 M) foram adicionadas cumulativamente. Adicionalmente, realizamos experimentos para quantificação da produção de NO e determinação da atividade da eNOS, AKT e AMPK em cultivo de células endoteliais, utilizando as
técnicas de citometria de fluxo e western blotting. Assim, observamos que -terpineol (1, 5, 10 e 20 mg/kg i.v., randomicamente) produziu uma hipotensão dose-
dependente em ratos WKY (-103, -399, -5211, -6212 mmHg, n=10) e SHR (-
375, -577, -715, -844 mmHg, n=9, respectivamente), associada a taquicardia. A resposta hipotensora foi atenuada significantemente, após o tratamento com L-NAME (20 mg/kg, i.v), sugerindo que esse efeito pode ser decorrente de uma diminuição da resistência periférica., α-terpineol demonstrou melhorar a sensibilidade do barorreflexo. A resposta vasorelaxante foi significativamente
atenuada quando comparada aos anéis na presença (WKY Emax= 60 4 e SHR Emax= 53,7 ± 3, p<0,05, n=9) e na ausência do endotélio funcional [WKY Emáx= 20,5
1 e SHR Emáx=16,1 ± 3, p<0,05, n=8]. Em anéis pré-contraídos com FEN na presença de L-NAME (100 μM), Hidroxicobalamina (30 μM) e ODQ (10 μM), a resposta relaxante foi atenuada significantemente, sugerindo uma participação da
via NO-GMPc. Adicionalmente, -terpineol aumentou os níveis de produção de NO e a atividade da eNOS por fosforilar vias como a PI3K e AMPK. No entanto, na
presença de atropina (1 M) ou indometacina (10 M), a resposta vasorelaxante de
-terpineol não foi alterada indicando que os receptores muscarínicos e metabólitos da enzima Ciclooxigenase parecem não estar envolvidos. KCl (20mM) foi capaz de
atenuar o efeito de -terpineol, e preparações com endotélio vascular incubados
com glibenclamida (10 M) e 4-aminopiridina (1 mM), tetraetilamônio (1 mM) e caribdotoxina + apamina (0,2 μM). Deste modo, concluímos que resposta
vasorelaxante promovida pelo -terpineol é dependente de endotélio e envolve a via L-Arginina-NO-GMPc por aumentar a fosforilação da eNOS por vias PI3K e AMPK, produção de NO e EDHF com participaçãode canais para potássio do tipo KCa, KV e KATP em SHR e WKY e estes efeitos são responsáveis por eventos in vivo. Palavras chaves: artéria mesentérica superior, canais para potássio, hipotensão,
óxido nítrico, -terpineol.
RIBEIRO, T. P. Mecanismos de sinalização endoteliais envolvidos na atividade cardiovascular do α-terpineol em ratos hipertensos. 2012. Tese (Pós-graduação em Produtos Naturais e Sintéticos Bioativos, Farmacologia) Centro de Ciências da Saúde, Universidade Federal da Paraíba, João Pessoa, Brasil.

12
The essential oils are volatile organic constituents found in aromatic plants, which
present several monoterpenes, such -terpineol. Studies have demonstrated some biologic activities such as hypotensive and vasorelaxant (Guedes et al., 2004). In the
present work the cardiovascular effects of -terpineol was investigated and the pharmacodynamics of this effect was characterized. Wistar Kyoto and spontaneously hypertensive rats (SHR) were anaesthetized and polyethylene catheters were inserted into the low abdominal aorta and inferior vena cava for blood pressure measurements and administration of drugs. Isolated superior mesenteric rings (1-2 mm) were suspended by cotton threads for isometric tension recordings in Tyrode’s solution (37°C, gassed with 95% O2 and 5% CO2), under 0.75g resting tension were measured by using pressure transducers, coupled to a computer set and CVMS software Miobath-4, WPI, Sarasota, EUA. In addition, the bioavailability of NO and eNOS, AKT and AMPK activity were quantified when exposing cells to α-terpineol in the cultured endothelial cells. In both SHR and normotensive rats, i.v. bolus injections of α-terpineol (1–20 mg/kg) decreased mean arterial pressure (MAP) in a dose-
related manner, WKY (-103, -399, -5211, -6212 mmHg, n=10) and SHR (-375,
-577, -715, -844 mmHg, n=9) associated with tachycardia. However, hypotensive and tachycardic responses were significantly attenuated after L-NAME (20 mg/kg,
i.v.). The -terpineol demonstrated improves the baroreflex sensitivity. In intact
isolated rat mesenteric rings -terpineol (10-12–10-5M) induced concentration-
dependent relaxation of the contractions induced by phylephrine (10M) WKY Emax=
60 4 or SHR Emax= 53.7 ± 3, p<0.05, n=9). After endothelium removal the
vasorelaxant elicited by -terpineol was significantly attenuated WKY [Emax= 20.5 1*] and SHR [Emax= 16.1 ± 3*, p<0.05, n=8]. Similar results were obtained in the
presence of L-NAME 100M, a competitive antagonist of NOS, hydroxocobalamin 30 μM, a NO scavenger or ODQ 10μM, a selective inhibitor of soluble guanylyl cyclase.
In addition, in endothelial cells, -terpineol increased eNOS activation and NO levels by phosphorylation of PI3K/ AKT and AMPK pathway. However, atropine (1ηM) or
indometacin (10 μM) had no effect on the -terpineol -induced vasorelaxation. Furthermore, vasorelaxation was significantly attenuated in the presence of 20 mM KCl a modulator K+ efflux or several blocking of potassium channels: 1mM 4-
aminopirimidine, 10 M glibenclamide, 1 mM tetraethylammonium and carybdotoxin
plus apamin (0.2M). In conclusion, the present study demonstrated that -terpineol induced hypotensive effect, probably due to a decrease of peripheral vascular resistances, which seems to be mediated by endothelium derived relaxant factors, at least NO induced. These results suggest that vasorelaxant response, almost completely mediated by the endothelium, likely via NO release and activation eNOS by PI3K and AMPK with consequently activation of NO-cGMP pathway and potassium channels activation at least, KCa, KV, and KATP are involved in the
vasorelaxant effect induced by -terpineol.
Key- Words:, hypotension, K+ channels, Nitric Oxide, superior mesenteric artery, -terpineol.
RIBEIRO, T. P. Endothelial signaling mechanisms involved in
cardiovascular effect to α-terpineol in hypertensive rats.
2012. Thesis (Graduate program in Natural Products and
Synthetic Bioactives, Pharmacology) Health Sciences Center,
Federal University of Paraíba, Joao Pessoa, Brazil.

13
LISTA DE FIGURAS
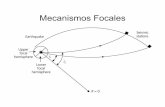
Figura 1: Fatores relaxantes derivados do endotélio.............................................. 27
Figura 2: Esquema da biosíntese do óxido nítrico.................................................. 28
Figura 3: Representação do cavéolo, da caveolina-1 e interação com a eNOS...... 29
Figura 4: Representação de proteínas cinases envolvidas na fosforilação da
eNOS......................................................................................................................... 31
Figura 5: Estrutura química do α-terpineol............................................................... 35
Figura 6: Representação esquemática dos vasos onde foram implantados os
cateteres para o registro dos parâmetros cardiovasculares e administração de
drogas. .................................................................................................................... 43
Figura 7: Aparato utilizado para as medidas de pressão arterial e frequência cardíaca em ratos.....................................................................................................
43
Figura 8: Representação esquemática do protocolo experimental. Protocolo da
administração de doses crescentes de -terpineol em ratos WKY e SHR antes e após tratamento agudo com diferentes inibidores...................................................
44
Figura 9: Fotografia do sistema de cubas de aquisição de dados de tensão
isométrica para órgãos isolados................................................................................ 47
Figura 10: Representação esquemática do protocolo experimental para estudo
do efeito de concentrações crescentes -terpineol (10-12 a 10-5 M) ......................... 48
Figura 11: Efeitos do α-terpineol sobre (a) a pressão arterial média (PAM, mmHg)
e (b) frequência cardíaca cardíaca (FC, bpm) em ratos normotensos (WKY) (n=10) e hipertensos (SHR) não-anestesiados ............................................
59
Figura 12: Registro representativo dos efeitos do α-terpineol (4.8 mg/kg) sobre a
pressão arterial média (PAM, mmHg) e frequência cardíaca (FC, bpm) em ratos
(A) normotensos (WKY) (n=10) e (B) hipertensos (SHR) (n=9)............................... 60

14
Figura 13: Efeitos do α-terpineol sobre (a) a pressão arterial média (% de PAM,
mmHg) e (b) frequência cardíaca (% de FC, bpm) em ratos normotensos (WKY)
(n=10) e hipertensos (SHR) não-anestesiados......................................................... 62
Figura 14: Efeitos do α-terpineol sobre (a) a pressão arterial sistólica em ratos
normotensos (WKY) (n=10) e hipertensos (SHR) não-anestesiados..................... 63
Figura 15: Efeitos do α-terpineol sobre (a) a pressão arterial média (PAM, mmHg)
e (b) frequência cardíaca (FC, bpm) em ratos normotensos (WKY) e hipertensos
(SHR) não-anestesiados (n=6) antes e após o tratamento com
atropina...................................................................................................................... 65
Figura 16: Efeitos do α-terpineol sobre (a) a pressão arterial média (PAM, mmHg)
e (b) frequência cardíaca (FC, bpm) em ratos normotensos (WKY) e hipertensos
(SHR) não-anestesiados (n=6) antes e após o tratamento com
hexametônio.............................................................................................................. 67
Figura 17: Efeitos do α-terpineol sobre (a) a pressão arterial média (PAM, mmHg)
e (b) frequência cardíaca (FC, bpm) em ratos normotensos (WKY) e hipertensos
(SHR) não-anestesiados (n=6) antes e após o tratamento com
atenolol...................................................................................................................... 68
Figura 18: Efeitos do α-terpineol sobre (a) a pressão arterial média (PAM, mmHg)
e (b) frequência cardíaca (FC, bpm) em ratos normotensos (WKY) e hipertensos
(SHR) não-anestesiados (n=5) antes e após o tratamento com
prazosin..................................................................................................................... 70
Figura 19: do α-terpineol sobre (a) a pressão arterial média (PAM, mmHg) e (b)
frequência cardíaca (FC, bpm) em ratos normotensos (WKY) e hipertensos (SHR)
não-anestesiados (n=7). antes e após o tratamento com L-NAME.......................... 72
Figura 20: Efeitos do α-terpineol sobre a sensibilidade do barorreflexo em ratos
normotensos (WKY) e hipertensos (SHR) não-anestesiados................................... 74
Figura 21: -Terpineol induz relaxamento em anéis de artéria mesentérica de
ratos hipertensos SHR e controles WKY................................................................... 75
Figura 22: Registro original da ação do α-terpineol (10-12 - 10-5 M) em anéis de
artéria mesentérica superior isolada de rato............................................................. 76

15
Figura 23: Efeito do α-terpineol sobre o tônus basal de anéis de artéria
mesentérica superior isolada de rato........................................................................ 77
Figura 24: α-Terpineol induz relaxamento vascular dependente do endotélio
envolve a participação da enzima eNOS.................................................................. 79
Figura 25: α-Terpineol promove efeito vasorelaxante via óxido nítrico/GMPc......... 80
Figura 26: Metabólitos da ciclooxigenase ou receptores muscarínicos não estão
envolvidos na resposta vasorelaxante induzida pelo de -terpineol......................... 82
Figura 27: Caracterização da participação do EDHF no efeito vasorrelaxante
induzido pelo α-terpineol (10-12 – 10-5M)................................................................... 83
Figura 28: Efeito inibitório dos bloqueadores de canais de potássio no
relaxamento vascular induzido pelo α-terpineol em SHR e WKY............................. 85
Figura 29: Identificação dos canais de potássio que participam do relaxamento
vascular induzido pelo α-terpineol em SHR e WKY.................................................. 87
Figura 30: Acetilcolina e bradicinina induzem aumento nos níveis de NO em
cultura de células endoteliais de aorta de coelho..................................................... 89
Figura 31: α-Terpineol aumenta os níveis de NO em células endoteliais................ 91
Figura 32: α-Terpineol aumenta os níveis de NO em células endoteliais. Gráfico
dos dados que expressam a produção de NO induzida por acetilcolina ou α-
terpineol em cultura de células endoteliais de aorta de coelho................................. 92
Figura 33: A enzima eNOS está envolvida na produção de NO induzida pelo -
Terpineol.................................................................................................................... 93
Figura 34: A enzima eNOS está envolvida na produção de NO induzida pelo -
Terpineol. Gráficos da produção de NO em cultura de células endoteliais de aorta
de coelho tratados por α-terpineol ou L-NAME + α-terpineol em diferentes
concentrações............................................................................................................ 94
Figure 35: Análises representativas do efeito da insulina em cultura primária de
células endoteliais de coronária de porco................................................................. 95
Figura 36: α-terpineol induz fosforilação da eNOS................................................... 96

16
Figura 37: α-terpineol induz rápida fosforilação da Akt em Ser473 e da eNOS em
Ser1177 em cultura de células endoteliais de coronária de porco ........................... 97
Figura 38: α-terpineol induz fosforilação da Akt em Ser473 e da eNOS em
Ser1177 dependente da concentração em cultura de células endoteliais de
coronária de porco..................................................................................................... 98
Figura 39: α-terpineol induz fosforilação da AMPK em Tyr 172 em cultura de
células endoteliais de coronária de porco................................................................. 99
Figura 40: Imagens com fluorescência de DAF-2 obtidas nas imagens das
culturas de células endoteliais tratadas com α-terpineol (10-4 M ) ou L-NA (100μM)
+ α-terpineol 10-4 M).................................................................................................. 101
Figura 41: Representação da farmacodinâmica do α-terpineol................................ 116

17
LISTA DE TABELAS
Tabela 1 Porcentagem de inibição da resposta máxima e contração com FEN
(10 μM) para estudos da via NO/GMPc em anéis de artéria mesentérica superior
isolada de rato.......................................................................................................... 51
Tabela 2 Porcentagem de inibição da resposta máxima e contração com FEN
(10 μM) para estudos de metabolitos da ciclooxigenase e receptores
muscarínicos em anéis de artéria mesentérica superior isolada de rato................. 55
Tabela 3 Porcentagem de inibição da resposta máxima e contração com FEN
(10 μM) para estudos de canais de potássio em anéis de artéria mesentérica
superior isolada de rato............................................................................................ 60

18
LISTAS DE ABREVIATURAS E SIGLAS
4 – AP 4 – Aminopiridina
AA Ácido araquidônico
ACh Acetilcolina
ADP Difosfato de adenosina
AKT/ PKB Proteína cinase serina treonina tipo B
ATP Trifosfato de adenosina
AMPc Monofosfato de adenosina cíclico
AMPK Proteína cinase dependente de 5’ monofosfato de adenosina
ANOVA Análise de variância
BH4 (6R-)5,6,7,8-tetrahidro-L-biopterina
BKca Canais de potássio de grande condutância sensíveis ao Ca+2
BK Bradicinina
b.p.m. Batimentos por minuto
[Ca2+4 – CaM] Complexo Cálcio – Calmodulina
CaM Calmodulina
CaMKII Proteína cinase II dependente da calmodulina
Cav-1 Proteína caveolina -1
CECP Células endoteliais de coronária de porco
COX Ciclooxigenase
DAG Diacilglicerol
DC Débito cardíaco
DMSO Dimetilsulfóxido

19
EDHF Fator hiperpolarizante derivado do endotélio
EDRF Fator relaxante derivado do endotélio
EGTA Ácido etilenoglicol-bis-(-aminoetiléter) N,N,N´,N´- tetraacético
eNOS Sintase do NO endotelial
FC Frequência cardíaca
FEN Fenilefrina
GC Ciclase de guanilil
GDP Difosfato de guanosina
Gi Proteína G inibitória
GMPc Monofosfato de guanosina cíclico
Gs Proteína G estimulatória
GTP Trifosfato de guanosina
GTPase Trifosfatase de guanosina
HDX Hidroxicobalamina
HETE Ácido hidroxiepoxieicosatrienóico
HSP90 Proteína de estresse 90 kDa
IKCa Canal de K+ de condutância intermediária ativado pelo Ca+2
INDO Indometacina
iNOS Sintase de óxido nítrico induzida
IP3 Trifosfato de inositol
KATP Canais de potássio sensíveis ao ATP
Kca Canais de potássio sensíveis ao Ca+2
KIR Canais de potássio retificadores de entrada
KV Canais de potássio sensíveis a voltagem

20
L-NAME NG-Nitro-L-arginina metil éster
L-NOHA N-hidróxi-L-arginina
MeOH Metanol
MLC Cadeia leve de miosina
MLCK Cinase da cadeia leve da miosina
NO Óxido Nítrico
NOS Sintase do NO
NPS Nitroprussiato de sódio
ODQ 1 H-[1,2,4] oxadiazólo [4,3-a] quinoxalin-1-ona
PAM Pressão arterial média
PBS Solução salina tamponada com fosfato
PGI2 Prostaciclina
PI3K fosfatidil-inositol 3-cinase
PIP2 4,5 – difosfato de inositol
PKA Proteína cinase A
PKC Proteína cinase C
PKG Proteína cinase G
PLC Fosfolipase C
RAEC Células endoteliais de aorta de coelho
RE Retículo endoplasmático
ROCC´s Canais de cálcio operados por receptores
ROS Espécies reativas de oxigênio
RS Retículo sarcoplasmático
RYR Receptor de rianodina

21
Ser Serina
SHR Rato espontaneamente hipertenso
SKCa Canal de K+ de condutância baixa ativado pelo Ca+2
Src Proteína tirosina cinase Src
TEA Tetraetilamônio
Thr Treonina
Tyr
Tirosina
TXA2 Tromboxano A2
VEGF Fator de crescimento do endotélio vascular
Vm Potencial de membrana
VOCC’s Canais de cálcio operados por voltagem
WKY Rato Wistar-Kyoto normotenso
.

22
SUMÁRIO
1 – INTRODUÇÃO................................................................................................ 24
1.1 Sistema cardiovascular: O endotélio e mediadores endoteliais..................... 24
1.2 Óxido Nítrico: biosíntese e função vascular................................................... 28
1.3 Mecanismos de ativação da enzima eNOS:.................................................. 29
1.4 Disfunção endotelial associada à hipertensão: Alvos para tratamento.......... 32
1.5 Produtos Naturais: Monoterpenos e α-terpineol............................................ 34
2 – OBJETIVOS .................................................................................................. 37
2.1 Gerais............................................................................................................. 37
2.2 Específicos..................................................................................................... 37
3 – MATERIAIS................................................................................................... 39
3.1. Animais.......................................................................................................... 39
3.2 Obtenção do -terpineol................................................................................. 39
3.3 Substâncias e sais......................................................................................... 39
3.4 Soluções nutritivas......................................................................................... 40
3.5 Preparação da solução de -terpineol........................................................... 40
4 – MÉTODOS...................................................................................................... 42
4.1 Ensaios Farmacológicos in vivo. ................................................................... 42
4.2 Ensaios Farmacológicos in vitro..................................................................... 46
4.3 Ensaios bioquímicos realizados in vitro......................................................... 51
4.4 Análise Estatística........................................................................................... 56

23
5 – RESULTADOS .............................................................................................. 58
5.1 ESTUDOS in vivo............................................................................................ 58
5.2 ESTUDOS in vitro........................................................................................... 75
5.3 ENSAIOS BIOQUÍMICOS............................................................................... 88
6 – DISCUSSÃO................................................................................................... 103
7– CONCLUSÕES................................................................................................ 118
8– PERSPECTIVAS............................................................................................. 120
9– REFERÊNCIAS............................................................................................... 122
ANEXOS............................................................................................................... 149
Certificado do Comitê de ética
Vita
Publicações

24
Introdução

25
1. INTRODUÇÃO
1.1. Sistema cardiovascular: O endotélio e mediadores endoteliais
1.1.1 Homeostase cardiovascular
O controle do sistema cardiovascular envolve diferentes mecanismos e tem
por objetivo manter a homeostase do organismo promovendo um aporte de
substâncias essenciais para manutenção dos tecidos. A regulação da pressão
arterial (PA) é exercida por sistemas de retroalimentação que operam momento a
momento ou a longo prazo e dependem de uma interação do sistema nervoso
simpático e hormônios circulantes (COWLEY; ROMAN; KRIEGER, 1991; GUYTON,
1981).
A pressão arterial é regulada a curto prazo por sistemas de barorreceptores,
quimioreceptores e receptores cardiopulmonares (neurônios especializados no arco
aórtico e seios carotídeos), cujas aferências se projetam para o sistema nervoso
central, especificamente ao núcleo do trato solitário (NTS) via nervos vagos e
glossofaríngeo. O processamento dessas informações no sistema nervoso central
produz uma regulação das vias autonômicas eferentes, havendo, assim, o controle
da distribuição do débito cardíaco em diferentes leitos vasculares. Este evento
fornece um feedback negativo em que a pressão arterial elevada reflexivamente
provoca diminuição da pressão; em contraste, a diminuição da pressão arterial
deprime o barorreflexo, fazendo com que a pressão arterial aumente. Em níveis
normais de pressão arterial, os barorreceptores inibem tonicamente os efeitos
simpáticos sobre os vasos sanguíneos e coração (TAYLOR; BISOGNANO, 2010).
O controle da PA a longo prazo é exercido pelo sistema renina-angiotensina-
aldosterona com a regulação do volume dos líquidos corporais (volemia), regulando
o equilíbrio hidroeletrolítico do corpo. A pressão arterial corresponde ao produto do
débito cardíaco (DC) pela resistência vascular periférica total (RVPT), e pode ser
influenciada pela ação de drogas sobre um ou ambos os parâmetros (MARC;
LLORENS-CORTES, 2011). A resistência vascular é influenciada, em graus
variados, dependendo da região, pela atividade de nervos simpáticos vasomotor,
pelo nível de hormônios vasoativos circulantes e por fatores locais, incluindo fatores
metabólicos produzidos pela camada endotelial (THRASHER, 2006).

26
1.1.2 O endotélio: Foco nos fatores de regulação do tônus vascular
O endotélio vascular é um importante órgão endócrino, formado por uma
monocamada de células, que exerce papel fundamental no controle de fluidez de
sangue, agregação plaquetária e regulação do tônus vascular em resposta a
hormônios vasoativos ou metabólitos, assegurando assim a provisão adequada de
nutrientes (FÉLÉTOU; KÖHLER; VANHOUTTE, 2011). As células endoteliais
vasculares são fisiologicamente expostas a forças hemodinâmicas, como a força de
cisalhamento (shear stress). Essas células sintetizam fatores que conduzem à
contração ou ao relaxamento do músculo liso vascular. Os principais fatores
contracturantes são os derivados dos metabólitos do ácido araquidônico (AA) pela
ciclooxigenase (COX) (tromboxano (TXA2) e prostaglandinas (PGH2)), as espécies
reativas de oxigênio (ROS) e endotelina-1 (ET-1). Os fatores vasodilatadores
endoteliais são o óxido nítrico (NO), metabólitos do AA produzidos pelas enzimas
COX (prostaglandinas (PGI2)), lipoxigenase (ácido 15-s-hidroxieicosatetraenóico –
15-HETE) e citocromo P450 (CYP450), como ainda o fator hiperpolarizante derivado
do endotélio (EDHF) (FÉLÉTOU; KÖHLER; VANHOUTTE, 2010; JIN, 2011).
Estes fatores são secretados pelo endotélio e se ligam principalmente a
receptores acoplados a proteína G produzindo um aumento do cálcio intracelular em
resposta a diferentes estímulos: autacóides (bradicinina BK), hormônios circulantes
(angiotensina II), neurotransmissores (acetilcolina, noradrenalina) e ainda produtos
derivados de plaquetas e coagulação (serotonina, trombina) sendo responsável pela
ativação de diferentes enzimas produzindo diferentes efeitos vasoativos (TRIGGLE;
DING, 2011).
A) Fatores Contracturantes:
As contrações dependentes do endotélio são bloqueadas por antagonistas do
receptor de tromboxano (TP), indicando que derivados do AA são gerados em
direção a células musculares lisas vasculares e ativam diretamente os receptores. O
AA é o substrato preferencial da COX-1 e COX-2, produzindo eicosanóides
biologicamente ativos os quais são fatores contracturantes. O TXA2 e a PGH2
exercem uma maior importância no controle do tônus vascular por induzir a ativação
da via proteína G-fosfolipase C (PLC) e aumento do cálcio, levando à contração da
célula muscular (WONG; VANHOUTTE, 2010).

27
Endotelina -1 (ET1) é um vasoconstrictor ativador do subtipo de receptor para
endotelina A (ETA) ou B (ETB), em células musculares vasculares, a ET1 leva à
ativação de receptores acoplados a proteína G, predominantemente, Gq/11 e G12
levando a vias de mobilização do cálcio intracelular e ativação de vias dependentes
da RhoA/ Rho-cinase. No entanto, a ativação dos receptores ETB presentes na
célula endotelial pode levar à ativação de fatores relaxantes derivados do endotélio
(RUBANYI, 2011).
As forças de cisalhamento podem induzir contração por produzir, na célula
endotelial, espécies reativas de oxigênio (ROS), como H2O2 e O2 . Estes podem ser
produzidos pelas enzimas NADPH oxidase, xantinas oxidases e ainda eNOS e COX,
principalmente na ausência de seus substratos, formando ainda peróxidos de nitrito
ao interagir com o NO (FISSLTHALER, et al. 2007).
B) Fatores Relaxantes:
Vários trabalhos descrevem a participação do endotélio vascular em
relaxamentos induzidos por uma variedade de substâncias químicas (FURCHGOTT;
ZAWADZKI, 1980; FURCHGOTT, 1983, MONCADA et al., 1988) demonstrados na
figura 1. Eicosanóides, derivados do AA, são constitutivamente produzidos pelas
células endoteliais e regulam a função vascular. Em humanos, a COX-2 parece ser o
maior contribuinte da produção de prostaciclina nas células endoteliais, embora a
COX-1 também apresente como uma importante fonte. A síntese de prostaciclina
(PGI2) é dependente da formação do AA, aciona receptores ligados à proteína Gs,
células musculares lisas, e ativam a ciclase de adenilil e resulta no aumento de
AMPc que, via PKA, induz o relaxamento. (TRIGGLE; DING, 2011).
Outro fator que desempenha um papel na vasodilatação mediada por fluxo e
contribui para o relaxamento dependente do endotélio é o fator hiperpolarizante
derivado do endotélio (EDHF). Sua formação pode ser dependente da sinalização do
cálcio intracelular, induzida pela ativação de receptores acoplados à proteína G. No
entanto, a natureza do fenômeno EDHF é questionada; Sabe-se apenas que ocorre
uma hiperpolarização dependente da ativação de canais de potássio dependentes
do cálcio com média e pequena condutância localizados nas células endoteliais. A
hiperpolarização endotelial é um pré-requisito para a hiperpolarização e relaxamento
de células musculares lisas vasculares (JIN et al. 2011). A transmissão da
hiperpolarização entre o endotélio e músculo vascular, produzida por junções tipo

28
gap mioendoteliais, implica na ativação de outros canais de potássio, como os
canais retificadores de entrada, e ativação da bomba Na+/K+ ATPase, aumentando o
estado hiperpolarizado da célula. Esta hiperpolarização é o principal efeito que
produz o fechamento dos canais de cálcio sensíveis à voltagem (CaV), ocorrendo
diminuição da concentração de cálcio intracelular e relaxamento da musculatura lisa
vascular. Atualmente, várias hipóteses são descritas para determinar a natureza
estrutural e bioquímica do EDHF, entre elas os metabólitos da enzima CYP450,
ácidos epoxieicosatrienóicos (EET), íons potássio (K+), peróxido de hidrogênio
(H2O2) e radicais nitroxil (HNO) (EDWARDS; FÉLÉTOU; WESTON, 2010).
Furchgott e Zawadzki (1980) descreveram que a ação de alguns
vasodilatadores, como a acetilcolina, era inteiramente dependente da presença do
endotélio intacto e envolvia a liberação de um fator essencial para o relaxamento
vascular, o qual foi chamado de endothelial-derivated relaxing factor (EDRF).
Posteriormente, baseados em semelhanças químicas estruturais com o EDRF,
investigadores concluíram que o endotélio era capaz de produzir óxido nítrico (NO),
tal produção é dependente da ativação da enzima sintase de óxido nítrico endotelial
(eNOS), resultado da conversão da L-arginina por estímulos externos que podem
induzir a sinalização dependente do cálcio (MONCADA et al. 1988).
Figura 1: Fatores relaxantes derivados do endotélio. Representação da produção de fatores dependentes da mobilização do cálcio na célula endotelial. PGI2: Prostaciclina, NO: Óxido Nítrico, EDHF: Fator hiperpolarizante derivado do endotélio (Adaptado de Vanhoutte, 1998)

29
1.2 Óxido Nítrico: biosíntese e função vascular
Uma das moléculas mais importantes sintetizadas pela célula endotelial é o
óxido nítrico (NO), um radical livre, gasoso, inorgânico, incolor, com uma meia vida
relativamente curta (MONCADA; PALMER; HIGGS, 1991). A produção de NO,
promovida pela conversão enzimática do aminonoácido L-arginina, é constituída de
duas etapas (Figura 2) (RAFIKOV, et. al. 2011). A primeira é uma N-hidroxilação do
grupo guanidina da L-arginina, formando um intermediário N-hidróxi-L-arginina (L-
NOHA) na presença de O2 e cofatores essenciais como NAD(P)H e (6R-)5,6,7,8-
tetrahidro-L-biopterina (BH4), na segunda etapa, L-NOHA é metabolizada em L-
citrulina e NO.
Figura 2: Esquema da biosíntese do óxido nítrico. RAFIKOV, et. al. 2011
Devido à sua natureza lipofílica, o NO difunde-se através das células da
musculatura lisa adjacentes, e pode atuar estimulando a ciclase da guanilil,
metabolizando o GTP e transformando-o em GMPc, que por sua vez, ativa a
proteína cinase G (PKG) promovendo a recaptação de Ca2+ para os estoques
intracelulares, via bomba de cálcio (SERCA), abertura dos canais de K+; fechamento
dos canais de Ca2+. Todos estes eventos levam à redução da concentração de
cálcio intracelular e vasorrelaxamento (FURCHGOTT, 1983; VANHOUTTE;
BOULANGER, 1995). A característica de radical livre do NO com meia-vida biológica
curta permite que a ligação do radical do NO ao grupo de heme de ciclase de guanilil
seja um processo reversível. No entanto, autores propuseram que o NO poderiam
ativar diretamente canais para K+ do músculo liso vascular, independente da
ativação da ciclase de glanilil solúvel, levando a hiperpolarização e ao relaxamento
vascular (BOLOTINA et al. 1994; MISTRY; GARLAND, 1998) .

30
A viabilidade do NO é promovida pela ativação da enzima sintase de óxido
nítrico (NOS). Esta produção de NO pode ser dependente ou independente do
aumento de Ca2+ que ativa a NOS em três isoformas: A sintase de óxido nítrico
neuronal (nNOS), induzível (iNOS) e endotelial NOS (eNOS). Em células endoteliais
foram caracterizadas duas diferentes isoenzimas, a eNOS e a iNOS (SCHINI-
KERTH; VANHOUTTE, 1995)
1.3 Mecanismos de ativação da enzima eNOS:
A isoforma da sintase de NO endotelial (eNOS) é um determinante chave da
homeostase vascular e é regulada por diversos receptores de superfície celular. A
atividade da eNOS é caracterizada através da ligação da calmodulina ligada ao
cálcio (CAM-Ca2+) e por alterações na fosforilação pela ação de cinases específicas
(RAFIKOV, et al. 2011). Além disso, proteínas interagem com eNOS e regulam sua
atividade, como a proteína de estresse de 90kDa (hsp90) que age como um
modulador de ativação alostérica e promotor do (des)acoplamento da eNOS
(ISENOVIĆ et al. 2011). Caveolina-1 é uma proteína de ancoragem de cavéolos, de
grande interesse e tem demonstrado atenuar a atividade da eNOS, levando à
inibição da enzima em um processo reversível modulado pela interação da CAM-
Ca2+ (DRAB, et al. 2001, MICHEL; VANHOUTTE, 2010). O recrutamento de CAM-
Ca2+ e hsp90 pode deslocar a caveolina-1 levando levar a ativação da eNOS
(GRATTON, et al. 2000, RATH; DESSY; FERON, 2009) (Fig 3).
Figura 3: Representação do cavéolo, da caveolina-1 e interação com a eNOS. HSP90 (proteína de estresse de 90 kDa); CAM (Calmodulina); eNOS (sintase de NO) (Adaptado de Lucy et al. 2003).

31
Elevações da concentração de Ca2+ intracelular permitem a formação do
complexo CAM-Ca2+ levando a ativação da eNOS. Receptores metabotrópicos,
como os para bradicinina (B1), tem sido relacionados com o aumento do Ca2+ por
ativar a proteína fosfolipase Cβ, convertendo o PIP2 em inositol 1, 4, 5, trifosfato (IP3)
e diacilglicerol (DAG). A interação do IP3 com seu receptor, no retículo
sarcoplasmático, promove a liberação do Ca2+ no meio extracelular, levando à
ativação de canais iônicos (como os canais para Ca2+ operados por voltagem, (CaV))
influenciados em sua maior parte pela PKC (VENEMA, 2002, BIRD, 2011).
Entretanto, estímulos que independem das concentrações plasmáticas de Ca2+,
como a ativação de proteínas cinases, podem induzir a fosforilação da eNOS em
sítios de ativação como resíduos de serina (Ser - em 1177, 635, 617, 615, 116) e
tirosina (Tyr - 567) e resíduos inibitórios como Tyr-81 e treonina (Thr - 495)
(SCHINI-KERTH; VANHOUTTE, 1995; FULTON et. al., 1999; LIN et. al., 2003,
FLEMING, 2010, FÖRSTERMANN; SESSA, 2011). O papel das proteínas cinases
na regulação da eNOS é um tópico de interesse para investigações, assim sendo,
vários estudos tem indicado proteínas cinases que fosforilam diferentes resíduos de
serina e modular a atividade da eNOS (Figura 4).
A identificação farmacológica permitiu a descrição da fosforilação em Ser1177
como alvo de um grande número de proteínas cinases, incluindo a proteína cinase A
(PKA), dependente da concentração de AMP cíclico, (SHAH; SINGH, 2006, BIRD,
2011). Mecanismos de sinalização que culminam na fosforilação da eNOS em Ser
1177 e Ser 615 foram inicialmente demonstrados em estudos independentes que
relataram a participação da via fosfatidil-inositol 3-cinase (PI3K)/ AKT em resposta a
estímulos mecânicos, como alterações do fluxo sanguíneo (shear stress) ou
receptores com ação catalítica, por exemplo, a resposta endotelial à insulina
(FULTON et. al., 1999, CONTRERAS et. al., 2011). Eventos adicionais a estes
estímulos extracelulares, tais como alterações de ATP, hipóxia e fator de
crescimento endotelial vascular (VEGF) são descritos ainda para relacionar o papel
da proteína cinase ativada por 5’-AMP (AMPK) que; após a fosforilação da porção α
em Thr 172 e consequente ativação da subunidade catalítica, produz a fosforilação
da eNOS em ser 1177 (LEVINE; LI; MICHEL, 2007, COLOMBO; MONCADA, 2009,
FISSLTHALER; FLEMING, 2010; STAHMANN et. al., 2010).
Mecanismos de transativação de proteínas cinases dependentes da
concentração de cálcio intracelular são descritas ainda para explicar os mecanismos

32
de ativação da eNOS. SCHNEIDER e colaboradores (2003) demonstraram que a
proteína cinase da cinase dependente da cálcio-calmodulina (CaMKK) ativa cinases
serina/treonina específicas que agem sobre a proteína Ca2+-CaM, como a proteína
cinase dependente de cálcio calmodulina (CAMK) I, II e IV. Estudos com inibidores
da CAMK II demonstraram a ação desta proteína em fosforilar resíduos de Ser 615 e
Ser 1177 da eNOS, levando a sua ativação e produção de NO (CAI; LIU; GARCIA,
2008). Estímulos decorrentes do estresse oxidativo levam à regulação de vias que
causam a ativação da proteína cinase C (PKC) (HEO; FUJIWARA; ABE, 2011). A
PKC interfere no processo de ativação da eNOS por fosforilar o resíduo de Thr 495,
uma vez que a desfosforilação desse resíduo está associada ao aumento da
atividade da eNOS e estímulos que elevam as concentrações de Ca2+ intracelulares
que culminam na ativação da PKC (XIE et. al., 2011).
Evidências apontam para a importância das alterações na atividade da eNOS
para a função endotelial. Modificações pós-tranducionais da atividade da enzima
estão implicadas em perturbações da sinalização dependente de endotélio que
originam a disfunção endotelial contribuindo para o desenvolvimento da doença
cardiovascular (VANHOUTTE, 2011).
Figura 4: Representação de proteínas cinases envolvidas na fosforilação da eNOS. Alterações do fluxo sanguíneo produzem estimulação de mecanoreceptores sensíveis ao estiramento que induzem a fosforilação da eNOS por proteínas cinases AKT (Ser 1177, 617), AMPK (Ser 1177), PKA (Ser 1177, 635) e CAMKII (Ser 1177) (Adaptado de ZHANG et al. 2009).

33
1.4. Disfunção endotelial associada à hipertensão: Alvos para tratamento
A disfunção endotelial é definida como um desequilíbrio de fatores vasoativos
derivados do endotélio, levando à vasoconstrição excessiva e mudanças estruturais
na parede do vaso; é um evento precoce na fisiopatologia das principais doenças
cardiovasculares (SERBAN; NILIUS; VANHOUTTE, 2010). É um distúrbio de
múltiplas facetas, que tem sido associado com hipertensão de diferentes etiologias,
que envolvem não apenas alterações da via L-arginina - NO-sintase - ciclase de
guanilil solúvel, mas também a capacidade de reduzir hiperpolarizações dependente
do endotélio e aumentar a produção de fatores contracturantes (FELÉTOU;
KÖHLER; VANHOUTTE, 2010).
A alteração da função vascular pode ser individualizada em diferentes
eventos como o aumento da produção de espécies reativas de oxigênio (ROS) e
outros radicais livres, que são capazes de induzir o estresse oxidativo, promovendo
vasoconstrição e remodelamento vascular (HEO; FUJIWARA; ABE, 2011). Outro
aspecto importante é a produção de agentes vasoconstrictores, em particular
derivados prostanóides, e formação de peptídeos como a endotelina. Portanto,
modulações da função celular que podem levar disfunção endotelial em pacientes
hipertensos e no envelhecimento, bem como a utilização de compostos
antioxidantes para prevenção e/ou inibidores da ação de vasoconstrictores têm sido
alvos de constantes estudos (VANHOUTTE, 2011).
A literatura mostra que atividade reduzida de NO é a referência atual para o
reconhecimento de disfunção endotelial (BOURQUE; DAVIDGE; ADAMS 2011).
Situações que levam ao estresse oxidativo estão envolvidas com alterações na
expressão de eNOS com diminuição da produção de NO e reduzida capacidade de
converter a L-arginina, estes eventos estão relacionados a diminuição da expressão
ou o desacoplamento da eNOS, entretanto, a formação de peróxido de hidrogênio
pode induzir um aumento da expressão da enzima (KOLLURU; SIAMWALA;
CHATTERJEE, 2010, FELÉTOU; KÖHLER; VANHOUTTE, 2011, ISENOVIĆ, et. al.
2011).
Achados mostram que o restabelecimento e a conservação da sinalização
adequada do NO estão associados aos tratamentos efetivos de doenças
cardiovasculares, como a hipertensão. Em particular, são descritos experimentos
que modulam a eNOS: por aumentar a viabilidade do seu substrato e de cofatores,

34
induzir a transcrição ou melhorar a sua atividade, ou ainda, que possam prevenir o
seu desacoplamento (BRAAM;VERHAAR, 2007, BOURQUE; DAVIDGE; ADAMS,
2011).
Outras estratégias terapêuticas têm sido delineadas para restaurar a atividade
vascular na disfunção endotelial, entre elas, a regulação da via ciclase de guanilil
solúvel, alvo fisiológico do NO, que estimula a enzima e utiliza moduladores
alostéricos favorecendo a atividade da via NO–GMPc, bem como a utilização de
inibidores de fosfodiesterase 5 (PDE5) e assim, manter a produção de GMPc na
célula muscular lisa vascular (KASS; CHAMPION; BEAVO, 2009; PRIVIERO;
WEBB, 2010; STASCH; HOBBS, 2009).
Recentemente, a maioria dos estudos sobre os mecanismos associados com
insuficiência da vasodilatação na hipertensão tem direcionado ao papel do EDHF
(BRÄHLER, et al. 2009, GARLAND, et al. 2010). Respostas hiperpolarizantes
endotélio-dependente mediadas pelo EDHF podem fornecer uma reserva do efeito
vasodilatador na hipertensão e compensar, ao menos temporariamente, a disfunção
endotelial devido à síntese comprometida ou disponibilidade de NO (VANHOUTTE,
et al. 2009). A via de sinalização do EDHF envolve a participação dos íons K+ e as
junções gap mioendoteliais com ativação de diferentes KCa endoteliais. No entanto,
como a natureza do EDHF e sua capacidade de induzir vasodilatação estão sendo
reveladas, ações farmacológicas que possam mimetizar as ações hiperpolarizantes
têm seu interesse crescente (SCHINI-KERTH, et al. 2011, DAL-ROS, et al. 2010).
Das diversas causas de hipertensão arterial, a sua maioria permanece de
etiologia desconhecida. Caracterizada como uma doença poligênica, com influência
dos fatores ambientais (Krieger, et al.,) Na hipertensão são descritas alterações
hemodinâmicas e fisiopatológicas, incluindo anormalidades no músculo liso vascular,
hipertrofia ventricular, disfunção endotelial, síndrome metabólica, estado pró-
coagulativo, entre outras (JULIUS, 2007).
A hipertensão é frequentemente alvo nos estudos de desenvolvimento de
novas drogas, nos quais são utilizados modelos experimentais em animais que
apresentam alterações fisiológicas semelhantes àquelas encontradas em humanos.
Diferentes modelos são propostos, entre eles o rato espontaneamente hipertenso
(SHR) com a utilização do controle normotenso Wistar-Kyoto (WKY). Este modelo é
o mais usado, devido às semelhanças com as características genéticas encontradas
em seres humanos. No entanto, outros modelos são utilizados como dependentes

35
de infusão de angiotensina II, modelo de hipertensão renal com constrição de
artérias renais (2R1C), administração crônica de inibidores da enzima NOS, ou
diminuição da secreção renal de sal, os quais têm sido estudados e seus parâmetros
vasculares e cardíacos investigados (EDRIS et al., 2007).
Dessa forma, embora existam muitos medicamentos para o tratamento da
hipertensão arterial, há um grande interesse na pesquisa de novos produtos
bioativos para encontrar alternativas ao tratamento de hipertensão (PAULIS;
UNGER, 2010; TOMASONI et. al., 2010). Estudos experimentais e clínicos indicam
que produtos naturais possuem um importante papel no desenvolvimento de novas
drogas e sugerem que metabólitos secundários obtidos de plantas apresentam um
desempenho em melhorar a função dos vasos sanguíneos e, portanto, proteger o
sistema vascular (DIAS et. al. 2007, CAVALCANTE, et. al., 2010, WALLACE, 2011).
1.5 Produtos Naturais: Monoterpenos e α-terpineol.
Atualmente tem-se verificado valiosos avanços envolvendo os compostos
químicos e/ou metabólitos derivados de plantas em vários processos farmacológicos
e bioquímicos (BARBOSA-FILHO, 2008). Devido à complexidade da composição
química dos óleos essenciais, diversas ações farmacológicas são apresentadas e
demonstrando o interesse vislumbrando o desenvolvimento de novas drogas. Estes
óleos essenciais apresentam, como constituintes majoritários, os terpenos -
monoterpenos (cerca de 90% dos óleos essenciais) que são considerados, em
muitos casos, como responsáveis pelos odores de plantas aromáticas, seguido dos
sesquiterpenos, diterpenos e fenilpropenos (SANTOS et al., 2011). Os terpenóides
são hidrocarbonetos que possuem como unidade básica, o isopreno
[CH3C(CH2)CH2CH2]. A classificação básica dos vários terpenos decorre do número
de unidades isoprênicas que contêm. Os monoterpenos são constituídos de duas
unidades de isopreno e são divididos em três subgrupos: acíclicos (ex. linalol),
monocíclicos (ex. α-terpineol) e bicíclicos (ex. cânfora).
Os monoterpenos têm representado uma nova classe de agentes químicos
com elevado potencial terapêutico (TISSERAND e BALACS, 1995). São relatadas
ações diversas destes compostos na literatura, dentre elas, efeito anti-neoplásico
(JIRTLE, 1993), atividades antimicrobianas (GARCIA et al. 2008b), antioxidante
(SINGH, 2010), agonistas de canais TRP (CALIXTO et al., 2005), antinociceptiva

36
(GONÇALVES et al. 2008), antiespasmolítica (MAGALHÃES et al. 1998). Recentes
estudos com monoterpenos sobre as ações cardiovasculares têm demonstrado
atividades vasorelaxantes e hipotensoras (GUEDES et al. 2004, BASTOS et al.
2010, MENEZES et al. 2010).
Deste modo, estudos com monoterpenos vêm sendo desenvolvidos no nosso
grupo de pesquisa, os estudos realizados por GUEDES e coloboradores (2002;
2004) utilizando a rotundifolona demonstraram hipotensão associado aos efeitos
vasorelaxantes com produção de EDRF’s e inibição do influxo de cálcio em ratos.
Estes efeitos demonstram que monoterpenos são promissores em prevenir as
complicações vasculares decorrentes do processo de hipertensão. Neste contexto,
Magalhães e colaboradores (1998; 2008) avaliaram os efeitos cardiovasculares do
óleo essencial de Croton nepetaefolius e seus constituintes majoritários metileugenol
e α-terpineol. Estes monoterpenos demonstraram atividades antiespasmódicas,
capazes de diminuir a resistência vascular de leito mesentérico.
Uma triagem farmacológica preliminar realizada em nosso laboratório com o
α-terpineol e seus análogos demonstrou uma atividade vasorelaxante utilizando a
metodologia in vitro para artéria mesentérica superior. Em adição, estudos anteriores
realizados no nosso grupo demonstraram que o -terpineol, 1-metil-4-isopropil-1-
ciclohexen-8-ol (Figura 5), produziu hipotensão e vasorrelaxamento dependente da
produção dos metabólitos produzidos pelo endotélio vascular com possível
envolvimento da enzima sintase de óxido nítrico (RIBEIRO, 2008). Nesse sentido,
estudos adicionais são pertinentes para avaliar, no sistema cardiovascular, a
capacidade do -terpineol em aumentar a disponibilidade de NO, em favorecer a
ocorrência de respostas mediadas pelo EDHF, ou ainda, determinar os efeitos que
interfiram na ação de fatores contracturantes. Estas respostas são fundamentais
para restaurar a função endotelial adequada e assim retardar o aparecimento de
complicações vasculares decorrentes no processo da hipertensão.
Figura 5: Estrutura química do α-terpineol (C10 H17 O1; MM=154)

37
Objetivos

38
2. OBJETIVOS
2.1 Geral
Investigar os mecanismos cardiovasculares do -terpineol em ratos
espontaneamente hipertensos.
2.2 Específicos
Avaliar as ações cardiovasculares induzidas pelo -terpineol in vivo utilizando-
se animais hipertensos;
Caracterizar a influência do sistema nervoso autônomo no efeito hipotensor
induzido pelo -terpineol em ratos hipertensos.
Investigar a influência do -terpineol na sensibilidade do barorreflexo em ratos
SHR e normotensos WKY.
Determinar o relaxamento vascular induzido pelo -terpineol em artéria
mesentérica superior de animais hipertensos;
Verificar a participação das vias endoteliais NO/GMPc, da via PGI2/AMPc e
EDHF envolvidos neste efeito vasorelaxante.
Avaliar os níveis da produção de NO em células endoteliais tratadas com -
terpineol.
Investigar o sítio de fosforilação da eNOS responsável pela ativação desta
enzima em resposta ao -terpineol em cultura primária de células endoteliais.
Pesquisar a participação de proteínas cinases como AKT e AMPK envolvidas
na fosforilação da eNOS induzida pelo -terpineol em células endoteliais.
Estudar o envolvimento dos receptores endoteliais muscarínicos (M3) no
vasorrelaxamento de artéria mesentérica de ratos hipertensos
Definir a participação dos canais de K+ na vasodilatação induzida pelo -
terpineol em ratos hipertensos.

39
Materiais

40
3. MATERIAIS
3.1 Animais:
Os animais utilizados foram ratos da espécie Rattus norvegicus, variedade
Wistar Kyoto normotensos (WKY) e ratos espontaneamente hipertensos (SHR),
todos machos e adultos (3 a 4 meses), pesando entre 250- 300g. Os animais foram
provenientes do biotério Prof. George Thomas do núcleo de pesquisa do Centro de
Biotecnologia da Universidade Federal da Paraíba. Os animais foram mantidos sob
condições de temperatura controlada (21 ±1ºC) e ciclo claro e escuro de 12 h (6-18
h), tendo livre acesso à água e a ração (Purina, Brasil).
3.2 Obtenção do -terpineol:
O monoterpeno -terpineol (Sigma/ Aldrich – EUA) e gentilmente cedido pelo
prof. Damião P. de Souza, Universidade Federal de Sergipe,
3.3 Substâncias e sais:
Cloridrato de acetilcolina (ACH); indometacina (INDO); glibenclamida (GLIB)
hidroxicobalamina (HDX); L (-) arginina; L (-) fenilefrina; nitroprussiato de sódio; N-
nitro-L(-) arginina-metil éster (L-NAME); ODQ (1H-[1,2,4] oxadiazolo [4,3,-
quinoxalino-1-ona), sulfato de atropina, cloridrato de tetraetilamônio (TEA), 4-
aminopiridina (4-AP) caribdotxina, apamina, cremofor, dimetilsulfóxido (DMSO),
albumina sérica bovina, HEPES (N-2-hidroxietilpiperazina-N’-2-etano-ácido
sulfônico), ortovanadato de sódio (Na3VO4), fosfato de sódio, fluoreto de sódio
(NaF), ácido ocadáico foram obtidos da empresa Sigma – Aldrich (EUA). Duodecil
sulfato de sódio (SDS) e kit de Bradford para quantificação de proteínas obtido da
Bio-Rad Laboratories (Califórnia - EUA). Cloreto de cálcio dihidratado (CaCl2.2H2O),
cloreto de potássio (KCl), cloreto de sódio (NaCl), glicose (C5H12O6), cloreto de
magnésio hexahidratado (MgCl2.6H2O) foram obtidos da empresa Merck (EUA).
Fosfato monossódico 1-hidratado (NaH2PO4.H2O), bicarbonato de sódio (NaHCO3)
da empresa Vetec (Brasil). Tiopental sódico (Cristália, Brasil). Sulfato de heparina e
inibidor de protease (Roche, Alemanha).

41
A indometacina foi dissolvida juntamente com o bicarbonato de sódio
(NaHCO3) a 5% em água destilada, o ODQ foi dissolvido com o DMSO e a GLIB foi
dissolvida em etanol PA (95%). As demais soluções estoques foram dissolvidas em
água destilada. Todas as soluções foram mantidas a 18 °C e, imediatamente antes
dos experimentos, diluídas em salina ou água destilada, para ensaios in vivo e in
vitro, respectivamente. As concentrações utilizadas de NaHCO3 (5%) e DMSO
(0,1%), nas soluções não apresentaram qualquer efeito sobre as preparações
controle (dados não demonstrados).
3.4. Soluções nutritivas:
Para a preparação das soluções nutritivas foram utilizadas as seguintes
substâncias em mM: cloreto de sódio (NaCl) 158,3; cloreto de potássio (KCl) 4;
cloreto de cálcio di-hidratado (CaCl2); 2, sulfato de magnésio hepta-hidratado
(MgSO4.7H2O) 1,05; glicose (C6H12O6) 5,6; bicarbonato de sódio (NaHCO3) 10.
Todas estas soluções foram mantidas em carbogênio (95 % de O2 e 5 % de
CO2) a 37ºC. Nas preparações das soluções despolarizantes de Tyrode com cloreto
de potássio a 20 mM, a concentração de sódio foi isosmoticamente alterada.
3.5 Preparação da solução de -terpineol:
O -terpineol foi solubilizado em cremofor 1% e diluídos em água destilada na
concentração de 10-2 M para os experimentos in vitro e diluídos em salina na
concentração de 20 mg/mL para experimentos in vivo. As concentrações utilizadas
cremofor na cuba não excedeu 0,01%. Nesta concentração o cremofor não
demonstra qualquer efeito em anéis de artéria mesentérica superior de rato.
Todas as soluções foram estocadas a 18 °C e, imediatamente antes dos
experimentos, diluídas em salina ou água destilada, para ensaios in vivo e in vitro,
respectivamente, de acordo com a necessidade de cada protocolo experimental.

42
Métodos

43
4 MÉTODOS
Foram utilizadas diferentes abordagens: ensaios farmacológicos in vivo, com
animais íntegros, e ensaios farmacológicos in vitro, com órgãos isolados e cultivo de
células endoteliais.
4.1 Ensaios Farmacológicos in vivo.
4.1.1 Medida direta de pressão arterial e freqüência cardíaca em ratos Wistar
Kyoto normotensos (WKY) e espontaneamente hipertensos (SHR) não
anestesiados.
A pressão sanguínea intra-aórtica foi registrada em animais normotensos e
hipertensos, não-anestesiados, de acordo com a técnica descrita por Botelho-Ono
(2010). Brevemente, 24 horas antes da realização dos experimentos, os animais
foram anestesiados com cetamina + xilazina (80mg + 4mg/ kg), e implantou-se
catéteres de polietileno (PE), um segmento de PE-10 (diâmetro interno e externo de
0,28 - 0,61 mm, respectivamente), acoplado a um segmento de PE-50 (diâmetro
interno e externo de 0,58 - 0,96mm, respectivamente). Foram implantados na aorta
abdominal inferior e na veia cava inferior, via artéria e veia femoral esquerda,
respectivamente. A redução do diâmetro do segmento PE-10 tem como finalidade
minimizar o risco de isquemia na perna cateterizada sem, no entanto, alterar o sinal
de pressão arterial (Figura 6). Após a inserção e fixação, os catéteres foram
tunelizados subcutaneamente e exteriorizados através de uma incisão na região
cervical posterior do animal (scapulae). A PA e FC foram medidas 24 h após o ato
cirúrgico pela conexão do cateter arterial a um transdutor de pressão pré-calibrado
acoplado a um amplificador (LabTrax 2-24T, World Precision Instruments - WPI,
Sarasota, FL, USA) e este, conectado a um computador e com o programa Datatrax
2 (WPI, Sarasota, FL, USA) para aquisição e tratamentos de sinais biológicos em
animais de pequeno porte (Figura 7). O cateter venoso foi implantado para a
administração das drogas.

44
Figura 6: Representação esquemática dos vasos onde foram implantados os cateteres para o registro dos parâmetros cardiovasculares e administração de drogas.
Figura 7: Aparato utilizado para as medidas de pressão arterial e frequência cardíaca em ratos

45
4.1.2 Protocolos experimentais empregados nos estudos in vivo.
Foram utilizados 10 animais normotensos WKY e 9 hipertensos SHR. Após
um período de recuperação de 24 horas o catéter aórtico foi conectado ao transdutor
de pressão para registro da PA e FC. Um período antes do início dos experimentos
foi permitido aos animais para que assim seus valores de PA e FC estabilizassem.
Para verificar a correta implantação do catéter venoso, foi administrado o
nitroprussiato de sódio, nas doses de 10 µg/kg. Após 15 min., doses crescentes de
-terpineol foram administradas de forma randomizada com o objetivo de verificar o
efeito sobre os parâmetros analisados. As doses administradas de -terpineol
obedeceram a intervalos de aproximadamente 1h para que os parâmetros
cardiovasculares retornassem aos seus valores da linha de base (Figura 8). Os
valores de PAM e FC foram computados antes (valores da linha de base) e
imediatamente após a administração de -terpineol, e suas variações foram
expressas para cada dose, calculadas através da seguinte fórmula:
= Variação dos valores de pressão arterial
PA depois = Valores de PA depois da administração das drogas
PA antes = Valores de PA antes da administração das drogas
Figura 8: Representação esquemática do protocolo experimental. Protocolo da
administração de doses crescentes de -terpineol em ratos WKY e SHR antes e após tratamento agudo com diferentes inibidores.
= PA depois – PA antes

46
4.1.2.1. Avaliação do controle autonômico nas variações da PA e da FC
induzidas pela administração de α-terpineol em ratos não-anestesiados WKY e
SHR.
Depois do período de estabilização dos parâmetros cardiovasculares, a DE50
de -terpineol (4.8 mg/Kg, i.v.) foi administrado e os efeitos registrados. Em seguida
os animais foram tratados em grupos separados com atropina (2 mg/kg, ,i.v, n=6),
um antagonista muscarínico não seletivo, ou hexametônio (30 mg/kg, ,i.v, n=6), um
bloqueador ganglionar, ou atenolol (20 mg/kg,i.v, n=6), um bloqueador dos
receptores β1, ou prazosin (1 mg/kg, i.v, n=5) antagonista dos receptores α1, e 30
minutos depois, as mesmas doses do monoterpeno, obedecendo a mesma
sequência anterior, foram administradas, obtendo-se uma nova curva dose-resposta
para de -terpineol. As influências do tratamento foram obtidas por comparações
dos valores da PA e FC da condição anterior (controle) com as registradas após a
administração do antagonista.
4.1.2.2. Verificação da participação da enzima sintase de óxido nítrico (NOS) no
efeito cardiovascular induzido por -terpineol em ratos normotensos e
hipertensos não-anestesiados.
Após estabilização dos parâmetros hemodinâmicos, a DE50 de -terpineol (4.8
mg/Kg, i.v.) foi administrada e os valores de PAM e FC foram então registrados,
como descrito anteriormente. Após o retorno dos valores de PAM e FC a níveis
basais, os animais foram tratados agudamente com L-NAME 20 mg/Kg, i.v., um
inibidor da NO-sintase, (MONCADA; HIGGS, 1993) e após 30 minutos, a DE50 de -
terpineol (4.8 mg/Kg, i.v., n=7) foram administradas conforme descrito anteriormente
(Figura 7). Mudanças na PAM e na FC induzidas por -terpineol, foram comparadas
antes (valores controle) e após o tratamento com L-NAME.

47
4.1.2.3. Teste de sensibilidade do controle barorreflexo.
A estimulação do barorreflexo foi realizada pela injeção intravenosa de doses
crescentes de substâncias vasoconstritoras (fenilefrina, agonista α-adrenérgico) e
substância vasodilatadora (nitroprussiato de sódio, doador de óxido nítrico), o que
produz aumento ou diminuição da PA respectivamente, que por sua vez aumenta ou
diminui a atividade dos barorreceptores arteriais e, reflexamente, induz alterações da
FC (bradicardia barorreflexa ou taquicardia barorreflexa). Para a avaliação do efeito
do -terpineol (4.8 mg/kg, i.v.) sobre o barorreflexo, foi realizado a estimulação do
barorreflexo com a administração de fenilefrina (8 μg/kg) e nitroprussiato de sódio
(25 μg /kg) antes e após o tratamento dos animais SHR e WKY com -terpineol.
A sensibilidade do barorreflexo foi avaliada relacionando-se as alterações
reflexas de FC induzidas por alterações transitórias da PAM. As mudanças da
frequência cardíaca produzida pela administração das drogas vasoativas foram
quantificadas e analisadas à razão dos valores de mudanças de frequência cardíaca
(FC) e pressão arterial média (PAM) (ΔFC/ΔPAM), conforme previamente descrito
por Braga et al. (2008).
4.2 Ensaios Farmacológicos in vitro.
4.2.1 Preparações de anéis de artéria mesentérica superior isolada de rato.
Os ratos normotensos e hipertensos foram eutanasiados. Em seguida, foi
retirada a artéria mesentérica superior por uma incisão no abdômen do animal, a
qual foi separada de tecidos conectivos e adiposos e então seccionada em anéis (1-
2 mm). Os anéis foram mantidos em cubas de 10 ml contendo solução de tyrode,
(pH=7,4) a 37 ºC e gaseificada com uma mistura 95% oxigênio e 5% gás carbônico.
Os anéis de artéria mesentérica superior foram suspensos por linhas de algodão, e
acopladas a um sistema de aquisição (Miobath-4, WPI, Sarasota-USA) para o
registro das contrações isométricas (Figura 9), ajustando-se uma tensão de 0,75 g, e
permanecendo por um período de 60 minutos de estabilização. Durante este período
o meio nutritivo era renovado a cada 15 minutos, para prevenir a interferência de
metabólitos (ALTURA; ALTURA, 1970).

48
Os anéis sem endotélio foram obtidos mecanicamente através do atrito entre
as paredes internas do vaso. Foram considerados anéis com endotélio, os anéis
com relaxamento superior a 80% após a aplicação de acetilcolina sobre a pré-
contração com FEN. Já os anéis com relaxamentos inferiores a 10 % foram
considerados sem endotélio. (FURCHGOTT; ZAWADZKI, 1980). Anéis com
relaxamento entre 10% e 80% foram descartados.
Figura 9: Fotografia do sistema de cubas de aquisição de dados de tensão isométrica para órgãos isolados.
4.2.2 Protocolos experimentais empregados nos estudos in vitro.
4.2.2.1 Anéis de artéria mesentérica superior de rato normotenso ou
espontaneamente hipertenso pré-contraídos com fenilefrina na presença ou
ausência de endotélio.
Após o período de estabilização, de 60 min, foi induzida uma contração com
fenilefrina (10 M) e a presença de endotélio foi então verificada através do nível de
relaxamento obtido pela adição de ACh (10 M). Após a verificação da presença ou
ausência de endotélio, foi obtida uma nova contração com FEN (10 M) e após a
estabilização tônica (aproximadamente 45 minutos) da contração concentrações
crescentes (10-12 a 10-5 M) de maneira cumulativa do -terpineol foram aplicadas em

49
anéis na presença ou ausência do endotélio (Figura 10). A percentagem de inibição
da contração foi mensurada pela comparação da resposta antes e após adição de -
terpineol.
O tempo necessário para que fossem obtidas as respostas máximas para
cada concentração de -terpineol variou entre 2 e 5 minutos. No final dos
experimentos, a reversão do relaxamento produzido por -terpineol foi conseguida
após 30 minutos de sua remoção das cubas, através da troca da solução de Tyrode
e verificação da resposta do tecido à FEN (10 μM). A reversibilidade foi
rotineiramente observada para assegurar que o relaxamento do tecido não foi
ocasionado por um possível dano tecidual.
Anéis com endotélio
Figura 10: Representação esquemática do protocolo experimental. Protocolo do
estudo do efeito de concentrações crescentes -terpineol (10-12 a 10-5 M) em anéis
de artéria mesentérica superior isolada de rato pré-contraídos com 10 M de FEN com endotélio. Quando necessário foram administrados inibidores durante 30
minutos, seguida de uma nova contração com FEN com adição do -terpineol. Ao final foi realizada a reversibilidade com uma nova contração de FEN.
4.2.2.2 Investigação do efeito do α- terpineol sobre o tônus intrínseco vascular
de anéis mesentéricos de ratos hipertensos e normotensos.
Com finalidade de avaliar o efeito do α-terpineol sobre o tônus muscular
espontâneo, foram realizados experimentos em anéis de artéria mesentérica de
ratos hipertensos e normotensos. Uma vez verificada a presença ou ausência do
endotélio vascular como descrito anteriormente, os anéis mesentéricos tiveram suas
Fen (10M)
ACh (10M)
Inibidores (30 min)
-terpineol
EE ((++))
?
1 h
Lav.
Fen (10M)
Estab.
Fen (10M)
Estab.

50
soluções nutritivas trocadas e após o período de estabilização do tônus vascular (30
min) concentrações crescentes de α-terpineol (10-12 a 10-5 M) foram adicionadas.
Após esse tratamento, avaliou-se um possível dano tecidual, portanto, lavagens
sucessivas com solução Tyrode foram feitas seguidas por um novo período de
estabilização (30 min). Na sequência, os anéis foram tratados com fenilefrina na
concentração de 10 μM para verificar a recuperação do órgão.
4.2.2.3 Verificação da influência da inibição da enzima sintase de NO sobre a
resposta vasorelaxante induzida por -terpineol em anéis de artéria
mesentérica isolada de rato normotenso e hipertenso.
Após a verificação da presença do endotélio conforme descrito anteriormente,
as preparações de anéis de artéria mesentérica superior de ratos foram incubadas
com L-NAME (100 M), um inibidor competitivo da enzima NO-sintase (MONCADA;
HIGGS, 1993) durante 30 minutos. Após este período, uma contração tônica com
fenilefrina (10 M) foi obtida e as concentrações crescentes e cumulativas de -
terpineol (10-12 a 10-5M) foram adicionadas. As respostas de -terpineol obtidas após
a adição das substâncias foram comparadas com as obtidas na ausência. Cada
protocolo experimental supracitado foi realizado em preparação específica.
4.2.2.4 Verificação da participação da via NO/GMPc na resposta vasorelaxante
induzida por -terpineol em anéis de artéria mesentérica isolada de rato
normotenso e hipertenso.
Preparações de anéis de artéria mesentérica superior isolada de rato
normotenso ou hipertenso, com endotélio, foram incubadas por 30 minutos com
ODQ (10 M), um inibidor da enzima ciclase de guanilil (GARTHWAITE et al., 1995;
KLOSS 2000) ou hidroxicobalamina (30M), um seqüestrador de óxido nítrico
(KRUSZYNA et al., 1998). Após este período, uma contração tônica com fenilefrina
(10 M) foi obtida e concentrações crescentes e cumulativas de -terpineol (10-12 a
10-5 M) foram adicionadas. A resposta de obtida após a adição deste inibidor foi
comparada com a resposta obtida na ausência desta substância.

51
4.2.2.5 Verificação da participação dos metabólitos da via da Ciclooxigenase
ou influência dos receptores muscarínicos na resposta vasorelaxante induzida
por -terpineol em anéis de artéria mesentérica superior isolada de rato
normotenso e hipertenso.
Conforme mencionado, após a verificação da integridade do endotélio, os
anéis de artéria mesentérica superior foram pré-incubados com indometacina 10 M,
inibidor da ciclooxigenase (CLARK; FUCHS, 1997), ou atropina (1 M) um
antagonista de receptores muscarínicos, por 30 minutos. Após este período, uma
contração tônica de fenilefrina (10 M) foi obtida e as concentrações crescentes e
cumulativas de -terpineol (10-12 a 10-5 M) foram adicionadas. A resposta de -
terpineol obtida após a adição do bloqueador foi comparada com aquela obtida na
sua ausência.
4.2.2.6 Verificação da participação de canais de K+ na resposta relaxante
induzida por -terpineol em anéis de artéria mesentérica superior isolada de
rato normotenso e hipertenso.
Após a verificação da integridade do endotélio, como descrito anteriormente,
a solução de Tyrode da cuba foi trocada pela solução despolarizante de Tyrode com
KCl a 20 mM (KCl 20 mM) e as preparações permaneceram nesta solução até o final
do experimento. Este procedimento produz alteração do efluxo de íons K+ e atenua
relaxamentos mediados por abertura de canais para K+ (CAMPBELL et al., 1996;
CLARK; FUCHS, 1997). Decorridos 30 min, foi induzida uma nova contração tônica
com FEN (10 M) e, em seguida, uma curva concentração-resposta para -terpineol
(10-12 a 10-5 M) foi obtida. A resposta obtida na presença de KCl (20 mM) foi
comparada com a resposta obtida na ausência do mesmo.
4.2.2.7 Identificação dos canais de potássio envolvidos na resposta relaxante
induzida por -terpineol em ratos normotensos e hipertensos.
Após a verificação da presença do endotélio, anteriormente as preparações
com endotélio foram incubadas separadamente com 1 mM de 4-AP, um bloqueador

52
seletivo de canais de K+ sensíveis a voltagem (KV) (LANGTON et al., 1991; LAGAUD
et al., 1999; BERG, 2002), 10 M de GLIB, um bloqueador seletivo de canais de K+
sensíveis ao ATP (KATP) (HUANG; KWOK, 1997; MOMBOULI; VANHOUTTE, 1997),
1 mM de TEA bloqueador dos canais de K+ (JACKSON, 2000), e o bloqueador
seletivo dos canais IKca e SKca (caribdotoxina associado com apamina, ambas na
concentração de 0.2μM). Após 30 min., foi induzida uma nova contração tônica com
FEN (10 M) e, em seguida, uma curva concentração-resposta para a -terpineol foi
obtida.
4.3 Ensaios bioquímicos realizados in vitro:
Estes experimentos foram realizados em colaboração com o grupo de
pesquisas da Prof. Dra. Lia Sumie Nakao do Laboratório De Neurobiologia do
Departamento de Patologia e Biologia Celular da Universidade Federal do Paraná,
em Curitiba, PR. E a colaboração da Prof. Dra. Valérie Bárbara Schini-Kert do
Laboratório de Farmacologia e Fisiopatologias Cardiovasculares, do Laboratório de
Biofotônica e Farmacologia, Faculdade de Farmácia, Universidade de Estrasburgo,
Estrasburgo, França.
4.3.1 Cultura celular
4.3.1.1 Células endoteliais imortalizadas de aorta de coelho (RAEC)
Nestes experimentos foram utilizadas células endoteliais imortalizadas de
aorta de coelho (RAEC) (BUONASSISI; VENTER, 1976), as quais foram mantidas
em incubadora com atmosfera umedecida, 5% CO2/ 90 % ar, 37 °C. O meio de
cultura foi o F12 suplementado com 10% de soro bovino fetal, 20 mM de HEPES e
antibiótico gentamicina (100 μg/mL). A confluência foi atingida entre as 48h que se
seguiam. Todos os experimentos foram realizados em culturas celulares
confluentes. As células foras expostas ao meio de cultura contendo 0,1% de soro
fetal bovino durante 6 horas antes do tratamento das células.

53
4.3.1.2 Cultura primária de células endoteliais de coronária de porco
As artérias coronárias de porco foram isoladas e os segmentos longos foram
lavados internamente com PBS sem cálcio, para remover o sangue remanescente.
Em seguida, as células endoteliais foram isoladas por meio do tratamento com
colagenase (tipo I, Worthington, 1 mg/ml) durante15 min a 37 °C) e cultivadas em
placas contendo meio MCDB 131 (Invitrogen) e 15% de soro fetal bovino
suplementado com penicilina, (100 U/ ml), estreptomicina (100 U/ml), fungizona (250
μg/ml), e L-glutamina (2 mM) (todos da Cambrex). A confluência foi atingida entre as
48 a 72 horas que se seguiam. Todos os experimentos foram realizados em culturas
celulares confluentes e de primeira passagem. As células foras expostas ao meio de
cultura contendo 0,1% de soro fetal bovino (QBiogene) durante 6 horas antes do
tratamento das células.
Todos os protocolos experimentais foram executados de acordo com Guide
for the care and use of laboratory animals publicado pelo U.S. National Institutes of
Health (NHI1996).
4.3.2 Determinação da produção do NO
4.3.2.1 Quantificação dos níveis de NO em células endoteliais de aorta de
coelho induzida pelo α-terpineol.
A produção de NO em células endoteliais de aorta de coelho induzida pelo α-
terpineol foi quantificado por fluorescência. O citomêtro de fluxo (marca B&D
FACSCALIBUR) foi usado para avaliar mudanças relativas nas concentrações
intracelulares de NO por monitoramento de fluorescência de DAF-2. Para isso foi
utilizado a sonda o DAF-2DA (diacetato 4,5-diaminofluoresceína,10-5M, Calbiochem)
que apresenta uma característica permeante a célula. DAF2-DA penetra nas células
endoteliais onde é clivado através de estearases plasmáticas para DAF-2 que é
retido então na célula e reage com o NO na presença de oxigênio. Esta reação
produz combinações fluorescentes emitidas em 488 nm até 515 nm e permitem a

54
quantificação da produção do óxido nítrico. Quantificação do NO foi determinada
com software convencional de análise em níveis de intensidade fluorescente em
proporção ao DAF2-DA ao qual aumenta a quantidade de NO liberado pelas células
vasculares no basal ou condições estimuladas.
4.3.2.2 Protocolos experimentais para quantificação da produção de óxido
nítrico induzida pelo α-terpineol em células endoteliais de aorta de coelho.
As amostras foram mantidas em cultura momentos antes do experimento.
Para o tratamento com α-terpineol, as amostras foram agrupadas e o DAF-2-DA foi
adicionado.
Para os protocolos experimentais foram formados 3 grupos, o primeiro grupo
foi realizado em condições não estimuladas (NO basal) com a emissão de
fluorescência do DAF-2 formado foi utilizada como controle. Em um segundo grupo
as amostras com emissão de fluorescência pelo DAF-2 formado na presença de 10-5
M ou 10-4 M acetilcolina ou bradicinina (10-4 M) (condição de estimulação de NO)
foram utilizadas como controle positivo. Em um terceiro grupo as amostras foram
analisadas pela emissão de fluorescência pelo DAF-2 após a pré-incubação com o
monoterpeno α-terpineol (após 30 min) em diferentes concentrações (10-6 M, 10-5 M,
10-4 M).
4.3.2.3 Avaliação da influência da inibição da enzima NO sintase na produção
de óxido nítrico induzida pelo α-terpineol em células endoteliais de aorta de
coelho.
Os protocolos experimentais foram formados em 4 grupos, onde o primeiro
grupo foi realizado em condições não estimuladas (NO basal) com a emissão de
fluorescência do DAF-2 foi utilizada como controle. No segundo grupo foi utilizada
acetilcolina na concentração de 10-5 M, no terceiro grupo a concentração de 10-5 M
de α-terpineol (após 30 min) e no quarto grupo foram realizados experimentos na
presença do inibidor da enzima NO sintase, L-NAME 100 μM, adicionado às
preparações 15 minutos antes da adição do α-terpineol.

55
4.3.2.4 Confirmação do efeito α-terpineol de produzir NO em células endoteliais
de artéria coronária de porco.
A produção de NO em células endoteliais de artéria coronária de porco
induzida pelo α-terpineol foi quantificado por fluorescência. Foram realizadas
análises rápidas e de alta sensibilidade utilizando a citometria para captura amostras
em placas com o citometro Celigo Cytometer da marca Cyntellect (San Diego –
EUA). As mudanças relativas nas concentrações intracelulares de NO foi
determinado por monitoramento de fluorescência de DAF-2 (emissão 488 nm até
515 nm). A avaliação dos níveis de NO foi determinada com software convencional
Cyntellect® para análise dos níveis de intensidade fluorescente.
4.3.2.5 Protocolos experimentais para quantificação da produção de óxido
nítrico induzida pelo α-terpineol em células endoteliais de artéria coronária de
porco.
Para os protocolos experimentais foram formados 4 grupos, o primeiro grupo
foi realizado em condições não estimuladas (NO basal) e a emissão de fluorescência
do DAF-2 foi utilizada como controle. Em um segundo grupo as amostras com
emissão de fluorescência pelo DAF-2 formado na presença de bradicinina 10-4 M
(condição de estimulação de NO) foi utilizada como controle positivo. Em um terceiro
grupo, as amostras foram analisadas pela emissão de fluorescência pelo DAF-2
após a pré-incubação com o monoterpeno α-terpineol (10-4 M) (após 30 min). No
quarto grupo foram realizados experimentos na presença do inibidor da enzima NO
sintase, L-NA 100 μM, adicionado as preparações 15 minutos antes da adição do α-
terpineol (10-4M).
4.3.3 Análises por western blotting
As fosforilações da eNOS, Akt e AMPK foram determinadas em cultura de
células endoteliais de coronária de porco através da técnica de western blotting,
exatamente como descrito por Anselm e colaboradores (2007).

56
Para determinar a fosforilação das proteínas em estudo, as células foram
previamente tratadas durante 30 minutos com PBS (controle negativo), ou com o -
terpineol (10-5 a 3x10-4 M). Após o tratamento, as células foram lavadas duas vezes
com o PBS e então lisadas com uma mistura contendo Tris/HCl 20 mM (pH 7.5;
QBiogene), NaCl 150 mM, Na3VO4 1 mM, fosfato de sódio 10 mM, NaF 20 mM,
ácido ocadáico 0.01 mM (Sigma), inibidor de protease (Roche) e 1% Triton X-100
(QBiogen). Alguns experimentos foram realizados para investigar o efeito das
diferentes concentrações e dos tempos de incubação sobre a fosforilação das
proteínas investigadas.
A quantificação de proteínas foi descrito por Bradford (1976) e o total de
proteínas usado por amostra foi 20 μg. As proteínas foram separadas em gel de
poliacrilamida SDS 8% (Sigma) a 70 V durante 2 horas. Em seguida foram
transferidas eletroforeticamente, a 100 V durante 120 minutos, para membranas
(difluoreto de polivinilidina da Amersham), as quais foram bloqueadas com meio
contendo 3 % de albumina sérica bovina, Tris (Biorad) e 0,1% de Tween-20 (Sigma)
(TBST) durante 1 hora. Para detecção das proteínas fosforiladas, as membranas
foram incubadas com os respectivos anticorpos primários (p-AMPK Tyr-172, p-Akt
Ser473 e p-eNOS Ser1177, Cell Signaling Technology; diluição de 1:1000), a 4 °C
durante 12h. Após a lavagem em PBS, as membranas foram incubadas com o
anticorpo secundário (anticorpo anti–rabbit IgG ligado à peroxidase, diluição de
1:10000; Cell Signaling Technology), em temperatura ambiente, durante 60 minutos.
Marcadores específicos (Invitrogen) foram utilizados para a determinação do peso
molecular e identificação das proteínas na membrana. As bandas imunorreativas
foram detectadas pelo aumento da quimioluminescência (Amersham).
Frequentemente uma solução de Ponceau foi utilizada para verificar a qualidade da
transferência das proteínas.

57
4.4 Análise Estatística
Os resultados são expressos como a média ± erro padrão da média de 3
experimentos (em cultura de células) ou 4 a 9 experimentos (com animais e artérias
isoladas). Os testes t de Student (não pareado) e análise de variância ANOVA de
uma ou duas vias, seguido de teste de Bonferronni. Os valores de p < 0,05 foram
considerados significativos em avaliar as diferenças entre as médias. Para avaliar o
efeito vasorelaxante induzido por -terpineol, o parâmetro do Emáx (efeito máximo
gerado pelo agonista) foi analisado de acordo com a diminuição da resposta
máxima. Para todos estes procedimentos foi utilizado o programa estatístico
GraphPad Prism versão 5.0.

58
Resultados

59
5. RESULTADOS
5.2 ESTUDOS in vivo
5.2.1 Efeito do α-terpineol sobre a pressão arterial média (PAM, mmHg) e
frequência cardíaca (FC, bpm) em ratos hipertensos (SHR) e normotensos
(WKY) não-anestesiados
Após o período de estabilização dos parâmetros cardiovasculares de ratos
normotensos não-anestesiados, os valores de pressão arterial média e frequência
cardíaca foram para PAM 105 ± 3 mmHg e FC 360 ± 3 bpm (n=10) e PAM de 185± 5
mmHg e FC de 380 ± 5 bpm para ratos SHR (n=11). α-Terpineol (1, 5, 10 and 20
mg/kg, i.v., administrado de maneira randômica) induziu hipotensão dependente de
dose em animais hipertensos SHR (-375, -577, -715, -844 mmHg, n=9) e
normotensos WKY: (-103, -399, -5211, -6212 mmHg, n=10) (Figure 11 A, B).
Este efeito hipotensor foi associado a uma taquicardia inicial, seguida de uma
bradicardia em ambos os grupos de animais.
Como observado nos valores de batimentos por minuto (bpm) de animais
normotensos, foi notado que o α-terpineol produziu uma taquicardia seguida de uma
bradicardia persistente evidente nas maiores doses de 10 e 20 mg/kg (WKY: tempo
inicial 0: 45±5, 64±11, 110±7, 113±22 bpm; tempo de 3 min: -3±5, -10±4, -73±4,
-125±2 bpm, n=10). Em animais hipertensos este efeito foi reproduzido, no entanto,
a dose de 5 mg/kg foi capaz de produzir a hipotensão e taquicardia com a
bradicardia secundária superior a 60 bpm (SHR: Tempo 0: 61±5, 75±9, 85±3, 72±8
bpm; Tempo 3 min: -33±12, -71±5, -126±16, -144±32 bpm, n=9; Figura 11 C, D).
O valor da DE50 α-terpineol foi de 4.8 mg/kg, este valor foi calculado de acordo
com a relação dose-efeito. Na figura 12 estão apresentados os registros
representativos do efeito do α-terpineol na dose de 4.8 mg/kg.

60
Figura 11: Efeitos do α-terpineol sobre (A e B) a pressão arterial média (PAM,
mmHg) e (C e D) frequência cardíaca (FC, bpm) em ratos normotensos (WKY) (n=10) e hipertensos (SHR) não-anestesiados (n=9). Os valores foram expressos
como média e.p.m.
SHR WKY
A B
C D

61
Figura 12: Registro representativo dos efeitos do α-terpineol (4.8 mg/kg) sobre a
pressão arterial média (PAM, mmHg) e frequência cardíaca (FC, bpm) em ratos (A)
normotensos (WKY) (n=10) e (B) hipertensos (SHR) (n=9).
A
B

62
5.2.2 Efeito do α-terpineol sobre a pressão arterial média (PAM, mmHg) e
frequência cardíaca (FC, bpm) em ratos hipertensos (SHR) e normotensos
(WKY) não-anestesiados
Nas figuras 13 A e B estão representados os valores em porcentagem de
delta (Δ) da PAM (mmHg) e FC (bpm) de ratos SHR e WKY tratados com α-
terpineol. Foi demonstrado que o efeito hipotensor induzido pelo monoterpeno foi
superior em animais hipertensos SHR em comparação com os animais normotensos
WKY, no entanto as respostas taquicárdicas e bradicárdicas não foram alteradas.
Observou-se, ainda, que o α-terpineol produziu respostas hipotensoras
superior sobre o efeito da PA sistólica em comparaç ão ao efeito observado com a
diastólica em animais hipertensos SHR. No entanto, os efeitos não foram diferentes
em animais normotensos WKY (Figura 14).

63
Figura 13: Efeitos do α-terpineol sobre (a) a pressão arterial média (% de PAM,
mmHg) e (b) frequência cardíaca (% de FC, bpm) em ratos normotensos (WKY) (n=10) e hipertensos (SHR) não-anestesiados (n=9). Os valores foram expressos
como média e.p.m.
A
B C

64
Figura 14: Efeitos do α-terpineol sobre (a) a pressão arterial sistólica em ratos
normotensos (WKY) (n=10) e hipertensos (SHR) não-anestesiados (n=9). Os valores
foram expressos como média e.p.m.
A
B

65
5.2.3 Efeito do α-terpineol sobre o controle autonômico de ratos não-
anestesiados normotensos e hipertensos.
5.1.3.1 Avaliação do bloqueio com atropina na resposta do α-terpineol.
Observou-se que α-terpineol exibe ações sobre o controle autonômico,
passamos a investigar inicialmente sobre o bloqueio parassimpático com atropina (2
mg ⁄ kg; i.v.) e foi notado que a resposta hipotensiva induzida por α-terpineol ED50:
4.8 mg ⁄ kg; i.v. em ambos os animais hipertensos SHR (valor de ΔPAM antes da
atropina -627 mmHg, n=6 e depois ΔPAM= -619 mmHg e normotensos WKY
(valor de ΔPAM antes da atropina -515 mmHg e depois ΔPAM= -546 mmHg, n=6)
não foi alterada (Figure 15 A e B).
Em contraste as respostas induzidas pelo α-terpineol foram significantemente
reduzidas após o pré-tratamento com atropina. Verificou-se que a taquicardia foi
diminuída de maneira significativa nos animais SHR [ΔFC antes da atropina (Tempo
0)= 89±5 bpm versus ΔFC depois (Tempo 0)= 60±4 bpm] e normotensos WKY [ΔFC
antes da atropina (Tempo 0)= 65±11 bpm; ΔFC depois (Tempo 0)= 59±3 bpm]
(figura 15 C e D).
Associado a este efeito exercido pela atropina, foi observado que o efeito
bradicárdico secundário decorrente do tratamento com α-terpineol foi fortemente
reduzido, especialmente em animais hipertensos [SHR: ΔFC antes da atropina
(Tempo 3 min.) = -125±6 bpm, n=5; ΔFC depois (Tempo 3 min.)= -10±4 bpm, n=6;
em comparação com os animais WKY [ ΔFC antes da atropina (Tempo 3) min. -11±4
bpm, n=5; ΔFC depois (Tempo 3 min.) -2±2 bpm, n=6] (figura 15 C e D)

66
Figura 15: Efeitos do α-terpineol sobre (a) a pressão arterial média (PAM, mmHg) e (b) frequência cardíaca (FC, bpm) em ratos normotensos (WKY) e hipertensos (SHR) não-anestesiados (n=6) antes e após o tratamento com atropina. Os valores
foram expressos como média e.p.m. * p < 0,05 em relação a ausência de tratamento (ANOVA de uma via seguida pelo teste de Bonferroni).
WKY SHR A B
C D

67
5.1.3.2 Avaliação da resposta ao tratamento intravenoso com α-terpineol após
o bloqueio simpático com atenolol ou hexametônio em ratos SHR ou WKY.
Nas figuras 16 e 17 estão representados os valores de delta (Δ) da PAM
(mmHg) e FC (bpm) de ratos SHR e WKY tratados com hexametônio ou atenolol. Foi
demonstrado que o bloqueio com hexametônio (30 mg ⁄ kg; i.v.) (Figura 16) ou
atenolol (20 mg ⁄ kg; i.v.) (Figura 17) não alterou a resposta hipotensiva induzida por
α-terpineol ED50: 4.8 mg ⁄ kg; i.v. em animais SHR ou WKY.
Isto foi observado nos valores de ΔPAM para SHR (valor de ΔPAM antes de
hexametônio= -656 mmHg e ΔPAM depois = -615 mmHg, n=6 ou para atenolol
ΔPAM antes = -643 mmHg e ΔPAM depois = -622 mmHg, n=6), bem como para
os animais WKY (valor de ΔPAM antes de hexametônio= -543 mmHg e ΔPAM
depois = -5110 mmHg, n=6 ou para atenolol ΔPAM antes= -535 mmHg, n=5 e
ΔPAM depois = -678 mmHg) (Figure 16 e 17 A e B).
Constatou-se que as respostas taquicádica e bradicárdica induzidas pelo α-
terpineol foram significantemente reduzidas quando os animais hipertensos ou WKY
foram tratados com hexametônio ou atenolol. Verificou-se que a taquicardia foi
diminuída de maneira significativa nos animais SHR tratados com hexametônio [ΔFC
antes de hexametônio (Tempo 0)= 88±4 bpm; ΔFC depois (Tempo 0) =5±1 bpm] ou
atenolol [ΔFC antes de atenolol (Tempo 0)= 77±6 bpm; ΔFC depois (Tempo 0)=
45±7 bpm], bem como a redução foi observada em animais WKY tratados com
hexametônio [ΔFC antes de hexametônio (Tempo 0)= 74±6 bpm; ΔFC depois
(Tempo 0) =0±0 bpm] ou atenolol [ΔFC antes de atenolol (Tempo 0)= 73±6 bpm;
ΔFC depois (Tempo 0)= 42±6 bpm].
De maneira semelhante, a resposta bradicárdica foi reduzida em animais SHR
[ΔFC antes de hexametônio (Tempo 3)= -120±34 bpm; ΔFC depois (Tempo 3)= -22±
10 bpm] ou atenolol [ΔFC antes de atenolol (Tempo 3)= -145±10 bpm; ΔFC depois
(Tempo 3)= -73 ± 22 bpm], bem como a redução foi observada em animais WKY
tratados com hexametônio [ΔFC antes de hexametônio (Tempo 3)= -10±3 bpm; ΔFC
depois (Tempo 3) =0±0 bpm] ou atenolol [ΔFC antes de atenolol (Tempo 3)= -26±7
bpm; ΔFC depois (Tempo 3)= -16±8 bpm].

68
Figura 16: Efeitos do α-terpineol sobre (a) a pressão arterial média (PAM, mmHg) e (b) frequência cardíaca (FC, bpm) em ratos normotensos (WKY) e hipertensos (SHR) não-anestesiados (n=6) antes e após o tratamento com hexametônio. Os
valores foram expressos como média e.p.m. * p < 0,05 em relação a ausência de tratamento (ANOVA de uma via seguida pelo teste de Bonferroni).
WKY SHR A B
C D

69
Figura 17: Efeitos do α-terpineol sobre (a) a pressão arterial média (PAM, mmHg) e (b) frequência cardíaca (FC, bpm) em ratos normotensos (WKY) e hipertensos (SHR) não-anestesiados (n=6). antes e após o tratamento com atenolol. Os valores
foram expressos como média e.p.m. * p < 0,05 em relação a ausência de tratamento (ANOVA de uma via seguida pelo teste de Bonferroni).
WKY SHR A B
C D

70
5.1.3.3 Efeito do α-terpineol após o bloqueio simpático periférico com prazosin em ratos SHR ou WKY.
A administração de prazosin (1 mg/kg, i.v), antagonista dos receptores α1,
não induziu alterações nas respostas hipotensoras induzidas pelo α-terpineol (ED50:
4.8 mg ⁄ kg; i.v.) em animais SHR ou WKY. Estes dados são apresentados nos
gráficos presentes na figura 15: Confirmados pelos valores em animais SHR [ΔPAM
antes= -677 e ΔPAM depois= -656 mmHg, n=6] e normotensos WKY [ΔPAM
antes= -594 mmHg, n=5 e ΔPAM depois = 569 mmHg] (Figura 18 A e B)
Associado a este efeito, prazosin não exerceu mudanças sobre os efeitos
taquicárdicos em animais hipertensos [SHR: ΔFC antes de prazosin (Tempo 0 min) =
77±6 bpm, n=5; ΔFC depois (Tempo 0 min.)= 85±7 bpm, n=5; em comparação com
os animais WKY [ ΔFC antes de prazosin (Tempo 0 min.)=73±3 bpm, n=5; ΔFC
depois (Tempo 0 min.)= 78±8 bpm, n=5]. De maneira semelhante, não alterou efeitos
os bradicárdicos tardios em SHR (Tempo 3 min.) = -143±10 bpm, n=5; ΔFC depois
(Tempo 3 min.)= -173±12 bpm, n=5; em comparação com os animais WKY [ ΔFC
antes da atropina (Tempo 3) min. -11±4 bpm, n=5; ΔFC depois (Tempo 3 min.) -36±3
-2±2 bpm, n=5] (Figura 18 C e D).

71
Figura 18: Efeitos do α-terpineol sobre (a) a pressão arterial média (PAM, mmHg) e (b) frequência cardíaca (FC, bpm) em ratos normotensos (WKY) e hipertensos (SHR) não-anestesiados (n=5). antes e após o tratamento com prazosin. Os valores
foram expressos como média e.p.m. * p < 0,05 em relação a ausência de tratamento (ANOVA de uma via seguida pelo teste de Bonferroni).
SHR WKY A B
C D

72
5.1.4 Investigação da enzima sintase de óxido nítrico (NOS) no efeito
cardiovascular induzido por -terpineol em ratos hipertensos não-
anestesiados.
Realizaram-se os experimentos in vivo que procuravam verificar a
participação da enzima NOS. Constatou-se que a resposta hipotensiva induzida pelo
α-terpineol (4.8 mg ⁄ kg; i.v.) foi atenuada após o bloqueio agudo da NOS com L-
NAME (20 mg/Kg) em animais hipertensos SHR [ΔPAM antes de L-NAME= -675
mmHg, n=8 e ΔPAM depois SHR: -351 mmHg, n=7] e seus controles normotensos
[ΔPAM antes=-499 mmHg, n=5 e ΔPAM depois= -292 mmHg, n=7] (Figura 19 A e
B).
A frequência cardíaca também foi atenuada de maneira significativa após o
tratamento com α-terpineol na dose de 4.8 mg ⁄ kg; i.v. demonstrando a importância
da ativação da NOS para α-terpineol exercer seus efeitos sistêmicos (figura 16 C e
D) tanto em animais hipertensos [SHR: ΔFC antes de L-NAME (Tempo 0 min.) =
78±8 bpm, n=5; ΔFC depois (Tempo 0 min.)= 45±8 bpm, n=7]. O mesmo foi
observado para os animais WKY [ ΔFC antes de L-NAME (Tempo 0 min.)= 64±11
bpm, n=5; ΔFC depois (Tempo 0 min.)= 45±7 bpm, n=7].
A resposta bradicárdica após 3 minutos de administração deste monoterpeno
foi reduzida apenas em animais hipertensos [SHR: ΔFC antes de L-NAME (Tempo
3) = -163±21 bpm, n=7 ΔFC depois (Tempo 3) = -87±22 bpm, n=7]. O tratamento
com L-NAME não alterou os efeitos bradicárdicos induzidos por α-terpineol em WKY
[ ΔFC antes de L-NAME (Tempo 3) min. -33±4 bpm, n=7; ΔFC depois (Tempo 3
min.) -37±22 bpm, n=5] (figura 19 C e D).

73
Figura 19: Efeitos do α-terpineol sobre (a) a pressão arterial média (PAM, mmHg) e (b) frequência cardíaca (FC, bpm) em ratos normotensos (WKY) e hipertensos (SHR) não-anestesiados (n=7). antes e após o tratamento com L-NAME. Os valores
foram expressos como média e.p.m. * p < 0,05 em relação a ausência de tratamento (ANOVA de uma via seguida pelo teste de Bonferroni).
SHR WKY A B
C D

74
5.1.5 Avaliação do efeito da infusão intravenosa de α-terpineol sobre as
respostas cardiovasculares à estimulação do barorreflexo
Neste protocolo experimental, avaliamos a influência do α-terpineol (4.8
mg/kg, i.v.) sobre as respostas cardiovasculares desencadeadas pela estimulação
do barorreflexo, como mostrado na figura 20.
Os ratos SHR tratados apenas com veículo apresentaram uma redução do
ganho do barorreflexo quando comparados ao grupo WKY controle tratados com
veículo (−0.86±0.07 vs. −2.51±0.2 bpm mm Hg−1, p<0.05). Entretanto, a
administração aguda de α-terpineol (4.8 mg/Kg, i.v.) foi capaz de restaurar a
sensibilidade do barorreflexo em ratos hipertensos SHR (SHR (veículo) −0.86±0.07
vs. SHR (α-terpineol) −1.5±0.08 bpm mm Hg−1, p<0.05, n=4). Estes dados
demonstram ainda que o α-terpineol melhora o ganho do barorreflexo, no entanto,
sem alterar a sensibilidade do barorreflexo dos animais WKY quando tratado com α-
terpineol (−2.23±0.2 mm Hg−1, P >0.05, n=4) (Figura 20)

75
Figura 20: Efeitos do α-terpineol sobre a sensibilidade do barorreflexo (bpmmmHg-1) em ratos normotensos (WKY) e hipertensos (SHR) não-anestesiados (n=4). Os
valores foram expressos como média e.p.m. *p< 0,05 em relação ao controle WKY, p< 0,05 entre os grupos SHR (ANOVA de uma via seguida pelo teste de Bonferroni).

76
5.2 ESTUDOS in vitro
5.2.1 Efeito do α-terpineol sobre as contrações induzidas por FEN em anéis de
artéria mesentérica superior isolada de ratos
A administração cumulativa de -terpineol (10-12 a 10-5M) induziu um
vasorrelaxamento dependente de concentração em anéis, pré-contraídos com FEN
(10 μM), com endotélio de artéria mesentérica superior de ratos hipertensos SHR
[Emáx = 53,7 ± 3, n=9] e seus controles normotensos WKY [Emáx = 60 4, n=9]. A
remoção do endotélio vascular inibiu a resposta vasorelaxante induzida pelo -
terpineol, com uma diminuição da porcentagem de relaxamento máximo (Emáx) em
ratos hipertensos [Emáx = 16,1 ± 3, p<0,05, n=8] e controles WKY [Emáx = 20,5 ± 1,
p<0,05, n=8] (figura 21; tabela 1).
Figura 21: -Terpineol induz relaxamento em anéis de artéria mesentérica de ratos
hipertensos SHR e controles WKY. Atividade vasorelaxante do -terpineol (10-12 a 10-5M) em anéis isolados de arteria mesentérica de rato SHR e WKY pré-contraídos
com fenilefrina. () Rato normotenso WKY com endotélio; () Rato normotenso WKY sem endotélio; () Rato hipertenso SHR com endotélio; () Rato hipertenso
SHR sem endotélio. Os resultados correspondem à média ± e.p.m. * p < 0,05; em
comparação aos respectivos controles (ANOVA de uma via e pós teste de Bonferroni).

77
5.2.2 Efeito do α-terpineol sobre o tônus intrínseco vascular de anéis
mesentéricos de ratos espontaneamente hipertensos e seus controles
normotensos.
A administração cumulativa de α-terpineol (10-12 - 10-5 M) não promoveu
efeito sobre o tônus muscular espontâneo em preparações de anéis com endotélio
funcional intacto ou sem endotélio em ratos espontaneamente hipertensos (SHR) e
seus controles normotensos (WKY).
A reversibilidade foi observada para assegurar que o α-terpineol não
ocasionou dano tecidual, demonstrado no registro original da ação do α-terpineol
sobre a artéria mesentérica (figura 22 A, B; figura 23).
Figura 22: Registro original da ação do α-terpineol (10-12 - 10-5 M) em anéis de artéria mesentérica superior isolada de rato (A) SHR ou (B) WKY, com o endotélio intacto, no tônus basal. As setas indicam o momento da adição do α-terpineol.
A
B

78
Figura 23: Efeito do α-terpineol sobre o tônus basal de anéis de artéria mesentérica
superior isolada de rato. () Rato normotenso WKY com endotélio; () Rato normotenso WKY sem endotélio; () Rato hipertenso SHR com endotélio; () Rato hipertenso SHR sem endotélio. Os resultados correspondem à média ± e.p.m. (n=4).

79
5.2.3. Participação da via L-arginina/NO/ GMPc na resposta vasorelaxante
induzida pelo -terpineol em anéis de artéria mesentérica isolada de rato
normotenso e hipertenso.
As respostas vasorelaxantes induzidas por concentrações crescentes de α-
terpineol (10-12 – 10-5M) foram significativamente atenuadas com diminuição de suas
respostas máximas na presença de fenilefrina 10 μM após o pré-tratamento L-
NAME (100 μM), um antagonista competitivo da NOS, em animais WKY [Emáx = 18,1
± 3,8] ou SHR [Emáx = 20,1± 3, *p < 0,05, n=8] (figura 24, tabela 1)
Em sequência, as respostas induzidas pelo α-terpineol (10-12 – 10-5M) foram
abolidas anéis de artéria mesentérica com endotélio de animais hipertensos pré-
incubados com hidroxicobalamina 30 μM, seqüestrador de NO ou de ODQ (10 μM),
um inibidor seletivo da ciclase de guanilil solúvel, SHR [Emáx = 17,3 ± 3; 18,1 ± 3, *p
< 0,05, n=8, respectivamente]. Esta resposta vasorelaxante reduzida foi semelhante
ao observado em animais WKY [Emáx = 23,5 ± 7; 20,8 ± 1 *p < 0,05, n=8,
respectivamente] (figura 25, tabela 1).
Tabela 1 Porcentagem de inibição da resposta máxima e contração com FEN (10
μM) para estudos com anéis de artéria mesentérica superior isolada de rato.
Condição experimental
% de Resposta máxima n
WKY SHR
Endotélio presente 60 4 53,7 ± 3 9
Sem endotélio 20,5 1* 16,1 ± 3* 8
L- NAME 100 M 18,1 ±3.8* 20,1± 3 * 8
Hidroxicobalamina 30 M 23,5 ± 7* 17,3 ± 3* 8
ODQ 10 M 20,8 ± 1* 18,1 ± 3* 8
Dados apresentados como médian ± e.p.m. *p < 0.05 quando comparados com preparações com endotélio presente.

80
Figura 24: α-Terpineol induz relaxamento vascular dependente do endotélio envolve a participação da enzima eNOS. Atividade vasorelaxante em anéis de artéria
mesentérica com endotélio funcional, pré-contraídos com FEN (10 M), na presença e na ausência de ()LNAME (100 μM) tratadas com α-terpineol (10-12 – 10-5M)
(n=8); (A) WKY e (B) SHR. * p <0,05

81
Figura 25: α-Terpineol promove efeito vasorelaxante via óxido nítrico/GMPc. Atividade vasorelaxante em anéis de artéria mesentérica com endotélio funcional,
pré-contraídos com FEN (10 M), na presença e na ausência de ()HDX 30 μM (n = 8) ou ()ODQ 10 μM (n = 8) tratadas com α-terpineol (10-12 – 10-5M). (A) WKY e (B)
SHR. * p <0,05

82
5.2.4 Verificação da participação dos metabólitos da via da Ciclooxigenase ou
influência dos receptores muscarínicos (M3) sobre a resposta vasorelaxante
induzida por -terpineol em anéis de artéria mesentérica superior isolada de
rato hipertenso SHR e normotenso WKY
O pré-tratamento com indomenetacina 10 μM, inibidor não seletivo da enzima
ciclooxigenase, em anéis de artéria mesentérica superior com endotélio intacto e
pré-contraídos com FEN (10 M) isolados de animais hipertensos [Emáx = 53,1 ± 4]
ou normotensos [Emáx =61,1 ± 5] não foi alterou o vasorrelaxamento induzido por
concentrações crescentes de -terpineol (10-12 – 10-5M).
Nos experimentos que investigaram a participação do endotélio e o
envolvimento dos receptores muscarínicos M3, na presença de atropina 1M,
antagonista não seletivo dos receptores muscarínicos, os efeitos vasorelaxantes
produzidos pelo tratamento com -terpineol (10-12 – 10-5M) não foram alteradas
significativamente em anéis de artéria mesentérica superior de rato SHR [Emáx =41,5
± 2] ou WKY [Emáx =53,3 ± 8, *p < 0,05, n=8], respectivamente (Figura 26, Tabela 2).
Tabela 2 Porcentagem de inibição da resposta máxima e contração com FEN
(10μM) para estudos com anéis de artéria mesentérica superior isolada de rato.
Condição experimental
% de Resposta máxima n
WKY SHR
Endotélio presente 60 4 53,7 ± 3 9
Sem endotélio 20,5 1* 16,1 ± 3* 8
Indometacina 10 M 61,1 ± 5 53,1 ± 4 8
Atropina 1 M 53,3 ± 8 41,5 ± 2 8
Dados apresentados como médian ± e.p.m. *p < 0.05 quando comparados com preparações com endotélio presente.

83
Figura 26: Metabólitos da ciclooxigenase ou receptores muscarínicos não estão
envolvidos na resposta vasorelaxante induzida pelo de -terpineol. Concentrações
crescentes de -terpineol (10-12 – 10-5M) em anéis com endotélio funcional de artéria
mesentérica superior isolada de rato, pré-contraídos com FEN (10 M), na ausência
(n = 9) e na presença de indometacina 10 μM (n = 8) () ou atropina1 ηM (n = 8)
(),(A) WKY e (B) SHR; * p <0,05.

84
5.2.5 Participação dos canais de potássio responsáveis pelo fator
hiperpolarizante derivado do endotélio (EDHF) no efeito vasorelaxante
induzido pelo α-terpineol em ratos SHR e WKY
Para a investigação sobre a participação do EDHF os anéis de artéria
mesentérica. Foram incubados em preparações de caribdotoxina mais apamina (0,2
μM). Observou-se que o relaxamento vascular induzido pelo -terpineol (10-12 – 10-5
M) foi alterado após incubação destes inibidores em animais SHR [Emáx = 29,5 ± 2]
ou WKY e [Emáx= 39,5 ± 3, *p < 0,05, n=8] respectivamente (figura 27, Tabela 3).
Figura 27: Caracterização da participação do EDHF no efeito vasorrelaxante induzido pelo α-terpineol (10-12 – 10-5M) em anéis com endotélio funcional de artéria
mesentérica superior isolada de rato SHR () e WKY, () pré-contraídos com FEN
(10 M), na ausência (n = 8) e na presença de caribdotoxina + apamina 0.2 μM (n = 6) [SHR () ou WKY ()]; * p <0,05.

85
5.2.6 Identificação dos canais de potássios envolvidos na resposta relaxante
induzida por -terpineol em anéis de artéria mesentérica superior isolada de
rato hipertenso e normotenso
5.2.6.1 Participação dos canais de potássio na resposta vasorelaxante induzida
por -terpineol
Na investigação para identificar qual canal de K+ estaria envolvido nos efeitos
vasculares induzidos pelo -terpineol (10-12 – 10-5 M) foi observado que em
preparações na contendo alta concentração de potássio (KCl 20mM) ou na
presença de tetraetilamônio (TEA; bloqueador não seletivo de canais de potássio (1
mM) reduziu o efeito vasorelaxante induzido pelo monoterpeno tanto em animais
hipertensos [Emáx = 36,4± 6; 38,5± 4, *p < 0,05, n=6] quanto normotensos [Emáx= 23±
4; 37,5± 4, *p < 0,05, n=6], respectivamente (figura 28, tabela 3).
É importante salientar que não foram observadas alterações significantes na
contração dos anéis de artéria mesentérica em resposta à fenilefrina após a
incubação dos bloqueadores de canais de K+ utilizados.

86
Figura 28: Efeito inibitório dos bloqueadores de canais de potássio no relaxamento
vascular induzido pelo α-terpineol em SHR e WKY. O relaxamento produzido pelo α-
terpineol (10-12 – 10-5M) foi testado na ausência e presença de KCl 20mM (modulador do efluxo de potássio) () ou tetraetilamônio (TEA, bloqueador não seletivo de canais de potássio) ()em anéis com endotélio funcional de artéria mesentérica superior isolada de rato SHR (B) ou WKY (A), pré-contraídos com FEN
(10 M), * p < 0,05;.

87
5.2.6.2 Avaliação dos canais de potássio sensíveis a ATP (KATP) e dependentes
de voltagem (KV) em anéis de artéria mesentérica isolada de rato hipertenso e
normotenso tratados com -terpineol.
Em anéis de artéria mesentérica com endotélio funcional na presença de 10
M de GLIB (um bloqueador dos canais KATP) ou na presença de 1 mM de 4-AP
(bloqueador dos canais Kv) foi observado que as curvas concentração-resposta para
-terpineol (10-12 – 10-5M) foram significantemente atenuadas Estes dados
apresentaram um deslocamento das curvas para a direita e diminuição de seus
efeitos máximos em animais SHR [Emáx = 24,2± 3; 42,5 ± 2, *p < 0,05, n=6] ou em
ratos normotensos WKY [Emáx= 33± 3; 38,7± 1, *p < 0,05, n=6] (figura 29, tabela 3).
Tabela 3 Porcentagem de inibição da resposta máxima e contração com FEN (10
μM) para estudos com anéis de artéria mesentérica superior isolada de rato.
Condição experimental % de Resposta máxima N
WKY SHR
Endotélio presente 60 4 53,7 ± 3 9
KCl 20mM 23± 4* 36,4± 6* 8
TEA 1mM 37,5± 4* 38,5± 4* 6
Caribdotoxina + apamina 0.2M 39,5 ± 3* 29,5 ± 2* 6
Glibenclamida 30 M 33± 3* 24,2± 3* 6
4 AP 1mM 38,7± 1* 42,5 ± 2* 6
Dados apresentados como médian ± e.p.m. *p < 0.05 quando comparados com preparações com endotélio presente TEA, Tetraetilamônio; 4-AP, 4-Aminopiridina.

88
Figura 29: Identificação dos canais de potássio que participam do relaxamento
vascular induzido pelo α-terpineol em SHR e WKY. O relaxamento produzido pelo α-
terpineol (10-12 – 10-5M) foi testado na ausência e presença de glibenclamida (10μM)
(bloqueador do KATP) () ou 4-aminopiridina (4-AP, bloqueador de KV) ()em anéis com endotélio funcional de artéria mesentérica superior isolada de rato SHR (B) ou
WKY (A), pré-contraídos com FEN (10 M), * p < 0,05;

89
5.4 ENSAIOS BIOQUÍMICOS
5.3.1 Determinação da produção do NO
5.3.1.1 Produção de óxido nítrico induzida por bradicinina e acetilcolina.
Neste experimento, uma cultura de linhagem imortalizada de células
endoteliais de aorta de coelho foi utilizada para investigar a produção de óxido
nítrico induzida por bradicinina 10-4M, acetilcolina 10-4M e 10-5M. Estes experimentos
foram utilizados como controle positivo das análises subsequentes.
Os valores de indução da produção de NO estão expressos em % de
fluorescência produzida pela reação para detecção de NO por DAF em células
endoteliais de aorta de coelho. Neste experimento foi observado que a acetilcolina e
bradicinina foram capazes de aumentar os níveis de NO (Figura 30).

90
A
B
Figura 30: Acetilcolina e bradicinina induzem aumento nos níveis de NO em cultura de células endoteliais de aorta de coelho. (A) Registro representativo da produção de NO induzida por bradicinina, acetilcolina (10-4 e 10-5 M) em cultura de células endoteliais de aorta de coelho (B) Gráfico representativo da produção de NO induzida por bradicinina, acetilcolina (10-4 and 10-5 M) em cultura de células endoteliais de aorta de coelho (n=3).

91
5.3.1.2 Quantificação dos níveis de NO em células endoteliais de aorta de
coelho induzida pelo α-terpineol
Nos experimentos que buscaram investigar os aumentos dos níveis de NO
utilizamos, inicialmente, células endoteliais de aorta de coelho e avaliamos em
condições controle de produção de NO em células endoteliais de aorta de coelho.
Realizamos experimentos na presença de acetilcolina 10-5M e diferentes
concentrações de -terpineol (10-6 M, 10-5 M, 10-4 M) foram quantificados por
fluorescência. A figura 31 A e B mostra o deslocamento da fluorescência após o
tratamento com acetilcolina e -terpineol em relação à população de células em
relação a unidades relativas de DAF-2 (Figura 31).
O gráfico apresentado na figura 32 representa os dados da produção de NO
determinado pela % em Δ da fluorescência de DAF detectada em células endoteliais
de aorta de coelho.

92
A
B
Figura 31: -Terpineol aumenta os níveis de NO em células endoteliais. (A) Registros representativos do aumento da intensidade de fluorescência de DAF-2 decorrente da produção de NO induzida por α-terpineol (10-6 ) ou ACh (10-5M e (B) por α-terpineol (10-6 e 10-4 M) em cultura de células endoteliais de aorta de coelho. (C) Gráfico representativo da produção de NO induzida por acetilcolina (10-5 M) ou α-terpineol (10-6 e10-4 M) em cultura de células endoteliais de aorta de coelho.

93
Figura 32: -Terpineol aumenta os níveis de NO em células endoteliais. Gráfico dos dados que expressam a produção de NO induzida por acetilcolina (10-5 M) ou α-terpineol (10-6 - 10-4 M) em cultura de células endoteliais de aorta de coelho (n=3).

94
5.3.1.3 Avaliação da influência da inibição da enzima NO sintase na produção
de óxido nítrico induzida pelo α-terpineol em células endoteliais de aorta de
coelho.
O -terpineol (10-6 M, 10-5 M, 10-4 M), incubado durante 30 minutos, foi capaz
de aumentar significativamente os níveis da produção de NO. Associado a este
efeito observamos que a presença do L-NAME (100 μM; inibidor da enzima eNOS)
foi capaz de reverter esta indução da produção de NO pelo -terpineol em cultura de
células endoteliais de aorta de coelho (Figura 34 A e B).
Na Figura 33 apresenta os dados representativos da intensidade de
fluorescência induzida pelo -terpineol (10-5 M) e o pré-tratamento com L-NAME.
Figura 33: A enzima eNOS está envolvida na produção de NO induzida pelo -Terpineol. Registros representativos do aumento da intensidade de fluorescência de DAF-2 decorrente da produção de NO induzida por α-terpineol (10-5 M) na presença
ou ausência de L-NAME (100 μM) em cultura de células endoteliais de aorta de
coelho.

95
A
B
Figura 34: A enzima eNOS está envolvida na produção de NO induzida pelo -Terpineol. (A e B) Gráficos da produção de NO em cultura de células endoteliais de aorta de coelho tratados por α-terpineol (10-5 M) ou L-NAME + α-terpineol em diferentes concentrações (n=3).

96
5.3.2 Análise por western blot
5.3.2.1 Efeito da insulina na fosforilação da eNOS (Ser 1177) e AKT (Ser 473)
Em nossos experimentos, com células endoteliais de artéria coronária de
porco, utilizou-se a insulina como controle positivo das fosforilação para eNOS e
AKT. Inicialmente, foi observado que a insulina induziu um forte aumento nos
primeiros 5 minutos da fosforilação da eNOS em Ser1177 quando comparado com o
controle. Adicional a estes dados foi observado o aumento da intensidade de
fosforilação em 30 minutos que se manteve durante o tempo avaliado de 180 min
(Figura 35)
Na sequência de experimentos, a exposição das células endoteliais a insulina
produziu fosforilação da eNOS e da AKT (ser 473) de maneira concentração
dependente (10-8 M, 3x10-8, 10-7, 3x10-7, 10-6), onde foram observadas maiores
níveis de fosforilações para as células que foram tratadas com as concentrações de
insulina de 10-6 M e 3x 10-7 M durante 30 minutos (Figura 35)
Figure 35. Análises representativas do efeito da insulina em cultura primária de células endoteliais de coronária de porco. Insulina causou fosforilação da eNOS em Ser 1177 dependente do tempo (A) e fosforilação da eNOS em Ser 1177 e AKT Ser 473 dependente da dose.

97
5.3.2.2 Efeito do tratamento com α-terpineol sobre a fosforilação da eNOS em
Ser 1177 de células endoteliais de artéria coronária de porco
A exposição das células endoteliais ao α-terpineol nas concentrações iniciais
de 10-4 M e 3x10-4 M causou a fosforilação intensa da eNOS desde os primeiros
minutos de exposição ao monoterpeno (Figura 36) Estes níveis de fosforilação
aumentaram de acordo com o tempo e se mantiveram estáveis durante os 60
minutos subseqüentes. Avaliamos como controle a expressão da eNOS total.
Figura 36: α-terpineol induz fosforilação da eNOS. (A) Análises representativas do
efeito de α-terpineol (10-4M e 3x10-4M) em cultura primária de células endoteliais de
coronária de porco. α-terpineol induz fosforilação da eNOS em Ser1177 e não altera
a eNOS total. Os resultados são mostrados como a média ± e.p.m. de 3 experimentos. * p < 0,05 em relação ao controle representado pelo tempo ―0‖ (ANOVA de uma via seguida pelo teste de Bonferroni).
A
B C

98
5.3.2.3 Efeito sobre a fosforilação da AKT em Ser 473 de células endoteliais de
artéria coronária de porco induzida pelo α-terpineol.
Para melhor compreender a via de sinalização endotelial envolvida na
produção do NO e ativação da enzima eNOS em resposta ao α-terpineol, os níveis
de fosforilação das proteínas AKT (Ser 473) e eNOS (Ser 1177) foram investigados
em cultura de células endoteliais de artéria coronária de porco após tratamentos
com α-terpineol (10-4 M) em diferentes períodos de tempo (Figura 37). Constatou-se
que α-terpineol induz fosforilação da enzima eNOS e AKT e estes níveis de
fosforilação aumentaram de acordo com o tempo e se mantiveram estáveis durante
os 30 min. de tratamento.
Figura 37: α-terpineol induz rápida fosforilação da Akt em Ser473 e da eNOS a
Ser1177 em cultura de células endoteliais de coronária de porco. (A) imunoblots representativos; (B) e (C) mostram a análise densitométrica das bandas para p-Akt e
p-eNOS nos diferentes tempos de exposição para a concentração de 10-4 M do α-
terpineol. Os resultados são mostrados como a média ± e.p.m. de 3 a 4 experimentos. * p < 0,05 em relação ao controle representado pelo tempo ―0‖ (ANOVA de uma via com pós-teste de Bonferroni).
B
A
C

99
5.3.2.4 Efeito dependente da concentração do α-terpineol na fosforilação da
AKT e da eNOS em células endoteliais de artéria coronária de porco
α-Terpineol (10-6M, 10-5M, 3x10-5M 10-4M) induziu o aumento da fosforilação
das proteínas AKT em Ser473 e da eNOS em Ser1177 em cultura de células
endoteliais da artéria coronária de porco dependente da concentração em relação ao
controle não tratado (Figura 38). Para estes experimentos utilizamos a insulina (10-6
M) como controle positivo.
Os níveis de fosforilação da AKT foram maiores nas células tratadas com as
concentrações de 3x10-5 M, 10-4 M (Figura 38 B). Esta tendência também foi
observada quanto aos níveis de fosforilação da eNOS, nos quais observou-se um
aumento na fosforilação nas concentrações de 3x10-5 M, 10-4 M (Figura 38)
A
Figura 38: α-terpineol induz fosforilação da Akt em Ser473 e da eNOS em Ser1177
dependente da concentração em cultura de células endoteliais de coronária de porco. (A) imunoblots representativos; (B) e (C) mostram a análise densitométrica das bandas para p-Akt e p-eNOS nos diferentes tratamentos com insulina (10-6 M) e
α-terpineol (10-6 M - 10-4 M). Os resultados são mostrados como a média ± e.p.m. de
3 experimentos. * ou # p < 0,05 em relação ao controle representado pelo tempo ―0‖ (ANOVA de uma via com pós-teste de Bonferroni).
B C

100
5.3.2.5 Efeito do α-terpineol em células endoteliais de artéria coronária de
porco em induzir a fosforilação da AMPK (Tyr 172)
Os níveis de fosforilação da AMPK (Tyr 172) foram fortemente aumentados
pelo tratamento das células endoteliais com o α-terpineol (10-4 M e 3x10-4 M),
durante os primeiros 15 minutos (Figura 39). No entanto os níveis de fosforilação
retornaram os níveis basais nos próximos 30 minutos e demais períodos de tempo
observados.
Figura 39: α-terpineol induz fosforilação da AMPK em Tyr 172 em cultura de células
endoteliais de coronária de porco. (A) imunoblots representativos; (B) e (C) mostram
a análise densitométrica das bandas para p-AMPKα nas concentrações de 10-4 M e
3x 10-4 M de α-terpineol. (Os resultados são mostrados como a média ± e.p.m. * p <
0,05 em relação ao controle representado pelo tempo ―0‖ (ANOVA de uma via com pós-teste de Bonferroni).
A
B C

101
5.3.3 Quantificação dos níveis de NO em células endoteliais de artéria
coronária de porco.
Nossos dados anteriores determinaram que a exposição do α-terpineol a uma
linhagem de células endoteliais de aorta de coelho produziu um aumento da
produção de NO. Para melhor caracterizar a via de sinalização endotelial envolvida
na produção do NO e fosforilação da eNOS, AKT e AMPK em resposta ao α-
terpineol, foram investigados os níveis de produção de NO induzidos pelo α-terpineol
em cultura primária de células endoteliais de artéria coronária de porco. E
observamos que a exposição ao α-terpineol induz aumento da formação de NO, por
aumento da intensidade de fluorescência do DAF-2, analisados por citometria. Este
efeito estimulatório foi reduzido quando as células endoteliais foram pré-tratadas
com o L-NA, um inibidor da eNOS. A produção induzida pela bradicinina foi usada
como controle positivo da produção de NO (Figura 40).

102
Figura 40: Imagens com fluorescência de DAF-2 obtidas nas imagens das culturas
de células endoteliais tratadas com α-terpineol (10-4 M ) ou L-NA (100 μM) + α-
terpineol 10-4 M). As barras correspondem à média ± e.p.m das porcentagens determinadas pela análise de pixels nas imagens escaneadas pelo citomêtro das células endoteliais (n = 3). A bradicinina (10-4 M) foi usada como controle positivo. * p< 0,05 (ANOVA de uma via com pós-teste de Bonferroni).
A
B

103
Discussão

104
6. DISCUSSÃO
A presente tese permite observar em destaque as ações cardiovasculares do
-terpineol em animais hipertensos, caracterizando a farmacodinâmica destes
efeitos. Tendo em conta os resultados parcelares incluídos na tese, estas
considerações deter-se-ão sobre os aspectos referentes ao conjunto de dados no
que diz respeito à: (a) Utilização de modelos experimentais de hipertensão e
controles normotensos in vivo e in vitro e (b) Abordagens bioquímicas para clarificar
os mecanismos moleculares envolvidos.
Em estudos iniciais desenvolvidos pelo nosso grupo (RIBEIRO, 2008)
evidenciamos que o -terpineol produziu efeito hipotensor, associado à diminuição
da resistência vascular dependente do endotélio, caracterizados pelo envolvimento
da via de sinalização L-arginina/ eNOS/ ciclase de guanilil solúvel em animais
normotensos experimentais in vivo. Nesta ordem de investigação, para melhor
compreender as ações cardiovasculares, os efeitos deste monoterpeno foram
avaliados em um modelo experimental de hipertensão espontânea (SHR). Desta
forma, foi observado que α-terpineol induziu uma hipotensão em animais hipertensos
dependente da participação da enzima NOS e produziu melhora na sensibilidade do
barorreflexo, provavelmente decorrente da melhora da função endotelial.
Diante da evidência do -terpineol exercer um efeito protetor sobre o sistema
cardiovascular foram avaliados os efeitos vasculares em modelos de animais
hipertensos e em cultivo de células endoteliais. Notou-se que o -terpineol produziu
um efeito vasorelaxante em animais hipertensos de maneira semelhante aos seus
controles normotensos, envolvendo mecanismos endoteliais de sinalização, como a
participação da via L-arginina/ NO/ GMPc. Em continuidade, foi demonstrado que -
terpineol induziu aumento dos níveis celulares de NO em células endoteliais. Ao
desvendar o mecanismo de sinalização deste monoterpeno em ativar células
endoteliais e estimular a formação de NO, um maior fator vasoprotetor, estes dados
indicaram que o -terpineol induziu a ativação das vias upstreams como a PI3K/AKT
e AMPK que exerceram um papel chave na ativação induzida por fosforilação da
enzima eNOS. Adicionalmente, os resultados obtidos neste trabalho demonstraram
outros mecanismos endoteliais envolvidos no relaxamento produzido pelo -

105
terpineol, associada à participação da via do NO, entre eles, a ativação do EDHF e
canais de potássio do músculo liso vascular.
Inicialmente, neste trabalho, foi evidenciado que a administração aguda de -
terpineol produziu uma hipotensão em animais WKY com livre movimentação (figura
11 A). Estes dados corroboram os resultados anteriormente obtidos no nosso grupo,
onde foi demonstrado que o -terpineol produziu hipotensão associada à taquicardia
e este evento foi sugerido envolver a via NO/ GMPc (RIBEIRO 2008). É importante
salientar que o α-terpineol apresenta baixa toxicidade, com uma DL50 de 4.300
mg/kg do peso corporal, quando administrado em ratos por via oral (JENNER et al.,
1964).
Estudos descreveram que a produção insuficiente de NO contribui para a
disfunção endotelial e alterações vasculares envolvidas na hipertensão(FÉLÉTOU;
KÖHLER; VANHOUTTE, 2011). Desta forma, investigou-se a capacidade do -
terpineol em contribuir com efeitos benéficos para melhora da hipertensão. Não é do
nosso conhecimento estudos com o -terpineol em modelos de hipertensão, além
dos descritos nesse trabalho de tese.
Animais SHR compreendem em um modelo experimental de hipertensão
arterial que se assemelha à hipertensão essencial humana, portanto, é amplamente
utilizado em estudos experimentais. Utilizamos animais não-anestesiados nos
experimentos para medida direta da pressão arterial (PA), uma vez que a anestesia
modifica o funcionamento dos principais sistemas de regulação da pressão arterial,
tais como o sistema renina-angiotensina, o sistema nervoso simpático e o
barorreflexo, produz depressão de algumas sinapses do sistema nervoso central,
alterando as respostas autonômicas, além de outros efeitos sobre os sistemas
básicos de controle fisiológico da pressão arterial (DORWARD et al., 1985;
FLUCKIGER et al., 1985).
Os dados demonstraram que de forma peculiar, -terpineol produziu a
diminuição da pressão arterial média dependente da dose, em animais hipertensos,
associado à taquicardia e bradicardia (Figura 11 B, D; Figura 12). Observou-se,
ainda, que -terpineol produziu efeito hipotensor superior em animais SHR em
comparação aos animais normotensos WKY, sem alterar as respostas taquicárdicas
e bradicárdicas (Figura 13 e Figura 14).

106
Para examinar a origem da hipotensão inicial, ocasionada pelo -terpineol, que
ocorre concomitantemente com uma taquicardia inicial e seguida de uma bradicardia
em animais hipertensos. Os experimentos foram focados, inicialmente, na
diminuição na pressão arterial (PA) resultante da inibição tônica vagal da freqüência
cardíaca, do débito cardíaco e do sistema nervoso simpático (SNS) do coração e da
vasculatura. Assim, o tratamento com inibidores poderia impedir as mudanças na
transição do sistema nervoso autônomo e das atividades que ocorrem durante o
curso da hipertensão. Em um grupo separado dos animais SHR e WKY, os animais
foram tratados com atropina e foi observado que as respostas hipotensora -
terpineol ED50 4,8 mg / kg, (i.v.) permaneceram inalteradas, no entanto, a resposta
bradicárdica secundária foi abolida, sugerindo a participação da ativação secundária
do barorreflexo no efeito hipotensor induzido pelo -terpineol (Figura 15). Estes
dados apresentam semelhança a outros estudos com respostas bifásicas exercidas
por compostos com ações cardiovasculares (INTERAMINENSE et al., 2011).
Em continuidade, avaliou-se o papel do sistema nervoso autônomo no efeito
cardiovascular do α-terpineol em animais hipertensos. Foi observado que os
inibidores como atenolol e hexametônio foram capazes de alterar a resposta do
monoterpeno sobre a bradicardia mediada pelo barorreflexo em SHR e WKY. No
entanto, a hipotensão não foi alterada (Figura 16 e 17). Este resultado foi esperado,
uma vez que, o bloqueio autonômico cardíaco não altera o efeito que diminui a PA.
Portanto, sugere que a bradicardia secundária é reflexa a ação da ativação dos
barorreceptores durante o rápido aumento da PA, observado na taquicardia inicial
decorrente do -terpineol. Esta atividade bradicárdica é normalmente mediada pelo
sistema nervoso parassimpático em ratos conscientes. A segunda constatação
importante do estudo é que as respostas hipotensoras ao -terpineol também
permaneceram inalterados após o tratamento com prazosin, um -1-adrenoceptor
seletivo antagonista, em ratos SHR e WKY (Figura 18).
A homeostase cardiovascular é controlada e coordenada por uma interação
contínua de mecanismos neurais e humorais. Os fatores vasculares são capazes de
diminuir a pressão arterial por promover a formação de fatores relaxantes derivados
do endotélio, como o NO com participação da via L-arginina- NO- GMPc. Diante
destas projeções, demonstramos através do bloqueio farmacológico da enzima NOS
(L-NAME), que os efeitos hipotensores em SHR e WKY induzidos pelo -terpineol

107
envolvem a ativação da enzima eNOS e conversão da L-arginina em NO (Figura 19).
No entanto, a utilização do L-NAME não produziu alterações sobre a bradicardia
secundária exercida 3 minutos após o tratamento com o monoterpeno, indicando
que o efeito é, em parte, devido a uma vasodilatação periférica e envolve a NOS no
vaso.
Portanto, neste estudo, demonstramos pela primeira vez as ações
cardiovasculares do tratamento intravenoso do -terpineol em animais hipertensos,
o qual produziu hipotensão envolvendo a participação da enzima NOS em animais
hipertensos. De maneira semelhante, as nossas evidências anteriores relacionadas
com os efeitos cardiovasculares do α-terpineol, em animais normotensos, nos
direcionam ao mecanismo relacionado à participação de óxido nítrico vascular
(RIBEIRO, 2008).
Os dados obtidos com o -terpineol disponíveis até o momento sugerem que
este monoterpeno exerce uma influência sobre mecanismos neuro-humorais de
controle da PA. Considerando que mudanças subsequentes na pressão arterial são
mediadas pelo sistema nervoso autônomo e a desregulação autonômica tem sido
reconhecida como um importante fator de alteração cardiovascular, com diminuição
na sensibilidade do barorreflexo cardíaco e alteração do balanço simpático-
parassimpático. Em sequência, a hipótese do α-terpineol em exercer influências
sobre a melhora do ganho no sistema barorreflexo foi avaliada.
Estudos anteriores evidenciaram que SHR com 13 semanas de idade já
apresentam reflexo barorreceptor prejudicado, no que diz respeito ao componente
parassimpático quando comparados com ratos controle normotensos (WKY)
(CORDELLINI et. al., 2006). Deste modo, para conhecer os efeitos antes ou depois
do pré-tratamento com -terpineol sobre a função barorreflexa, foi avaliado a
sensibilidade do barorreflexo em animais SHR e WKY acima de 13 semanas. E os
dados obtidos nos permitem afirmar que o -terpineol foi capaz de aumentar a
sensibilidade do barorreflexo (Figura 20) e este efeito pode ser atribuído,
possivelmente, por melhora da função endotelial.
A hipótese da interação entre NO e sistema nervoso simpático em regular
pressão sanguínea normal não pode ser descartada. Além disso, recentemente foi
relatado que a interação entre NO e o reflexo de baroreceptores exerce papel no

108
controle à longo prazo da pressão sanguínea (RAJAPAKSE; MATTSON, 2009).
Várias questões têm relacionado os mecanismos que envolvem a modulação da
frequência cardíaca com o NO, em particular interações existentes entre a via do NO
e do sistema nervoso autônomo (CHOWDHARY; TOWNEND, 1999,
CHARKOUDIAN; RABBITTS 2009).
Para melhor compreender a natureza do efeito hipotensor observado nos
experimentos in vivo com animais hipertensos, foram investigadas as atividades do
·α-terpineol utilizando o modelo experimental in vitro de artéria mesentérica superior
isolada rato, baseadondo-se em relatos de influências do componente vascular e o
papel importante na manutenção da PA. Os vasos de artéria mesentérica foram
utilizados uma vez que apresentam maior resistência à passagem do fluxo e são
amplamente implicadas na regulação do débito sanguíneo e da pressão capilar,
refletindo, desta forma, as variações da resistência periférica global (FOLKOW,
1982; AALKJAER, et. al., 1987). Inicialmente observou-se que o -terpineol não
exerce qualquer alteração sobre o tônus basal (Figura 22 e 23).
O endotélio vascular apresenta papel importante no controle do tônus vascular
e da pressão arterial através da liberação de substâncias vasoativas que agem
diretamente em células do músculo liso vascular, causando contração ou
relaxamento (SERBAN et. al. 2010). Várias substâncias derivadas do endotélio
podem causar relaxamento do músculo liso isolado: óxido nítrico (NO), prostaciclinas
(PGI2), e ácidos epoxieicosatrienóicos (FLEMING, 2010; FÉLÉTOU; VANHOUTTE,
2010). Assim, estudos que introduzem novas substâncias capazes de relaxar
artérias através do estímulo da liberação do NO endotelial têm sido relatados.
(LUCIANO et. al. 2011, SCHINI-KERT et. al., 2010).
Magalhães (2008) explanou que constituintes de óleos essenciais foram
capazes de diminuir a resistência vascular, em leito mesentérico, demonstrando a
característica de efeitos promissores desses constituintes no sistema cardiovascular.
Em nossos estudos anteriores, constatou-se que o -terpineol induziu um
relaxamento em animais normotensos, dependente do endotélio vascular e este
efeito foi mediado pela via NO/GMPc (RIBEIRO, 2008).
Na hipertensão vários modelos experimentais apresentam diminuições do
relaxamento em resposta a acetilcolina. (VANHOUTTE, 2011, FÉLÉTOU;

109
VANHOUTTE, 2010). Os mecanismos implicados nestes efeitos envolvem, em maior
parte, a inativação e desacoplamento da enzima eNOS, diminuição da
disponibilidade de NO e de outros fatores relaxantes derivados do endotélio e ainda,
o aumento da produção de ROS (FÖRSTERMANN; SESSA, 2011; FLEMING, 2010).
Dessa forma, estudos demonstram que diferentes compostos podem exercer
proteção vascular na hipertensão através de duas formas: (a) por meio da ação
direta nas células endoteliais, resultando no aumento da atividade da eNOS e/ou da
síntese e liberação do NO e EDHF (SCHINI-KERTH 2010; RAMLI, et. al. 2011), ou
(b) devido à habilidade desses compostos de prevenir a oxidação do NO,
aumentando a sua biodisponibilidade e diminuindo a produção de ROS
(TOMASONI, et. al. 2010; WALLACE, 2011)
Desta forma, foram avaliados os mecanismos de sinalização celular em que o
-terpineol poderia produzir um efeito vasoprotetor em um modelo experimental para
hipertensão. Nesta perspectiva, foi desenvolvido um estudo para avaliar o efeito
vasorelaxante do -terpineol em artéria mesentérica superior de rato SHR. Neste
vaso, o -terpineol causou o relaxamento dos anéis com endotélio vascular, de
forma dependente da concentração em animais hipertensos e seus controles
normotensos (Figura 21) e este efeito foi inibido na presença do L-NAME (inibidor
das NOS) (Figura 24 A e B). Estes resultados demonstram a participação NO no
mecanismo vasorelaxante do monoterpeno em vasos de resistência e corroboram
com os efeitos observados em ratos Wistar albinos normotensos (RIBEIRO, 2008).
A contínua produção de NO pelo endotélio vascular é crucial para regulação da
pressão arterial e regulação do fluxo sanguíneo foi utilizada a hidroxocobalamina (30
μM) para confirmarmos que NO, induzido pelo α-terpineol, seria o mediador
responsável pela resposta vasorelaxante em SHR, dependente de endotélio (Figura
25 A e B). A hidroxicobalamina, um seqüestrador do NO, apresenta a cobalamina
oxidada (Cb (III)) em sua estrutura, que captura o NO assim que ele sai da célula
endotelial formando um complexo Cb(III)–NO (KRUSZYNA et al., 1998). Desse
modo a resposta em anéis de artéria mesentérica de rato hipertenso e normotenso
com endotélio foi atenuada, sugerindo que o NO uma vez produzido poderá interagir
com sítios de ação na célula muscular lisa vascular.
Diferentes trabalhos têm demonstrado que o NO produz seus efeitos por via
dependente de GMPc, através da um mecanismo mediado por proteínas cinases

110
dependentes de GMPc (PKG) (STASCH; HOBBS, 2009). A PKG promove
fosforilações que levam a ativação da bomba de Ca2+ no retículo sarcoplasmático
(SERCA); aceleração da recaptação de Ca2+ para os estoques intracelulares;
abertura dos canais para K+ na membrana plasmática hiperpolarizando as células
musculares lisa; fechamento dos canais para Ca2+; ativação do trocador Na+/Ca2+.
Todos estes eventos levam a uma redução concentração de cálcio intracelular. Além
disso, a PKG promove fosforilação da cinase da cadeia leve da miosina (MLCK),
inativando-a, e estes eventos em conjunto promovem o vasorrelaxamento,
diminuindo assim a resistência vascular periférica (VANHOUTTE; BOULANGER,
1995; IRVINE; FAVALORO; KEMP-HARPER, 2003; HILGERS; WEBB, 2005, TODA,
2011). Assim, o pré-tratamento com ODQ, inibidor da ciclase de guanilil solúvel,
reduziu a resposta relaxante induzida por concentrações crescentes de -terpineol
em anéis de artéria mesentérica de rato SHR e WKY (Figura 25 A e B), indicando a
participação da via NO-GMPc.
Para confirmar se o NO seria o mediador responsável pela resposta relaxante
do -terpineol, dependente de endotélio vascular, realizamos experimentos em
linhagem de células endoteliais de aorta de coelho. Estes dados demonstraram a
capacidade da célula endotelial de aumentar os níveis de produção de NO em
condições tratadas com acetilcolina e bradicinina (Figura 30). Foi observado que, na
presença da bradicinina a produção de NO é superior a indução de NO promovida
pelas diferentes concentrações de acetilcolina. Estes dados corroboram dados na
literatura que demonstram maior expressão de receptores para bradicinina em
relação à de acetilcolina, demonstrado no efeito de indução da produção de óxido
nítrico (WOODLEY,et al. 1994; WANG et al.,1995). De maneira semelhante, o
tratamento com o -terpineol induziu aumento dos níveis de NO e esta indução foi
prevenida pelo tratamento com L-NAME, confirmando a participação da eNOS
(Figura 31 A e B; Figura 32; 33; 34 A e B).
Como já referido, a ativação da NOS ocorre com a ligação da calmodulina
ligada ao Ca2+ ou dependente da adição de um fosfato no resíduo de Ser 1177 em
seu sítio de ligação (FLEMING; 2010). Estudos demonstram existir diferenças
temporais na relação entre a indução do aumento da concentração de Ca2+
intracelular em células endoteliais e ativação de NOS, além das mudanças nos
níveis intracelulares de Ca2+ (PRESTA et al., 1997), vários mecanismos para regular

111
atividade de NOS foram propostos, incluindo a interação da NOS com proteínas
(entre elas a Hsp90 e caveolina-1), fosfolipídios de membrana, fosforilação com
participação de proteínas cinases, como também alterações no pH fisiológico
(PRITCHARD 2001; KIM, 2005; RATH 2009; FLEMING et al., 2010).
Nesse sentido, foram realizados estudos adicionais, em cultura primária de
células endoteliais de artérias coronárias de porco, para confirmar se o -terpineol
estaria relacionado com a ativação direta da NOS. Para isso, foi utilizada uma
metodologia que identifica a atividade da eNOS, de acordo com o nível de
fosforilação presente. A fosforilação da eNOS no resíduo de Ser1177 é
característica de ativações dependentes de proteínas cinases.
Em células endoteliais a insulina produz ativação da eNOS devido a
fosforilação do resíduo de Ser 1177 e este evento é dependente da ativação da AKT
(FULTON et al. 1999). Verificou-se que após o tratamento com a insulina a eNOS
apresentou um aumento da fosforilação dependente de tempo e concentração em
Ser1177 em cultura primária de células endoteliais de coronária de porco (Figura
35). Este mecanismo foi descrito para ativações decorrentes também de outros
receptores tirosina cinase (GONZÁLEZ-SÁNCHEZ; SERRANO-RÍOS 2007).
O tratamento das células endoteliais de artéria coronária de porco com -
terpineol produziram fosforilação da eNOS no resíduo de Ser 1177. Este efeito foi
observado pela fosforilação aumentada nas diferentes condições experimentais,
dependente do tempo de tratamento e concentração, resultado semelhante ao
encontrado na indução pela insulina (Figura 36 e 38). O -terpineol induziu uma
ativação persistente da via da eNOS mesmo após um curto período de tratamento (5
minutos) em células endoteliais de artéria coronária. Este dado foi semelhante aos
observados com o relaxamento de anéis de artéria mesentérica, em que o período
de tratamento foi de 2-5 min.
Dado a redundância que é inerente em sistemas fisiológicos, e a importância
crítica da fosforilação da eNOS em Ser1177 para produção de NO, não é
surpreendente que diferentes proteínas cinases estejam envolvidas nesta ativação
em resposta a estímulos, como a força de cisalhamento e fator de crescimento
endotelial vascular (NAKAGAWA; JOHNSON, 2011). A participação da proteína
cinase B (AKT) dependente da ativação da PI3-cinase foi investigada após o

112
tratamento com o -terpineol em conduzir à fosforilação em Ser1177 da eNOS. De
tal modo, foi mostrado que o -terpineol induziu a ativação da via PI3-cinase/AKT
em células endoteliais e este efeito foi dependente de concentração e apresentou
intensidade de fosforilação máxima em 30 minutos (Figuras 37 e 38). Este evento
sugere que a fosforilação da eNOS em Ser1177 (um sítio ativador) é secundária a
ativação da AKT. Estes dados são semelhantes ao encontrados na literatura ao que
concerne a ativação da eNOS decorrente do tratamento com diferentes produtos
naturais (LORENZ et. al. 2004; EDIRISINGHE et. al. 2008; ANSELM et. al, 2009).
Dentre as proteínas cinases envolvidas na ativação da eNOS, foi relatado que
a via de sinalização dependente da proteína cinase AMPK foi descrita fosforilar
resíduos de Ser1177 em diferentes modelos animais (LEVINE; LI; MICHEL, 2007;
FISSLTHALER 2007; 2009). O aumento da fosforilação da porção AMPKα (Thr 172)
foi observado em células endoteliais, após o tratamento com o -terpineol,
principalmente no tempo inicial de 15 minutos (Figura 39). Semelhante a esta
ativação, a AMPK é dependente de alterações do metabolismo celular e estímulos
como a força de cisalhamento e uma relação de elevada de AMP para ATP (SESSA
et al., 1992; ZHANG et. al., 2009). Esta fosforilação induzida pelo monoterpeno
indica que esta sinalização dependente de proteínas cinases é um importante
regulador upstream da p-eNOS Ser1177.
A sinalização induzida pelo -terpineol, via ativação das redes de interações
celular da AKT e AMPK (como mostrado no estudo presente), poderia evitar falhas
específicas na sinalização de fosforilação da eNOS em Ser1177 e aumentar a
biodisponibilidade de NO. Dessa forma, nós avaliamos as ações do -terpineol
sobre a indução da produção de NO, durante o sinal de transdução que induz a
fosforilação e consequente ativação da eNOS, em células endoteliais de artéria
coronária de porco. A meia vida do NO é muito curta, portanto, foi utilizado uma
metodologia associada à citometria com sensível detecção para o NO, a sonda
fluorescente DAF-2DA. Nós observamos que o -terpineol induz o aumento da
intensidade de fluorescência, caracterizando o aumento dos níveis de NO nesse tipo
celular e prevenida após o pré-tratamento com L-NAME (Figura 40), o que corrobora
os dados anteriores obtidos em linhagem de célula endoteliais de aorta de coelho.
Além do NO, o endotélio vascular produz um fator relaxante que produz
hiperpolarização no músculo liso vascular, que age independentemente da via do

113
NO e das prostaciclinas. Dentre os bloqueadores, o uso de apamina concomitante
com caribdotoxina demonstrou bloquear respostas produzidas por fatores
hiperpolarizantes derivados do endotélio (EDHF) (BUSSE et al., 2003, FELETOU;
VANHOUTTE 2010). Neste trabalho o relaxamento induzido pelo -terpineol foi
afetado pela associação de caribdotoxina + apamina, ambos bloqueadores de
canais KCa, envolvidos no mecanismo de ação vasorrelaxante do EDHF em vasos de
resistência de animais hipertensos (Figura 27).
Estudos foram propostos onde o NO, via GMPc, pode ativar vários tipos de
canais de potássio presentes na membrana plasmática do músculo liso vascular
(COLEMAN et al., 2004). Essa ativação poderia ser realizada também por uma via
independente da ativação de ciclase de guanilil solúvel, levando à hiperpolarização e
relaxamento das células musculares lisas (BOLOTINA et al., 1994). Para
evidenciarmos a participação de canais de potássio no vasorrelaxamento induzido
pelo α-terpineol, realizamos experimentos na presença de diferentes inibidores
destes canais.
Quatro classes diferentes de canais para K+ são expressas células de músculo
liso vascular. Estes incluem canais para K+ retificadores internos (KIR), canais para
K+ sensíveis a ATP (KATP), canais para K+ ativados pelo Ca2+ (KCa), e canais para K+
ativados por voltagem (KV) (IUPHAR 2002; HADDY et al., 2006).
Segundo a literatura, os abridores de canal de K+ são eficazes em inibir a
contração da musculatura lisa vascular em condições de aumento moderado da
concentração externa de potássio (< 40 mM) enquanto que, em níveis maiores de K+
externo são desprovidos deste efeito (NELSON, 1995). Uma vez que em altas
concentrações de K+, o potencial de membrana da célula muscular lisa está muito
próximo do potencial de equilíbrio do K+, onde o fluxo resultante de K+ e
hiperpolarização são evitados (NELSON, 1995). Em condições experimentais, em
anéis de artéria mesentérica de ratos hipertensos, foi observado que a presença 20
mM de KCl atenuou significantemente a resposta vasorelaxante induzida pelo -
terpineol em relação ao controle, de maneira similar este efeito foi reduzido na
presença de tetraetilamônio um inibidor de canais de potássio quando usado a altas
concentrações (> 1mM) em menores concentrações estas drogas são seletivas para
canais BKCa (BRAYDEN; NELSON, 1992). Sugerindo a participação dos canais para
K+ na indução neste vasorrelaxamento (figura 28).

114
Farouque (2003) demonstrou a interação entre canais para KATP e os fatores
vasoativos derivados do endotélio no controle do fluxo sanguíneo sobre o músculo
esquelético. Conforme descrito na literatura hiperpolarizações causadas por NO
normalmente são prevenidas por bloqueadores de canais KATP. Portanto, verificou-se
que a glibenclamida, um inibidor destes canais, em anéis com endotélio de artéria
mesentérica superior isolada de rato hipertenso foi capaz de atenuar
significativamente a resposta vasorelaxante induzida por -terpineol (Figura 29).
A ativação de canais KV aumenta efluxo de K+, resultando em hiperpolarização
de membrana. Estes canais são ativados por despolarização da membrana e têm
participação na regulação de retroalimentação negativa ao longo do potencial de
membrana associado a outros canais para K+ (JACKSON, 2000; 2005). Estes canais
em células musculares lisas constituem um mecanismo essencial na regulação da
despolarização e conseqüente vasoconstrição como também parecem estar
envolvidos na repolarização, além disso, o NO é capaz de ativar canais KV em
algumas artérias e ativá-los por mecanismos dependentes e independentes de
GMPc (COSTA et al., 2001; IRVINE; FAVALORO; KEMP-HARPER, 2003; YUAN et
al., 1996; JACKSON 2005). Costa e colaboradores (2001) propuseram ainda que
formas reduzidas de NO também sejam capazes de ativar canais KV em músculo liso
por um mecanismo dependente de GMPc. A diminuição da disponibilidade do NO
derivado do endotélio como presente em animais hipertensos SHR, pode levar à
despolarização das células musculares vasculares e conseqüente contração devido
à inibição ou fechamento dos canais KV (IRVINE; FAVALORO; KEMP-HARPER;
2003, JACKSON, 2005, FELETOU; VANHOUTTE, 2000). A 4-aminopiridina (4-AP)
(1 mM), um bloqueador seletivo de canais para K+ dependente de voltagem (KV)
(SOBEY, 2001; FOZARD; MANLEY, 2001) teve proeminente efeito inibitório,
sugerindo que a abertura destes canais (e conseqüente hiperpolarização da
membrana de células musculares lisas) é requerida para o vasorrelaxamento
induzido pelo -terpineol em anéis de artéria mesentérica de rato SHR na presença
do endotélio (Figura 29).
Nos vasos, as prostaciclinas são formadas em células endoteliais a partir de
uma sequência de reações enzimáticas iniciada pela ciclooxigenase (COX) e se
difundem até as células musculares (VANHOUTTE, 2009). O mecanismo de ação da
PGI2 envolve a ativação da proteína Gs, ativação da ciclase de adenilil e aumento
dos níveis intracelular de AMPc, promovendo a ativação da PKA e conseqüente

115
vasodilatação (VANHOUTTE, 2011). Para verificar a influência das prostaciclinas no
relaxamento induzido pelo -terpineol, foi utilizado a indometacina (10 μM) e
constatamos que o relaxamento induzido por este monoterpeno não foi atenuado
sugerindo que produtos formados a partir da via da COX não participam deste efeito
(Figura 26).
A liberação do NO e outros fatores relaxantes é conseqüente da ação de
mediadores endoteliais estimulados por diversas substâncias, endógenas ou não,
que agem em receptores localizados na membrana das células endoteliais, como a
acetilcolina (FURCHGOTT, 1983). Adicional a este conceito, nossos resultados
demonstraram que a atropina (um antagonista seletivo dos receptores muscarínicos)
não foi capaz de inibir a vasodilatação induzida pelo -terpineol em ratos
normotensos (Figura 26).
Dessa forma, é de grande interesse evidenciar a participação de receptores de
membrana da célula endotelial em resposta ao -terpineol, bem como a
possibilidade de mecanismos de ativação dependentes de proteínas cinases (AMPK
ou a via PI3-cinase/Akt) modular junções gap mioendoteliais e/ou atividade de
canais de potássio ainda precisa ser investigada. Recentes estudos apontam para o
envolvimento da AMPK ou da via PI3-cinase/ AKT na regulação KATP, KIR ou BKCa
(HABA et. al., 2010, CHANG et. al., 2009; DAL-CIM 2011), entretanto, o papel na
regulação da função vascular não está bem elucidada e carece de mais estudos.
Outro tópico de interesse está em conhecer as ações do monoterpeno em prevenir o
estresse oxidativo e assim contribuir com os demais mecanismos que previnem a
disfunção endotelial, uma vez que existem relatos na literatura que demonstram o
potencial antioxidante de vários monoterpenos (SINGH, 2010).
A formação de fatores endoteliais vasoprotetores induzido pelo -terpineol,
demonstrados neste trabalho, podem ajudar a esclarecer os efeitos benéficos
exercidos no sistema cardiovascular. O efeito benéfico está associado à restauração
dos efeitos vasoprotetores por induzir a formação de NO, aumento da atividade da
eNOS, via ativação de proteínas envolvidas com a prevenção de alterações do
metabolismo celular, como apoptose (PI3K/AKT) e diminuição do ATP disponível
(AMPK), fatores que contribuem para diminuir a disfunção endotelial. Por
conseguinte, o -terpineol demonstrou ser capaz de diminuir o estado excitável da

116
célula muscular lisa vascular, e originando a hiperpolarização, o que produz a
redução do potencial de membrana reduzindo o estado contrátil da célula muscular,
fator primordial para estados de prevenção e/ou tratamento para hipertensão.
Por fim, coletivamente neste trabalho, demonstrou-se a capacidade do -terpineol
em induzir a hipotensão e diminuir a resistência vascular periférica mediado por fatores
relaxantes derivados do endotélio em animais hipertensos. Este evento está implicado
acontecer no endotélio vascular, onde o -terpineol induz a ativação da via PI3-cinase/
AKT e AMPK e consequente ativação da enzima eNOS com aumento da produção de
NO e como conseqüência deste evento, ocorre a ativação da enzima ciclase de guanilil
solúvel. Um fato interessante foi que o -terpineol demonstrou-se capaz de induzir a
formação de outros fatores relaxantes derivados do endotélio, como o EDHF,
associado à ativação de canais KCa, KATP e KV (Figura 41).
Estes efeitos produzidos pelo -terpineol desempenham um papel crucial no
controle da homeostase vascular, incluindo em modelos experimentais de
hipertensão in vivo e in vitro. Portanto, estes efeitos obtidos com -terpineol revelam
a importância dos estudos que podem contribuir com substâncias que contenham a
propriedade de modular a produção endógena do NO, tendo os produtos naturais
como uma importante fonte.

117
Figura 41: Representação da farmacodinâmica do α-terpineol. Ativação de proteínas cinases AKT e AMPK envolvidas na fosforilação da eNOS (Ser 1177) e consequente produção de NO, associado a produção do EDHF, em células endoteliais, os quais favorecem o relaxamento na célula muscular lisa.

118
Conclusões

119
CONCLUSÕES
Conforme demonstrado, os resultados do presente estudo nos permitem concluir:
O -terpineol promove um vasorrelaxamento em anéis de artéria
mesentérica superior isolada de rato ocorre de maneira dependente de
endotélio vascular, com aumento dos níveis de NO em cultura celular.
A infusão intravenosa de -terpineol promove hipotensão e alterações nas
respostas cardiovasculares e reflexas, com aumento do ganho do
barorreflexo, em animais hipertensos e normotensos.
Verificamos que o -terpineol induz hipotensão e taquicardia em ratos
hipertensos e normotensos não-anestesiados. E esta hipotensão parece
estar envolvida, em parte a via L-arginina-NO-GMPc.
Identificamos a sinalização em que o -terpineol induz relaxamento, que
envolve mecanismos endoteliais NO/GMPc, e EDHF em artéria
mesentérica de animais hipertensos e normotensos.
O -terpineol leva a ativação de vias que acionam proteínas cinases como
AKT e AMPK para induzir a fosforilação da eNOS e consequente
produção de NO em células endoteliais.
A participação dos canais de K+ na vasodilatação induzida pelo -terpineol
em artéria mesentérica de rato hipertenso SHR e WKY foi confirmada, o
que leva à ativação de canais de K+ KCa, KATP, KV e hiperpolarização da
membrana da célula muscular, com conseqüente vasorrelaxamento.

120
Perspectivas

121
PERSPECTIVAS
Atualmente, o -terpineol oferece uma alternativa para os estudos que
avaliam os efeitos benéficos para o sistema cardiovascular. Novos estudos são
propostos para avaliar a farmacodinâmica do -terpineol sobre os fatores
predisponentes que desencadeiam o estresse oxidativo. Assim, poderemos
identificar alternativas para prevenção e/ou tratamento de condições relacionadas à
disfunção endotelial e levam a doenças cardiovasculares, como a hipertensão,
aterosclerose, e demais fatores de risco, como diabetes, resistência a insulina e
obesidade. Em adição, demais propostas de grande interesse podem ser
desenvolvidas para estudos de farmacocinética e desenvolvimento farmacotécnico,
em uma visão para o desenvolvimento de novas moléculas que visem à terapêutica.
.

122
Referências

123
REFERÊNCIAS
AALKJAER, C.; HEAGERTY, A. M.; PETERSEN, K. K.; SWALES, J. D.; MULVANY,
M. J.; Evidence for increased media thickness, increased neuronal amine uptake,
and depressed excitation-contraction coupling in isolated resistance vessels from
essential hypertensives. Circ. Res., v. 61, p.181-186, 1987.
ADEAGBO, A. S.; JOSHUA, I. G.; FALKNER, C.; MATHESON, P. J.; Tempol, an
antioxidant, restores endothelium-derived hyperpolarizing factor mediated
vasodilation during hypertension. Eur. J. Pharmacol., v.481, p. 91–100, 2003.
ALBUQUERQUE, A. A. C.; SORENSON, A. L.; LEAL-CARDOSO, J. H.; Effects of
essential oil of Croton zehntneir and of anethole and estragole on skeletal muscles.
J. Pharmacol., v. 49, p. 41-49, 1995.
ALEXANDER, S. P. H.; PETERS, J. A.; Receptor e ion channel nomenclature
supplement. Tr. Pharmacol. Sci., v. 21(suppl.), p. 106-112, 2000
ALIOUA, A.; TANAKA, Y.; WALLNER, M.; HOFMANN, F.; RUTH, P.; MEERA, P.;
TORO, L. The large conductance, voltage-dependent, and calcium-sensitive K+
channel, Also, is a target of cGMP-dependent protein kinase phosphorylation in vivo.
J. Biol. Chem., v.273, p.32950–32956,1998.
ALMEIDA, R. N.; MOTTA, S. C.; LEITE, J.R. Óleos essenciais com propriedades
anticonvulsivantes. Bol. Lat. Am. Caribe Plantas Med. Aromat., v.2, p.3–6, 2003.
ALTURA, B. M.; ALTURA, B. T.; Differential effects of substrate on drug-induced
contractions of rabbit aorta. Am. J. Physiol., v,219, p.1698-705,1970.
ANSELM, E.; CHATAIGNEAU, M.; NDIAYE, M.; CHATAIGNEAU, T.; SCHINI-
KERTH, V. B. Grape juice causes endothelium-dependent relaxation via a redox-
sensitive Src- and Akt-dependent activation of eNOS. Cardiovasc Res. v. 15; 73(2),
p.404-13, 2007.

124
ANSELM, E.; SOCORRO, V. F.; DAL-ROS, S. et al., Crataegus special extract WS
1442 causes endothelium-dependent relaxation via a redox-sensitive Src- and Akt-
dependent activation of endothelial NO synthase but not via activation of estrogen
receptors. J. Cardiovasc. Pharmacol., v.53, p. 253–260, 2009.
ARCHER, S. L.; WU, X. C.; THEBAUD, B.; NSAIR, A.; BONNET, S.; TYRRELL, B.;
et.al. Preferential expression and function of voltage-gated, O2-sensitive K+ channels
in resistance pulmonary arteries explains regional heterogeneity in hypoxic
pulmonary vasoconstriction: ionic diversity in smooth muscle cells. Circ. Res., v.
95(3), p. 308-18, 2004.
BAKKALI, F.; AVERBECK, S.; AVERBEC, D.; IDAOMAR, M. Biological effects of
essential oils – A review. Food Chem. Toxicol., v.46: (2), p. 446-475, 2008.
BARBOSA-FILHO, J. M.; CUNHA, R. M.; DIAS, C. S.; ATHAYDE-FILHO, P. F.;
SILVA, M. S.; DA-CUNHA, E. V. L.; MACHADO, M. I. L.; CRAVEIRO, A. A.;
MEDEIROS, I. A. GC-MS analysis and cardiovascular activity of the essential oil of
Ocotea duckei Rev. Bras. Farmacog., v.18: (1), p.56– 61, 2008.
BARREIRO, E. J.; Produtos naturais bioativos de origem vegetal e o
desenvolvimento de fármacos. Quím. Nova., v. 13 (1), p. 29- 39, 1990.
BASTOS, J. F.; MOREIRA, I. J.; RIBEIRO, T. P.; MEDEIROS, I. A.; ANTONIOLLI, A.
R.; DE SOUSA, D. P.; SANTOS, M. R. Hypotensive and Vasorelaxant Effects of
Citronellol, a Monoterpene Alcohol, in Rats. Basic Clin. Pharmacol. Toxicol., v.106
(4), p. 331 – 337, 2010. doi.10.1111/j.1742-7843.2009.00492.x
BEZERRA, M. A. C.; Alpinia speciosa Schum: Estudo das frações fixas e do óleo
essencial. 1994. Dissertação (Mestrado em Farmacologia) - Departamento de
Fisiologia e Farmacologia, Universidade Federal do Ceará. Fortaleza
BIRD, I. M. Endothelial nitric oxide synthase activation and nitric oxide function: new
light through old windows. J. Endocrinol., v.210(3), p.239-41, 2011.

125
BOLOTINA, V.M.; NAJIBI, S.; PALACINO, J. J.; PAGANO, P. J.; COHEN, R. A. Nitric
oxide directly activates calcium-dependent potassium channels in vascular smooth
muscle. Nature, v. 28, p.850–853, 1994.
BOURQUE, S.L.;DAVIDGE, S.T.; ADAMS, M. A. The interaction between endothelin-
1 and nitric oxide in the vasculature: new perspectives. Am. J. Physiol. Regul.
Integr. Comp. Physiol., v. 300 (6), p.R1288-95, 2011.
BRAAM, B.; VERHAAR, M. C. Understanding eNOS for pharmacological modulation
of endothelial function: a translational view. Curr. Pharm. Des.,. v.13(17), p.1727-40,
2007.
BRADFORD, M. M. A rapid and sensitive method for the quantitation of microgram
quantities of protein utilizing the principle of protein-dye binding. Anal. Biochem.,
v.72 (7), p.248-54. 1976.
BRÄHLER, S.; KAISTHA, A.; SCHMIDT, V. J.; WÖLFLE, S. E.; BUSCH, C.;
KAISTHA, B. P.; KACIK, M.; HASENAU, A. L., et.al. Genetic deficit of SKca and IKca
channels disrupts the endothelium-derived hyperpolarizing factor vasodilator pathway
and causes hypertension. Circulation, v.5;119(17), p.2323-32, 2009.
BRAYDEN, J. E.; Functional roles of KATP channels in vascular smooth muscle. Clin.
Exp. Pharmacol. Physiol., v. 29, p. 312-316, 2002.
BRAYDEN, J. E.; NELSON, M. T. Regulation of arterial tone by activation of calcium-
dependent potassium channels. Science, v.256, p.532−535.
BRUNNER H. R.; NUSSBERGER J.; WAEBER B. Angiotensin II blockade compared
with other pharmacological methods of inhibiting the renin-angiotensin system. J.
Hypertension, v. 11 (Suppl. 3) p. 53-58, 1993.
BUSSEMAKER, E.; POPP, R.; FISSLTHALER, B.; LARSON, C. M.; FLEMING, I.;
BUSSE, R. .; et al.. Aged spontaneously hypertensive rats exhibit a selective loss of

126
EDHF-mediated relaxation in the renal artery. Hypertension, v. 42, p. 562–568,
2003.
CAI, H.; LIU, D.; GARCIA, J. G. CaM Kinase II-dependent pathophysiological
signalling in endothelial cells. Cardiovasc. Res., v.77(1), p.30-4, 2008.
CALIXTO, J. B.; KASSUYA, C. A. L.; ANDRÉ, E.; FERREIRA, J. Contribution of
natural products to the discovery of the transient receptor potential (TRP) channels
family and their functions. Pharmacol. Therap., v. 106, p. 179 - 208, 2005.
CAMPBELL, W. B.; FALCK, J. R.; EVANGELOS, D.; MCMURTRY, M.; KIM, D. H.;
PLATONOV, M.; KOSHAL, A.; HASHIMOTO, K.; ARCHER, S. L.; GRAGASIN, F. S.;
WU, X.; SEAN, S. W.; Channels Ca2+ Smooth Muscle BK Artery Is 11,12-
Epoxyeicosatrienoic Acid and Causes Relaxation by Activating Endothelium-Derived
Hyperpolarizing Factor in Human Internal Mammary. Circulation. v. 107, p. 769-776
2003.
CAMPBELL, W. B.; GEBREMEDHIN, D.; PRAIT, P. F.; HERDER, D. R. Identification
of epoxyeicosatrienoic acids as endothelium-derived hyperpolarizing factors. Circ.
Res., v. 78, p. 415-423, 1996.
CASTRO, H. G.; OLIVEIRA, L. O.; BARBOSA, L. C. A.; SILVA, D. J. H.;
NASCIMENTO, E. A.; Teor e Composição do Óleo Essencial de Cinco Acessos de
Mentrasto. Quim. Nova., v. 27 (1), p. 55-57, 2004.
CAULFIELD, M. P.; BIRDSALL, N. J. International Union of Pharmacology. XVII.
Classification of muscarinic acetylcholine receptors. Pharmacol. Rev., 1998; 50: (2)
279–90.
CAVALCANTE, H. M.; RIBEIRO, T. P.; SILVA, D. F.; NUNES, X. P.; BARBOSA-
FILHO, J. M.; DINIZ, M. F.; CORREIA, N. A.; BRAGA, V. A.; MEDEIROS, I. A.;
Cardiovascular Effects Elicited by Milonine, a New 8,14-Dihydromorphinandienone
Alkaloid. Basic Clin. Pharmacol. Toxicol., v.108(2), p.122-30, 2011. doi:
10.1111/j.1742-7843.2010.00631.x..

127
CHANG, H. R.; LEE, R. P.; WU, C. Y.; CHEN, H. I. Nitric oxide in mesenteric
vascular reactivity: a comparison between rats with normotension and hypertension.
Clin. Exp. Pharmacol. Physiol., v.29 (4), p.275-80, 2002.
CHANG, T. J.; CHEN, W. P.; YANG, C.; LU, P. H.; LIANG, Y. C.; SU, M. J.; LEE, S.
C.; CHUANG, L. M.; Serine-385 phosphorylation of inwardly rectifying K+ channel
subunit (Kir6.2) by AMP-dependent protein kinase plays a key role in rosiglitazone-
induced closure of the K(ATP) channel and insulin secretion in rats. Diabetologia.
v.52 (6), p.1112-21, 2009.
CHARKOUDIAN, N.; RABBITTS, J. A. Sympathetic neural mechanisms in human
cardiovascular health and disease. Mayo Clin. Proc., v.84: (9), p.822-30, 2009.
CHIOU, W. F.; CHANG, P. C.; CHOU, C. J.; CHEN, C. F.; Protein constituent
contributes to the hypotensive and vasorelaxant activities of Cordyceps sinensis. Life
Sci., v.66, p.1369—1376, 2000.
CHOWDHARY, S; TOWNEND, J. N. Role of nitric oxide in the regulation of
cardiovascular autonomic control. Clin. Sci., v.97, p.5–17, 1999.
CLAPHAM, D. E.; JULIUS, D.; MONTELL, C.; SCHULTZ, G. International Union of
Pharmacology. XLIX. Nomenclature and Structure-Function Relationships of
Transient Receptor Potential Channels. Pharmacol. Rev., v. 57, p. 427 - 450, 2005.
COLOMBO, S. L.; MONCADA, S. AMPKalpha1 regulates the antioxidant status of
vascular endothelial cells. Biochem. J., v. 26; 421(2), p.163-9, 2009.
CONTRERAS, C.; SÁNCHEZ, A; GARCÍA-SACRISTÁN, A.; MARTÍNEZ, M. C.;
ANDRIANTSITOHAINA, R.; PRIETO, D. Preserved insulin vasorelaxation and up-
regulation of the Akt/eNOS pathway in coronary arteries from insulin resistant obese
Zucker rats. Atherosclerosis., v.217(2), p.331-9, 2011.
CORDELLINI, S.; NOVO, R.; LANZA JÚNIOR, U. Exposure to stress differential
vascular adaptive response in spontaneously hypertensive and Wistar rats: Role of

128
nitric oxide, and prehypertensive and hypertensive states. Life Sci., v. 10; 79 (7), p.
646-53, 2006.
CORNWELL, T. L; et al. Regulation of sarcoplasmic reticulum protein
phosphorylation by localized cyclic GMP-dependente protein kinase in vascular
smooth muscle cells. Mol. Pharmacol. v. 40, p. 923-931, 1991.
COSTA, G; LABADIA, A.; TRIGUERO, D.; JIMENEZ, E.; GARCIA-PASCUAL, A.;
Nitrergic relaxation in urethral smooth muscle: involvement of potassium channels
and alternative redox forms of NO. Naun. Sch. Arch. Pharmacol., v. 364, p. 516–
523, 2001.
COWLEY A.W. J.R.; ROMAN, R.J.; KRIEGER, J.E. Pathways linking renal excretion
and arterial pressure with vascular structure and function. Clin. Exp. Pharmacol.
Physiol., v. 18(1): p. 21-7, 1991.
COWLEY, A. W. J. R. Long-term control of arterial blood pressure. Physiol. Rev.,
v.72(1), p.231-300, 1992.
COX, R. H.; Changes in the expression and function of arterial potassium channels
during hypertension. Vasc. Pharmacol., v 38, p. 13-23, 2002.
CRANE, G. J.; GALLAGHER, N.; DORA, K. A.; GARLAND, C. J. Small- and
intermediate- conductance calcium-activated K+ channels provide different facets of
endothelium-dependent hyperpolarization in rat mesenteric artery. J. Physiol., v.553,
p.183–189, 2003.
CRAVEIRO, A. A.; FERNANDES, A. G.; ANDRADE, C. H. S.; MATOS, F. J. A.;
ALENCAR J. W.; MACHADO, M. I. L. Óleos Essenciais de Plantas do Nordeste –
Fortaleza, Ed. UFC, p. 7-19. 1981.
DAL-CIM, T.; MARTINS, W. C.; SANTOS, A. R.; TASCA, C. I. Guanosine is
neuroprotective against oxygen/glucose deprivation in hippocampal slices via large
conductance Ca²+-activated K+ channels, phosphatidilinositol-3 kinase/protein

129
kinase B pathway activation and glutamate uptake. Neuroscience. V. 2;183, p.212-
20, 2011.
DAL-ROS, S.; OSWALD-MAMMOSSER, M.; PESTRIKOVA, T.; SCHOTT, C.
BOEHM, N.; BRONNER, C.; CHATAIGNEAU, T.; GÉNY, B.; SCHINI-KERTH, V. B.;
Losartan prevents portal hypertension-induced, redox-mediated endothelial
dysfunction in the mesenteric artery in rats. Gastroenterology, v.138(4), p.1574-84,
2010
DAMPNEY, R. A.; COLEMAN, M. J.; FONTES, M. A.; HIROOKA, Y.; HORIUCHI, J.;
LI, Y. W.; POLSON, J. W.; POTTS, P. D.; TAGAWA, T. Central mechanisms
underlying short- and long-term regulation of the cardiovascular system. Clin. Exp.
Pharmacol. Physiol., v.29(4), p.261-8, 2002.
De SOUSA, D. P.; GONÇALVES, J. C.; QUINTANS-JUNIOR, L.; CRUZ, J. S.;
ARAÚJO, D. A.; DE ALMEIDA R. N. Study of anticonvulsant effect of citronellol, a
monoterpene alcohol in rodents. Neurosc. Let., v.401, p. 231–235, 2006.
DORWARD, P. K.; RIEDEL, W.; BURKE, S. L.; GIPPS, J.; KORNER, P. I.; The renal
sympathetic baroreflex in the rabbit. Arterial and cardiac baroreceptor influences,
resetting, and effects of anesthesia. Circ. Res., v. 57, p. 618 - 633, 1985.
DRAB, M.; VERKADE, P.; ELGER, M.; KASPER, M.; LOHN, M.; LAUTERBACH, B.;
MENNE, J.; LINDSCHAU, C.; MENDE, F.; LUFT, F.C.; SCHEDL, A., HALLER, H.;
KURZCHALIA, T. V. Loss of caveolae, vascular dysfunction, and pulmonary defects
in caveolin-1 gene-disrupted mice. Science, v.293, p.2449–2452, 2001.
EDIRISINGHE, I.; BURTON-FREEMAN, B.; VARELIS, P.; et al. Strawberry extract
caused endothelium-dependent relaxation through the activation of PI3 kinase/Akt. J.
Agric. Food. Chem., v.56, p.9383–9390, 2008.
EDRIS, A. E.; Pharmaceutical and therapeutic potentials of essential oils and their
individual volatile constituents: a review. Phytother. Res., v.21, p. 308-323, 2007.

130
EDWARDS, G.; DORA, K. A.; GARDENER, M. J.; GARLAND, C. J.; WESTON, A.
H.; K+ is an endothelium-derived hyperpolarizing factor in rat arteries. Nature, v.396,
p. 269–272. 1998.
EDWARDS, G.; FÉLÉTOU, M.; WESTON, A. H., Endothelium-derived
hyperpolarising factors and associated pathways: a synopsis. Pflugers Arch.,
v.459(6), p. 63-79, 2010.
FAROUQUE, H. M.; OMAR, A. N. D.; MEREDITH, T. I.; Relative contribution of
vasodilator prostanoids, NO, and KATP channels to human forearm metabolic
vasodilation. Am. J. Physiol. Heart. Circ. Physiol. v. 284, p. H2405–H2411, 2003.
FEIG, P. U.; ROY, S.; CODY, R. J. Antihypertensive drug development: current
challenges and future opportunities. J. Am. Soc. Hypertens., v.4(4), p.163-73, 2010.
FEITOSA, E. M. A.; ARRIAGA, A. M. C.; SANTIAGO, G. M. P.; LEMOS, T. L. G.;
OLIVEIRA, M. C. F.; VASCONCELOS, J. N.; LIMA, J. Q.; et. al. Chemical
Composition and Larvicidal Activity of Rollinia leptopetala (Annonaceae) J. Braz.
Chem. Soc., v.20: (2), p. 375-378, 2009.
FÉLÉTOU, M.; KÖHLER, R.; VANHOUTTE, P. M. Nitric oxide: Orchestrator of
endothelium-dependent responses. Ann. Med., 2011. [in press];
doi:10.3109/07853890.2011.585658.
FÉLÉTOU, M.; KÖHLER, R.; VANHOUTTE, P. M., Endothelium-derived vasoactive
factors and hypertension: possible roles in pathogenesis and as treatment targets.
Curr. Hypertens. Rep., v.12(4), p. 267-75, 2010.
FÉLÉTOU, M.; VANHOUTTE, P. M. Endothelium-dependent hyperpolarization of
vascular smooth muscle cells. Acta Pharmacol. Sin., v.21(1), p.1-18, 2000.
FÉLÉTOU, M.; VANHOUTTE, P.M. Endothelial dysfunction: a multifaceted disorder,
Am. J. Physiol., Heart Circ. Physiol. v.291, p. H985–H1002, 2006.

131
FERREIRA-DA-SILVA, F. W.; BARBOSA, R. et al. Effects of 1,8-cineole on
electrophysiological parameters of neurons of the rat superior cervical ganglion. Clin.
Exp. Pharmacol. Physiol., v.36, p.1068–1073, 2009.
FILHO, Y. C.; YUNES, R. A.; Estratégias para obtenção de compostos
farmacologicamente ativos a partir de plantas medicinais. Conceitos sobre
modificação estrutural para otimização da atividade. Quím. nova, v. 21(1), p.99-105,
1998.
FISSLTHALER, B.; FLEMING, I. Activation and signaling by the AMP-activated
protein kinase in endothelial cells. Circ. Res., v.17;105(2), p.114-27, 2009.
FISSLTHALER, B.; FLEMING, I.; KESERU, B.; WALSH, K.; BUSSE, R., Fluid shear
stress and NO decrease the activity of the hydroxy-methylglutaryl coenzyme A
reductase in endothelial cells via the AMP activated protein kinase and FoxO1. Circ.
Res., v.100, p. e12–e21, 2007.
FLEMING I, FISSLTHALER B, DIMMELER S, KEMP BE, BUSSE R. Phosphorylation
of Thr(495) regulates Ca(2+)/calmodulin-dependent endothelial nitric oxide synthase
activity. Circ. Res., v.8;88(11), p.E68-75, 2001.
FLEMING I. Molecular mechanisms underlying the activation of eNOS. Pflugers
Arch., v.459, p.793–806, 2010.
FLEMING, I.; BUSSE, R.; NO: primary EDRF. J. Mol. Cell. Cardiol., v. 31, p. 5-14,
1999(a).
FLEMING, I.; BUSSE, R.; Signal transduction of eNOS activation ―Review;‖ Cardiov.
Res., v. 43, p. 532– 541, 1999(b).
FLUCKIGER J.P., SONNAY M., BOILLAT N.; ATKINSON J. Attenuation of the
baroreceptor reflex by general anesthetic agent in the normotensive rat. Eur. J.
Pharmacol., 109 : 105 - 109, 1985.

132
FOLKOW B. Physiological aspects of primary hypertension. Physiol. Rev., v. 62, p.
347-504, 1982.
FÖRSTERMANN, U., SESSA, W. C. Nitric oxide synthases: regulation and function.
Eur. Heart J., 2011. doi:10.1093/eurheartj/ehr304
FOZARD, J. R.; MANLEY, P. W.; Potassium Channel Openers. Prog. Respir. Res.
Basel. Karger., v. 31, p. 77-80, 2001.
FULTON, D.; GRATTON, J. P.; MCCABE, T. J.; FONTANA, J.; FUJIO, Y.; WALSH,
K.; FRANKE, T. F.; PAPAPETROPOULOS, A.; SESSA, W. C. Regulation of
endothelium-derived nitric oxide production by the protein kinase Akt. Nature, v.399,
p.597–601, 1999.
FURCHGOTT, F. F. ZAWADZKI, J. V., The obligatory role of endothelial cells in the
relaxation of arterial smooth muscle by acetylcholine. Nature. v. 288, p. 373-376,
1980.
FURCHGOTT, R. F. Role of the endothelium in responses of vascular smoth
muscles. Cir. Res., v.53, p. 557-573, 1983.
GARCÍA, D. A.; VENDRELL, I.; GALOFRÉ, M.; SUÑOL, C. Gaba released from
cultured cortical neurons influences the modulation of t-[(35)S]
butylbicyclophosporothianate binding at the GABAA receptor effect of thymol. Eur. J.
Phamacol., v.600: (1-3), p. 26-31, 2008.
GARCIA, R.; ALVES, E. S. S.; SANTOS, M. P.; AQUIJE, G. M. F. V.; FERNANDES,
A. A. R.; SANTOS, R. B.; VENTURA, J. A.; FERNANDES, P. M. B. Antimicrobial
activity and potential use of monoterpenes as tropical fruits preservatives. Braz. J.
Microbiol., v.39, p.163-168, 2008b.
GARCÝA-CARDENA, G.; FAN, R.; SHAH, V. l.; Dynamic activation of endothelial
nitric oxide synthase by Hsp90. Nature v. 292, p. 821– 824, 1998.

133
GARLAND, C. J.; Compromised vascular endothelial cell SK(Ca) activity: a
fundamental aspect of hypertension? Br. J. Pharmacol., v.160(4), p.833-5, 2010.
GARTHWAITE, J.; SOUTHAM, E.; BOULTON, C.L.; NIELSEN, E. B.; SCHMIDT, K.;
MAYER, B. Potent and selective inhibition of nitric oxide-sensitive guanylyl cyclase
by 1H-[1,2,4]oxadiazolo[4,3-a]quinoxalin-1-one. Mol. Pharmacol., 1995; 48: 184-
188.
GEWALTIG, M. T.; KOJDA, G.; Vasoprotection by nitric oxide: mechanisms and
therapeutic potencial. Cardiovasc. Res., v. 55, p. 250-60, 2002.
GIACHINI, F. R.; CARNEIRO, F. S.; LIMA, V. V.; CARNEIRO, Z. N.; DORRANCE,
A.; WEBB, R. C.; TOSTES, R. C. Upregulation of intermediate calcium-activated
potassium channels counterbalance the impaired endothelium-dependent
vasodilation in stroke-prone spontaneously hypertensive rats. Transl. Res., v.154(4),
p.183-93, 2009.
GONÇALVES, J. C. R.; OLIVEIRA, F. S.; BENEDITO, R. B.; DE SOUSA, D. P.;
ALMEIDA, R. N.; ARAÚJO, D. A. M. Antinociceptive activity of (−)-carvone: evidence
of association with decreased peripheral nerve excitability. Biol. Pharm. Bull., v. 31,
p.1017–1020, 2008.
GOTTLIEB, O. R.; KAPLAN, M. A. C. Amazônia: Tesouro químico a preservar.
Ciência Hoje., 11 (61): 17-20, 1990.
GONZÁLEZ-SÁNCHEZ, J. L.; SERRANO-RÍOS, M. Molecular basis of insulin action.
Drug News Perspect. v.20 (8), p.527-31, 2007.
GRASSMANN, J.; HIPPELI, S.; SPITZENBERGER, R.; ELSTNER, E. F.; The
monoterpene terpinolene from the oil of Pinus mugo L. in concert with alpha-
tocopherol and beta-carotene effectively prevents oxidation of LDL. Phytomedicine,
V. 12(6-7), p. 416-23 2005(b).

134
GRASSMANN, J.; Terpenoids as Plant Antioxidants. Vitam. Horm., 72: 505-535,
2005.
GRATTON, J.P.; FONTANA, J.; O’CONNOR, D. S.; GARCIA-CARDENA, G.;
MCCABE, T. J.; SESSA, W. C. Reconstitution of an endothelial nitric-oxide synthase
(eNOS), hsp90, and caveolin-1 complex in vitro. Evidence that hsp90 facilitates
calmodulin stimulated displacement of eNOS from caveolin-1. J. Biol. Chem., v.275,
p.22268–22272, 2000.
GRUNFELD, S.; HAMILTON, C. A.; MESAROS, S.; MCCLAIN, S. W.; DOMINICZAK,
A. F.; BOHR, D. F.; MALINSKI, T. Role of superoxide in the depressed nitric oxide
production by endothelium of genetically hypertensive rats. Hypertension, v. 26(Part
1): p. 854–857, 1995.
GUEDES, D. N.; SILVA, D. F.; BARBOSA-FILHO, J. M.; MEDEIROS, I. A. Calcium
antagonism and the vasorelaxation of the rat aorta induced by rotundifolone. Braz. J.
Med. Biol. Res., v. 37(12), p.1881-7, 2004.
GUEDES, D. N.; SILVA, D. F.; BARBOSA-FILHO, J. M.; MEDEIROS, I. A.
Muscarinic agonist properties involved in the hypotensive and vasorelaxing
responses of rotundifolone in rats. Planta Med., v. 68: p. 700-704, 2002.
GUYTON, A. C. The relationship of cardiac output and arterial pressure control.
Circulation. Review.; v. 64(6), p.1079-88, 1981.
HABA, M.; HATAKEYAMA, N.; KINOSHITA, H.; TERAMAE, H.; AZMA, T.; HATANO,
Y.; MATSUDA, N.; The modulation of vascular ATP-sensitive K+ channel function via
the phosphatidylinositol 3-kinase-Akt pathway activated by phenylephrine. J.
Pharmacol. Exp. Ther., v. 334(2), p.673-8, 2010.
HADDY, F. J.; VANHOUTTE, P. M.; FELETOU, M.; Role of potassium in regulating
blood flow and blood pressure Am. J. Physiol. Regul. Integr. Comp. Physiol., v.
290, p. R546–R552, 2006.

135
HALL, J. E. Control of blood pressure by the renin-angiotensin-aldosterone system.
Clin Cardiol., v.14(8 Suppl 4), p.IV6-21; discussion IV51-5, 1991.
HECK, D. E.; LASKIN, D. L.; GARDNER, C. R.; LASKIN, J. D.; Epidermal growth
factor suppresses nitric oxide and hydrogen peroxide production by keratinocytes.
Potential role for nitric oxide in the regulation of wound healing, J. Biol. Chem., v.
267, p. 21277–21280, 1992.
HECKER, M.; MULSCH, A.; BASSENGE, E.; FORSTERMANN, U.; BUSSE, R.;
Subcellular localization and characterization of nitric oxide synthase(s) in endothelial
cells: physiological implications. Biochem. J., v. 299, p. 247-252, 1994.
HEO, K. S.; FUJIWARA, K.; ABE, J. Disturbed-flow-mediated vascular reactive
oxygen species induce endothelial dysfunction. Circ. J., v.25;75(12), p.2722-30,
2011.
INOUE, R.; JENSEN, L. J.; SHI, J.; MORITA, H.; NISHIDA, M.; HONDA, A.; ITO, Y.
Transient receptor potential channels in cardiovascular function and disease. Circ.
Res., 99:119 –131, 2006.
IRVINE, J. C.; FAVALORO, J. L.; KEMP-HARPER, B. H.; Resistance Arteries
Channels to Vasodilate Activates Soluble Guanylate Cyclase and K+ - NO
Hypertension v. 41, p. 1301-1307, 2003.
ISENOVIĆ, E.; SOSKIĆ, S.; DÜNGEN, H. D.; DOBUTOVIC, B.; ELVIS, T.; SIMONE,
I.; MARCHE, P. Regulation of endothelial nitric oxide synthase in pathophysiological
conditions. Cardiovasc. Hematol. Disord. Drug. Targets., [in press]. 2011.
INTERAMINENSE, L. D. E. F., DE SIQUEIRA, R. J., XAVIER, F. E., DUARTE, G. P.,
MAGALHÃES, P. J,, DA SILVA, J. K., et al. Cardiovascular effects of 1-nitro-2-
phenylethane, the main constituent of the essential oil of Aniba canelilla, in
spontaneously hypertensive rats. Fundam. Clin. Pharmacol., v,25(6), p. 661-9,
2011. doi: 10.1111/j.1472-8206.2010.00891.x.

136
IUPHAR - INTERNATIONAL UNION OF PHARMACOLOGY. Ion Channel
Compendium: potassium channels. International Union of Pharmacology [www.
iuphar. org], 2002.
JACKSON, W. F. Ion channel and vascular tone. Hypertension. v.35, p.173 -178,
2000.
JACKSON, W. F.; Potassium channels in the peripheral microcirculation.
Microcirculation. V.12(1), p.113-27, 2005.
JIN X, SATOH-OTONASHI Y, ZAMAMI Y, TAKATORI S, HASHIKAWA-HOBARA N,
KITAMURA Y, KAWASAKI H. New molecular mechanisms for cardiovascular
disease: contribution of endothelium-derived hyperpolarizing factor in the regulation
of vasoconstriction in peripheral resistance arteries. J. Pharmacol. Sci., v.116 (4), p.
332-6, 2011.
JIRTLE, R. L.; Increased mannose 6-phosphate (insuline-like growth factor II
receptor and transforming grown factor beta 1 levels during monoterpene – induced
regression of mammary tumors. Cancer. Res., v. 53, p. 3849 – 3852, 1993.
JUERGENS, U. R.; DETHLEFSEN, U.; STEINKAMP, G.; GILLISSEN, A.; REPGES,
R.; VETTER, H. Anti-inflammatory activity of 1,8-cineol (eucalyptol) in bronchial
asthma: A double-blind placebo-controlled trial. Respir. Med., V.97, p. 250–6, 2003.
JULIUS, S.; Blood Pressure Lowering Only or More? Has the Jury Reached Its
Verdict? Am. J. Cardiol., v.100, p.32J-32J, 2007.
KAGIYAMA, S.; TSUCHIHASHI, T.; ABE, I.; FUJISHIMA, M. Enhanced depressor
response to nitric oxide in the rostral ventrolateral medulla of spontaneously
hypertensive rats. Hypertension. V.31(4), p.1030-4, 1998.
KANG, D. G.; LEE, K. J.; CHOI, D. H.; SOHN, E. J.; MOON, M. K.; LEE, H. S.
Vascular Relaxation by the Methanol Extract of Sorbus Cortex via NO-cGMP
Pathway. Biol. Pharm. Bull., v.28: (5), p. 860—864, 2005.

137
KARLBERG, B. E.; Cough and inhibition of the renin-angiotensin system. J.
Hypertension., v. 11 (Suppl 3) p. 49-52, 1993.
KASS, D. A.; CHAMPION, H. C.; BEAVO, J. A. Phosphodiesterase type 5: expanding
roles in cardiovascular regulation. Circ. Res., v.101, p.1084–1095, 2007,
KELEN, M.; TEPE, B. Chemical composition, antioxidant and antimicrobial properties
of the essential oils of three Salvia species from Turkish flora. Bioresour. Technol.,
V.99, p.4096–104, 2008.
KELM, M.; The L-arginine-nitric oxide pathway in hypertension, Curr. Hypertens.
Rep., v. 5, p. 80–86, 2003.
KEVIN, S. T.; NELSON, M. T. Ion channels in smooth muscle: regulators of
intracellular calcium and contractility. Can. J. Pharmacol., v.83, p.215 - 242, 2005.
KIRCHHEIM HR: Systemic arterial baroreceptor reflexes. Physiol. Rev. v. 56, p.100-
77, 1976.
KIM, J; MARSHALL, M. R; WEI, C. Antibacterial Activity of Some Essential Oil
Components against Five Foodborne Pathogens? J. Agric. Food Chem., v.43, p.
2839-2845, 1995.
KISHI, T.; HIROOKA, Y.; KIMURA, Y.; SAKAI, K.; ITO, K.; SHIMOKAWA, H.;
TAKESHITA, A. Overexpression of eNOS in RVLM improves impaired baroreflex
control of heart rate in SHRSP. Hypertension. V.41, p.255–260, 2003.
KISHI, T.; HIROOKA, Y.; SAKAI, K.; SHIGEMATSU, H.; SHIMOKAWA, H.;
TAKESHITA, A. Overexpression of eNOS in the RVLM causes hypotension and
bradicardia via GABA release. Hypertension. v.38, p. 896 –901, 2001.
KOJIMA, H. NAKATSUBO, N.; KIKUCHI, K.; KAWAHARA, S.; KIRINO, Y.;
NAGOSHI, H.; HIRATA, Y.; NAGANO, T. Detection and imaging of nitric oxide with

138
novel fluorescent indicators: diaminofluoresceins. Anal. Chem., v. 70, p. 2446–2453,
1998.
KOLLURU, G. K.; SIAMWALA, J. H.; CHATTERJEE, S. eNOS phosphorylation in
health and disease. Biochimie, v. 92 (9), p.1186-98, 2010.
KRUSZYNA, H.; MAGYAR, J. S.; ROCHELLE, L. G.; RUSSEL, M. A.; SMITH, R. P.
E.; WILCOX, D. E. Spectroscopic Studies of Nitric Oxide (NO) Interations with
Cobalamins: Reaction of NO with Supéroxocobalamin(III) Likely Accounts for
Cobalamin Reversal of the Biological Effects of NO. J. Phamacol. Exp. Ther., v.285:
(2), p.665-671, 1998.
LAHLOU, S.; LEAL-CARDOSO, J. H.; MAGALHÃES, P. J. Essential oil of Croton
nepetaefolius decreases blood pressure through an action upon vascular smooth
muscle: studies in DOCA-salt hypertensive rats. Planta Med., v. 66, p. 138-143,
2000.
LEVINE, Y. C.; LI, G. K.; MICHEL, T. Agonist-modulated regulation of AMP-activated
protein kinase (AMPK) in endothelial cells. Evidence for an AMPK -> Rac1 -> Akt ->
endothelial nitric-oxide synthase pathway. J. Biol. Chem., v. 13; 282 (28), p. 20351-
64, 2007.
LI, C.; RUAN, L.; SOOD, S. G.; PAPAPETROPOULOS, A.; FULTON, D.; VENEMA,
R. C. Role of eNOS phosphorylation at Ser-116 in regulation of eNOS activity in
endothelial cells. Vasc. Pharmacol., v. 47, p. 257–264, 2007.
LIN, M. I.; FULTON, D.; BABBITT, R.; FLEMING, I.; BUSSE, R.; PRITCHARD, K. A.
J. R.; SESSA, W. C. Phosphorylation of threonine 497 in endothelial nitric-oxide
synthase coordinates the coupling of L-arginine metabolism to efficient nitric oxide
production. J. Biol. Chem., v.278, p.44719–44726, 2003.
LIP, G. Y. H.; Target organ damage and the prothrombotic state in hypertension.
Hypertension v. 36, p. 975-77, 2000.

139
LORENZ, M.; WESSLER, S.; FOLLMANN, E., et al A constituent of green tea,
epigallocatechin-3-gallate, activates endothelial nitric oxide synthase by a
phosphatidylinositol-3-OH-kinase-, cAMPdependent protein kinase-, and Akt-
dependent pathway and leads to endothelial-dependent vasorelaxation. J. Biol.
Chem., v. 279, p. 6190–6195, 2004.
LUCIANO, M. N.; RIBEIRO, T. P.; DE FRANÇA-SILVA, M. D.; DO NASCIMENTO,
R. J.; OLIVEIRA, E. J.; FRANÇA, K. C.; ANTUNES, A. A.; NAKAO, L. S.; AITA, C. A.;
BRAGA, V. A.; DE MEDEIROS, I. A. Uncovering the vasorelaxant effect induced by
Vale do São Francisco red wine: A role for nitric oxide. J. Cardiovasc. Pharmacol.,
2011 Mar 9. doi: 10.1097/FJC.0b013e318217db1f.
MAGALHÃES, P. J. C.; LAHLOU, S.; JUCA, D. M.; COELHO-DE-SOUZA, L. N.;
FROTA, P. T. T.; COSTA, A. M. G.; LEAL-CARDOSO, J. H. Vasorelaxation induced
by the essential oil of Croton nepetaefolius and its constituents in rat aorta are
partially mediated by the endothelium. Fund. Clin. Pharmacol., V.22, p.169–177,
2008.
MAGALHÃES, P.J.C.; CRIDDLE, D. N.; TAVARES, R. A.; MELO, E. M.; MOTA, T.L.;
LEAL-CARDOSO, J. H. Intestinal myorelaxant and anti-spasmodic effects of the
essential oil of Croton nepetaefolius, and its constituents cineole, methyl-eugenol and
terpineol. Phytother. Res., v.12, p.172–177, 1998.
MARC ,Y.; LLORENS-CORTES, C.; The role of the brain renin-angiotensin system in
hypertension: implications for new treatment. Prog. Neurobiol., v. 95(2), p.89-103.
2011.
MENEZES, I. A. C.; BARRETO, C. M. N.; ANTONIOLLI, A. R.; SANTOS, M. R. V.;
DE SOUSA, D. P. Hypotensive activity of terpenes found in essential oils. J.
Bioscience, v. 65, p. 562-566, 2010.
MICHEL, T.; VANHOUTTE, P. M. Cellular signaling and NO production. Pflugers.
Arch., v. 459(6), p.807-16, 2010.

140
MICHELL, B. J.; GRIFFITHS, J. E.; MITCHELHILL, K. I. et al., The Akt kinase signals
directly to endothelial nitric oxide synthase. Curr. Biol., v.9, p.845–848,1999.
MISTRY, D. I.; GARLAND, C. J. Nitric oxide (NO)-induced activation of large
conductance Ca2+ -dependent K+ channels (BKCa) in smooth muscle cells isolated
from the rat mesenteric artery. Br. J. Pharmacol., v.124, p. 1131–1140, 1998.
MONCADA, S. et al. Endothelium-derivated relaxing factor identification as nitric
oxide and role in the control of vascular tone and platelet function. Biochem.
Pharmacol., v.37, p. 2495-501,1988.
MONCADA, S. HIGGS, E. A. The L-arginine - nitric oxide pathway. N. Engl. J. Med.,
V. 29, p. 2002 – 2012, 1993.
MONCADA, S.; PALMER, R.; HIGGS, E. A. Nitric oxide: physiology,
pathophysiology, and pharmacology (Review). Pharmacol. Rev., v.43, p. 109–142,
1991.
MOREIRA, M. R; CRUZ, G. M. P; LOPES, M. S; ALBUQUERQUE, A. A. C; LEAL-
CARDOSO, J. H. Effects of terpineol on the compound action potential of the rat
sciatic nerve. Braz. J. Med. Biol. Res., v.34, p. 1337-1340, 2001.
NAKAGAWA, T.; JOHNSON, R. J. Endothelial nitric oxide synthase. Contrib.
Nephrol., v. 170, p. 93-101, 2011.
NAKATSUBOA, N.; KOJIMAA, H.; KAZUYA, K.; NAGOSHIB, H.; HIRATAB, Y.;
MAEDAA, D.; IMAIA, Y.; IRIMURAA, T.; NAGANOA, T. Direct evidence of nitric oxide
production from bovine aortic endothelial cells using new fluorescence indicators:
diaminofluoresceins. FEBS Lett., v.427, p. 263-266, 1998.
NAVARRO-ANTOLIN J, LAMAS S. Nitrosative stress by cyclosporine A in the
endothelium: studies with the NO-sensitive probe diaminofluorescein-2/diacetate
using flow cytometry. Nephrol. Dial. Transplant., v.16: (Suppl. 1), p. 6–9, 2001;

141
NELSON MT, QUAYLE JM. Physiological roles and properties of potassium channels
in arterial smooth muscle. Am. J. Physiol. v.268, p. C799–C822, 1995;
OHTA H, TALMAN WT. Alteration of baroreceptor and chemoreceptor reflexes in
spontaneously hypertensive rats. Clin. Exp. Pharmacol. Physiol. v.22: p. S60–S61,
1995.
OLIVEIRA EJ, MEDEIROS IA, MUKHERJEE R, Hypotensive and spasmolytic effects
of normacusine B from Strychnos atlantica roots. Phytomed., 3: (1) 45–49, 1996.
OSBORN JW, JACOB F, GUZMAN P. A neural set point for the long-term control of
arterial pressure: beyond the arterial baroreceptor reflex. Am. J. Physiol. Regul.
Integr. Comp. Physiol., v. 288 (4), p.R846-55, 2005.
PAGE, C.P.; CYRTIS, M.J.C.; SUTTIER, M.C.; WALKER, M.J.A. & HOFFAMANN,
B.B. As drogas e o sistema cardiovascular. Farmacologia Integrada. 1ª ed.editora
Manole, São Paulo-SP, 153-193, 1999.
PAPAPETROPOULOS, A.; GARCIA-CARDENA, G.; MADRI, J. A.; SESSA, W. C.;
Nitric oxide production contributes to the angiogenic properties of vascular
endothelial growth factor in human endothelial cells, J. Clin. Invest., V. 100, p.
3131–3139, 1997
PARNAS, M.; PETERS, M.; DADON, D.; LEV, S.; VERTKIN, I.; SLUTSKY, I.;
MINKE, B. Carvacrol is a novel inhibitor of Drosophila TRPL and mammalian TRPM7
channels. Cell Calcium, v.45, p. 300–309, 2009.
PAULIS, L,; UNGER, T. Novel therapeutic targets for hypertension. Nat. Rev.
Cardiol., v.7(8), p.431-41, 2010.
POLLMAN, M. J.; YAMADA, T.; HORIUCHI, M.; GIBBONS, G. H.; Vasoactive
substances regulate vascular smooth muscle cell apoptosis. Countervailing
influences of nitric oxide and angiotensin II. Circ. Res., 79(4): 748-56, 1996. 155-69,
2000.

142
PONCE-MONTER H, CAMPOS MG, PÉREZ S, PÉREZ C, ZAVALA M, MACÍAS A,
OROPEZA M, CÁRDENAS N. Chemical composition and antispasmodic effect of
Casimiroa pringlei essential oil on rat uterus Fitoterapia., 2008; 76: (6) 446-450.
PORTO DL, SILVA DF, DIAS KLG, CORREIA NA, DE SOUSA DP, MEDEIROS IA,
GUEDES, D. N. Evaluation of the vasorelaxant activity induced by α-terpineol and
analogous. In: 38º Congresso Brasileiro de Farmacologia e Terapêutica
Experimental, 2006, Ribeirão Preto, São Paulo, Brasil.
PRESTA, A.; LIU, J.; SESSA, W. C.; STUEHR, D. J.; Substrate binding and
calmodulin binding to endothelial nitric oxide synthase coregulate its enzymatic
activity. Nitric Oxide, v.1, p. 74–87, 1997.
PRITCHARD, K. A. J. R.; ACKERMAN, A. W.; GROSS, E. R.; STEPP, D. W.; SHI,
Y.; FONTANA, J. T.; BAKER, J. E.; SESSA, W. C. Heat shock protein 90 mediates
the balance of nitric oxide and superoxide anion from endothelial nitric-oxide
synthase. J. Biol. Chem., v.276, p.17621–17624, 2001.
PRIVIERO FB, WEBB RC. Heme-dependent and independent soluble guanylate
cyclase activators and vasodilation. J. Cardiovasc. Pharmacol., v. 56 (3): p. 229-33,
2010.
RADOMSKI, M. W.; PALMER, R. M. J.; MONCADA, S.; Endogenous nitric oxide
inhibits human platelet adhesion to vascular endothelium. Lancet., v. 2, p.1057-
1058, 1987.
RAFIKOV, R.; FONSECA, F. V.; KUMAR, S.; PARDO, D.; DARRAGH, C.; ELMS, S.;
FULTON, D.; BLACK, S. M., eNOS activation and NO function: structural motifs
responsible for the posttranslational control of endothelial nitric oxide synthase
activity. J Endocrinol., v. 210(3), p.271-84, 2011
RAJAPAKSE N, MATTSON DL. Role of L-arginine in nitric oxide production in health
and hypertension Clin. Exper. Pharmacol. Physiol., v.36, p.249–255, 2009.

143
RAMLI, J.; CALDERONARTERO, P.; BLOCK, R. C.; MOUSA, S. A. Novel
therapeutic targets for preserving a healthy endothelium: strategies for reducing the
risk of vascular and cardiovascular disease. Cardiol. J., v. 18(4), p.352-63, 2011.
RATH, G., DESSY, C., FERON, O. Caveolae, caveolin and control of vascular tone:
nitric oxide (NO) and endothelium derived hyperpolarizing factor (EDHF) regulation.
J. Physiol. Pharmacol., V.60 Suppl 4, p.105-9, 2009.
RIBEIRO, T. P. Estudo da atividade cardiovascular do α-terpineol em ratos –
Abordagens in vivo e in vitro. Dissertação (Mestrado: área Farmacologia) –
Programa de Pós-Graduação em Produtos Naturais e Sintéticos Bioativos/
Universidade Federal da Paraíba, Thaís Porto Ribeiro - João Pessoa, 2008.
RIBEIRO, T.P.; PORTO, D.L.; MENEZES, C. P.; ANTUNES, A. A.; SILVA, D. F.; DE
SOUSA D. P. et al., Unraveling the cardiovascular effects induced by alpha-terpineol:
a role for the NO-cGMP pathway. Clin. Exp. Pharmacol. Physiol., v.37(8), p. 811-6,
2010. doi: 10.1111/j.1440-1681.2010.05383.x.
RUBANYI, G.M., The discovery of endothelin: the power of bioassay and the role of
serendipity in the discovery of endothelium-derived vasocative substances.
Pharmacol. Res., V.63(6), p. 448-54, 2011.
RUSSIN, W. A.; et al. Inhibition of rat mammary, carcinogenesis by
monoterpenenoids. Carcinogenesis, v. 10, p. 2161-2164, 1989.
SAITO, K. et al. The biological properties of monoterpenes hypotensive effects on
rats and antifungal activites on plant pathogenic fungi of monoterpenes. Mokuzai
Gakaishi., v.42: (7), p. 677-680, 1996.
SANTOS, M. R. V.; CARVALHO, A. A.; MEDEIROS, I. A.; ALVES, P. B.;
MARCHIORO, M.; ANTONIOLLI, A. R. Cardiovascular effects of Hyptis fruticosa
essential oil in rats. Fitoterapia. v.78 (3), p201, 2007.

144
SANTOS, M. R. V.; MOREIRA, F. V.; FRAGA, B. P.; DE SOUSA, D. P.;
BONJARDIM, L. R.; QUINTANS-JUNIOR, J. L. Cardiovascular effects of
monoterpenes: a review. Braz. J. Pharmacog., v. 21(4): p. 764-771, 2011
SCHIFFRIN, E. L.; DENG, L. Y.; LAROCHELLE, P.; Effects of a -blocker or a
converting enzyme inhibitor on resistante arteries in essential hypertension.
Hypertension, v. 23, p. 83-91, 1994.
SCHINI-KERTH V. B.; VANHOUTTE P. M.; Nitric oxide synthases in vascular cells
(review) Exper. Physiol., v. 80, p. 885- 905, 1995
SCHINI-KERTH VB, AUGER C, ETIENNE-SELLOUM N, CHATAIGNEAU T.
Polyphenol-induced endothelium-dependent relaxations role of NO and EDHF. Adv.
Pharmacol., v.60, p.133-75, 2010.
SCHINI-KERTH VB, ETIENNE-SELLOUM N, CHATAIGNEAU T, AUGER C.
Vascular protection by natural product-derived polyphenols: in vitro and in vivo
evidence. Planta Med., V. 77(11), p.1161-7, 2011.
SCHINI-KERTH, V. B.; FISSLTHALER, B.; BUSSE, R.; CGRP enhances induction of
nitric oxide synthase in vascular smooth muscle cells via a cAMP-dependent
mechanism. Am. J. Physiol., v. 267, p. H2483 2490. 1994.
SCHNEIDER, J. C. E. L.; KEBIR, D.; CHÉREAU, C.; LANONE, S.; HUANG, X. L.; De
BUYS-ROESSINGH, A. S.; MERCIER, J. C.; DALL'AVA-SANTUCCI, J.; DINH-
XUAN, A. T. Involvement of Ca2+/calmodulin-dependent protein kinase II in
endothelial NO production and endothelium-dependent relaxation. Am. J. Physiol.
Heart. Circ. Physiol., V.284(6) p.H2311-9, 2003.
SERBAN, D. N.; NILIUS, B.; VANHOUTTE, P. M. The endothelial saga: the past, the
present, the future. Pflugers Arch., v.;459(6), p.787-92, 2010.
SESSA, W. C.; HARRISON, J. K.; BARBER, C. M.; ZENG, D.; DURIEUX, M. E.;
D'ANGELO, D. D.; LYNCH, K. R.; PEACH, M. J.; Molecular cloning and expression

145
of a cDNA encoding endothelial cell nitric oxide synthase. J. Biol. Chem., v. 267, p.
15274- 15276. 1992
SHAH, D. I.; SINGH, M. Activation of protein kinase A improves vascular endothelial
dysfunction. Endothelium, V.13(4), p.267-77, 2006.
SHIEH, C. C.; COGHLAN, M.; SULLIVAN, J. P.; GOPALAKRISHNAN, M.; Potassium
channels: molecular defects, diseases and therapeutic opportunities. Pharmacol.
Rev.,v. 52, p. 557–593, 2000.
SINGH, P.; SHUKLA, R.; PRAKASH, B.; KUMAR, A.; SINGH, S.; MISHRA, P. K.;
DUBEY, N. K. Chemical profile, antifungal, antiaflatoxigenic and antioxidant activity
of Citrus maxima Burm. and Citrus sinensis (L.) Osbeck essential oils and their cyclic
monoterpene, DL-limonene. Food Chem. Toxicol., v.48: p.1734-1740, 2010.
SHIMADA, K.; FUKUDA, S.; MAEDA, K.; KAWASAKI, T.; KONO, Y.; JISSHO, S.;
TAGUCHI, H., et.ai. Aromatherapy alleviates endothelial dysfunction of medical staff
after night-shift work: preliminary observations Hypertens. Res., v. 34 (2), p. 264-7,
2011.
SHOROFSKY, S. R.; BALKE, W.; Calcium currents and arrythmias: Insights from
molecular biology. Am. J. Med., v. 110, p 127-140, 2001.
SOARES, M. C. M. S.; DAMIANI, C. E. N.; MOREIRA, C. M.; STEFANON, I.;
VASSALLO, D. V.; Eucalyptol, an essential oil, reduces contractile activity in rat
cardiac muscle, Braz. J. Med. Biol. Res., v. 38(3), 2005.
SOBEY, C. G.; Potassium Channel Function in Vascular Disease. Arterioscler.
Thromb. Vasc. Biol., V. 21, p. 28-38, 2001.
STAHMANN, N.; WOODS, A.; SPENGLER, K.; HESLEGRAVE, A.; BAUER, R.;
KRAUSE, S.; VIOLLET, B.; CARLING, D.; HELLER, R. Activation of AMP-activated
protein kinase by vascular endothelial growth factor mediates endothelial

146
angiogenesis independently of nitric-oxide synthase. J. Biol. Chem., v.2;285(14),
p.10638-52, 2010.
STASCH, J. P.; HOBBS, A. J. NO-independent, haem-dependent soluble guanylate
cyclase stimulators. Handb. Exp. Pharmacol., v.191, p.277–308, 2009.
STERNER O, SZALLASI A. Novel natural vanilloid receptor agonists: new
therapeutic targets for drug development. Trends Pharmacol. Sci., v.20, p. 459–
465, 1999.
SVENDSEN, A. B.; SCHEFFER, J. J. C.; Natural products in therapy: prospects, gols
and means in modern research. Pharm. Week., v. 4, p. 96-103, 1992.
TANAKA, Y.; TANG, G.; TAKIZAWA, K.; OTSUKA, K.; EGHBALI, M.; SONG, M.;
NISHIMARU, K.; et. al. Kv Channels Contribute to Nitric Oxide- and Atrial Natriuretic
Peptide-Induced Relaxation of a Rat Conduit Artery. J. Pharmacol. Exper. Ther.. V.
317, N. 1, 2006.
TAYLOR, J.G.; BISOGNANO, J. D.; Baroreflex stimulation in antihypertensive
treatment. Curr. Hypertens. Rep., v. 12(3), p.176-81, 2010.
THRASHER, T. N.; Arterial baroreceptor input contributes to long-term control of
blood pressure. Curr. Hypertens. Rep., v. 8(3), p. 249-54, 2006.
TISSARAND, R.; BALACS, T. Essential oil safety, a guide for professionals. Churchill
Livingstone, London, 1995.
TOBIN T, SWERCZEK TW, BLAKE JW. Pine oil toxicity in the horse: drug detection,
residues and pathological changes. Res. Commun. Chem. Pathol. Pharmacol.,
v.15: (2), p. 291-301, 1976.
TODA N, OKAMURA T. The pharmacology of nitric oxide in the peripheral nervous
system of bood vessels. Pharmacol. Rev., v. 55, p. 271–324, 2003.

147
TODA N. Age-related changes in endothelial function and blood flow regulation.
Pharmacol. Ther., 2011
TOMASONI, L.; SITIA, S.; BORGHI. C.; CICERO, A. F.; CECONI, C.; CECARO, F.;
MORGANTI, A.; DE GENNARO-COLONNA, V. et.al. Effects of treatment strategy on
endothelial function. Autoimmun. Rev., v.9(12), p.840-4, 2010.
TOMHS H.; Treatment of mild hypertension. Arch. Intern Med., 151, 1991.
TÖRÖK J. Participation of nitric oxide in different models of experimental
hypertension. Physiol. Res., 2008;57(6):813-25.
TRIGGLE, C.R.; DING, H., The endothelium in compliance and resistance vessels.
Front. Biosci., (Schol Ed), v.1 (3), p.730-44, 2011.
TRIGGLE, D. J.; The pharmacology of ion channel: with particular reference to
voltage-gated Ca2+ channels. Eur. J. Pharmacol., v. 375, p. 311-325, 2002.
VANHOUTTE PM, SHIMOKAWA H, TANG EH, FELETOU M. Endothelial
dysfunction and vascular disease. Acta Physiol. (Oxf) ., v.196(2), p.193-222, 2009.
VANHOUTTE PM. COX-1 and Vascular Disease. Clin. Pharmacol. Ther., 86: (2)
212–215, 2009.
VANHOUTTE, P. M. Endothelium-dependent contractions in hypertension: when
prostacyclin becomes ugly. Hypertension. 2011 Mar;57(3):526-31.
VANHOUTTE, P. M.; BOULANGER, C. M. Function the endothelium in arterial
hypertension. La Revue Du Praticieu, V.45, Issue 20,p-2513-2518, 1995.
VANHOUTTE, P. M.; FELETOU, M.; TADDEI, S.; Endothelium-dependent
contractions in hypertension. Br. J. Pharmacol., v.144, p. 449–458, 2005.
VENEMA, R. C. Post-translational mechanisms of endothelial nitric oxide synthase
regulation by bradykinin. Int. Immunopharmacol., v.2 (13-14), p.1755-62, 2002.

148
VOGT-EISELE, A. K.; WEBER, K. SHERKHELI, M. A. et al., Monoterpenoid
agonists of TRPV3. Br. J. Pharmacol., v.151, p. 530–540, 2007.
WAGNER, K. H.; ELMADFA, I. Biological relevance of terpenoids. Overview focusing
on mono-, di- and tetraterpenes. Ann. Nutr. Metab., 47:(3-4), 95-106, 2005.
WALLACE, T. C. Anthocyanins in cardiovascular disease. Adv. Nutr., (Bethesda).
v.2(1), p.1-7, 2011.
WANG X, CHU W, LAU F, VAN BREEMEN C. Bradykinin potentiates acetylcholine
induced responses in native endothelial cells from rabbit aorta. Biochem. Biophys.
Res. Commun., v.24;213(3), p.1061-7, 1995.
WANSTALL JC, HOMER KL, DOGGRELL SA., Evidence for, and importance of,
cGMP-independent mechanisms with NO and NO donors on blood vessels and
platelets. Curr. Vasc. Pharmacol., v.3: (1), p. 41-53, 2005.
WERNER ER, BLAU N, THÖNY B. Tetrahydrobiopterin: biochemistry and
pathophysiology. Biochem. J. v.15; 438(3), p.397-414, 2011.
WONG, M. S.; VANHOUTTE, P. M., COX-mediated endothelium-dependent
contractions: from the past to recent discoveries. Acta Pharmacol. Sin., V.31(9),
p.1095-102, 2010.
WOODLEY N, BARCLAY JK. Cultured endothelial cells from distinct vascular areas
show differential responses to agonists. Can. J. Physiol. Pharmacol., v.72(9), p.
1007-12, 1994.
XIE, L.; LIU, Z.; LU, H.; ZHANG, W.; MI, Q.; LI, X.; TANG, Y.; CHEN, Q.; FERRO, A.;
JI, Y. Pyridoxine ameliorates uncoupled endothelial nitric oxide synthase induced by
ox-LDL via PKCα signal pathway in human umbilical vein endothelial cells. Br. J.
Pharmacol., 2011. doi: 10.1111/j.1476-5381.2011.01607.x.

149
YANGA, Q.; YIMA, A. P.; HE, G. W.; The significance of endothelium-derived
hyperpolarizing factor in the human circulation. Curr. Vasc. Pharmacol. v. 5(1), p.
85-92, 2007.
YU, F. H.; CATTERALL, W. A.; The VGL-Chanome: A Protein Superfamily
Specialized for Electrical Signaling and Ionic Homeostasis Sci. STKE v. 15 2004.
YUAN, X. J.; TOD, M. L.; RUBIN, L. J.; BLAUSTEIN, M. P.; NO hyperpolarizes
pulmonary artery smooth muscle cells and decreases the intracellular Ca2+
concentration by activating voltage-gated K+ channels. Proc. Natl. Acad. Sci., USA.
V. 93, p. 10489 –10494, 1996.
ZHANG QJ, MCMILLIN SL, TANNER JM, PALIONYTE M, ABEL ED, SYMONS JD.
Endothelial nitric oxide synthase phosphorylation in treadmill-running mice: role of
vascular signalling kinases. J. Physiol., v. 1;587(Pt 15), p. 3911-20, 2009.
ZHOU E, QING D, LI J. Age-associated endothelial dysfunction in rat mesenteric
arteries: roles of calcium-activated K(+) channels (K(ca)). Physiol. Res., 59(4):499-
508, 2010.
ZYGMUNT, P. M.; EDWARDS, G.; WESTON, A. H.; LARSSON, B.;
HOÈGESTAÈTT, E. D.; Involvement of voltage-dependent potassium channels in the
EDHF-mediated relaxation of rat hepatic artery. Br. J. Pharmacol., v. 121(1), p. 141-
9 1997.
ZYGMUNT, P. M.; PLANE, F.; PAULSSON, M.; GARLAND, C.J.; HOÈGESTAÈTT,
E. D.; Interactions between endothelium-derived relaxing factors in the rat hepatic
artery: focus on regulation of EDHF Br. J. Pharmacol., v. 124, p. 992 -1000, 1998.

150
Anexos

151
Certificado do Comitê de ética

152
VITA
Lista de Publicações
Artigos integrantes da tese
Artigos Completos publicados.
1. Ribeiro TP, Porto, DL, Menezes, CP Antunes, AA, Silva, DF, De Sousa, DP, Nakao, LS, Braga, VA, Medeiros, I A. Unraveling the cardiovascular effects induced by alpha-terpineol: a role for the NO-cGMP pathway. 2010. Clin Exp Pharmacol Physiol; 37 (8) 811-6. doi: 10.1111/j.1440-1681.2010.05383.x.
Artigos propostos para submissão.
1. Ribeiro, Thaís P., Oliveira, A.C., França-Silva, Maria S., Mendes-Junior L G, Braga, Valdir A, Medeiros, Isac A., α-Terpineol induces endothelial function and baroreflex sensitivity improvement in spontaneously hypertensive rat. J Cardiov. Pharmacol, 2012.
2. Ribeiro, Thaís P.; Bruna P. V. Dantas; José G. F. Albuquerque; Lazare Belamelaba; Valdir A. Braga; Valérie B. Schini-Kerth, Isac A. Medeiros. Endothelial signaling mechanisms involved in vasodilation to α-terpineol in spontaneously hypertensive rats. Pharmacological Research, 2012.
Artigos publicados durante o período doutoral (2008-2012) Artigos Completos publicados.
1. Bastos, JF., Moreira, IJ., Ribeiro, TP., Medeiros, IA., Antoniolli, AR., De Sousa, DP., Santos, MR. 2010. Hypotensive and Vasorelaxant Effects of Citronellol, a Monoterpene Alcohol, in Rats. 2010. Basic Clin Pharmacol Toxicol 106 (4) 331 - 337. doi.10.1111/j.1742-7843.2009.00492.x
2. Nunes, FC.; Ribeiro, TP. ; França-Silva, MS. ; Medeiros, IA. ; Braga, VA. Superoxide scavenging in the rostral ventrolateral medulla blunts the pressor response to peripheral chemoreflex activation. 2010. Brain Research 10;1351:141-9.
3. Cavalcante, H.M., Ribeiro, T.P., Silva, D.F., Nunes, X.P., Barbosa-Filho, J.M., Diniz, M.F. Correia, NA, Braga, VA, Medeiros, IA. Cardiovascular Effects Elicited by Milonine, a New 8,14-Dihydromorphinandienone Alkaloid. 2011. Basic Clin. Pharmacol. Toxicol 108(2):122-30. doi: 10.1111/j.1742-7843.2010.00631.x..

153
4. Luciano MN, Ribeiro TP, de França-Silva MD, do Nascimento RJ, de Jesus Oliveira E, França KC, Antunes AA, Nakao LS, Aita CA, Braga VA, de Medeiros IA. Uncovering the vasorelaxant effect induced by Vale do São Francisco red wine: A role for nitric oxide. J Cardiov. Pharmacol. 2011. doi: 10.1097/FJC.0b013e318217db1f.]
5. Braga VA, Medeiros IA, Ribeiro TP, et al. Angiotensin-II-induced reactive oxygen species along the SFO-PVN-RVLM pathway: implications in neurogenic hypertension. Review. Brazilian Journal of Medical and Biological Research (BJMBR)-on line., 2011.
6. Oliveira, A.C., Sena-Filho JG., Mendes-Junior L G., Anjos R M., Ribeiro, TP., Barbosa-filho, J. M., Braga, V. A., Medeiros, I. A. Erythroxylum pungens O.E.Schulz elicits vasorelaxation by reducing intracellular calcium concentration in vascular smooth muscle cells of rats. Revista Brasileira de Farmacognosia (Impresso). , v.01, 2011.
Artigos submetidos para publicação.
1. França-Silva, Maria S., Ribeiro, Thaís P., Luciano, Melissa N, Silva, Juliane
S., Santos, A. F., França, K C, Nakao, Lia S, Athayde-Filho, P. F., Braga, Valdir A, Medeiros, Isac A., Introducing a new nitric oxide donor: the 2-nitrate-1,3-dibuthoxypropan (NDBP) and its vasorelaxant effect. Nitric Oxide (Print). , 2012. 3
2. DANTAS, B. P. V., Magalhães, N, Ribeiro, Thaís P, Oliveira, A. C., Assis, K. P, Câmara, C., Braga, Valdir A, Medeiros, Isac A., Alencar, J.L. Naphthoquinone, a new oxime, induces vasorelaxation via nitric oxide signaling mechanisms. Fundamental & Clinical Pharmacology. , 2012.

154
Publicações

155
Este trabalho tem por objetivo investigar e caracterizar a farmacodinâmica do
α-terpineol, um monoterpeno constituinte de diferentes óleos essenciais, sobre o
sistema cardiovascular de ratos espontaneamente hipertensos (SHR) e seus
controles normotensos (WKY), utilizando metodologias in vivo e in vitro. Este estudo
compreende ainda em avaliar os efeitos do α-terpineol sobre a variação da produção
de óxido nítrico e os mecanismos de ativação da enzima eNOS em células
endoteliais cultivadas.
Esta seção abrange 3 artigos formados a partir dos resultados da tese:
O primeiro artigo (estudo A) consiste na caracterização dos efeitos
cardiovasculares do α-terpineol com foco sobre o óxido nítrico.
No segundo artigo (estudo B) foram evidenciados os mecanismos
adicionais envolvidos na resposta cardiovascular do α-terpineol com
experimentos in vivo. Os efeitos do α-terpineol foram investigados sobre o
controle autonômico de ratos espontaneamente hipertensos (SHR) e seus
controles normotensos (WKY), bem como a participação da via dependente
de óxido nítrico em animais conscientes e livre movimentação.
E por fim, no último artigo (estudo C), foi investigada a rede de sinalização
celular envolvida no relaxamento vascular de animais hipertensos, com
ênfase sobre o papel do endotélio vascular. Foi caracterizado a via de
ativação da enzima eNOS e consequente produção de NO e participação
da enzima guanili ciclase solúvel e a participação do EDHF e dos canais de
potássio.

156
Estudo A: Caracterização dos efeitos cardiovasculares induzidos por -terpineol:
um papel para via NO-GMPc
Artigo 1: Unraveling the cardiovascular effects induced by -terpineol: a role for the
NO-cGMP pathway
Revista: Clinical and Experimental Pharmacology and Physiology, 37(8),811-6, 2010
RESUMO
Introdução: -Terpineol é um monoterpeno presente em óleos essenciais de
diversas espécies de plantas aromáticas. Objetivos: No presente estudo,
investigamos o mecanismo de ações cardiovasculares induzidas pelo -terpineol.
Resultados: O monoterpeno -terpineol (1, 5, 10, 20 e 30 mg ⁄ kg, i.v.) produziu
hipotensão dependente da dose (-10 ± 3, -20 ± 8, -39 ± 16, -52 ± 21 e -57 ± 23
mmHg, respectivamente; n = 5) seguida da taquicardia. A resposta hipotensora foi
atenuada após a administração do N-nitro-Larginina metil-éster (L-NAME; 20 mg⁄
kg, i.v.; -2 ± 1, -5 ±2, -7 ± 3, -22 ± 9 and -22 ± 10 mmHg, respectivamente; P < 0,05;
n = 5). Em anéis de artéria mesentérica pré-contraídas com 10 μM de fenilefrina
(PE), -terpineol (10-12 a 10-5 μM) causou relaxamento dependente de concentração
(relaxamento máximo em resposta a fenilefrina 10μM (Emax)= 61 ± 6%; n = 7). Após
a remoção do endotélio vascular o vasorrelaxamento foi atenuado (Emáx= 20 ± 1%;
p<0,05; n= 7). Em adição o vasorrelaxamento induzido pelo -terpineol em anéis de
artéria mesentérica pré-tratados com 100 ou 300 μM L-NAME, 30 μM
hidroxicobalamina ou 10 μM 1H-[1,2,4]oxadiazolo[4,3-a]quinoxalina-1-ona foi
atenuado (Emax=18 ± 3, 23 ± 3, 24 ± 7 and 21 ± 1%, respectivamente; n = 6; P <
0,05). Em seguida, o -terpineol (10-6, 10-5 e 10-4 μM) induziu aumento dos níveis de
óxido nítrico (NO) (12 ± 6, 18 ± 9 e 34 ± 12% fluorescência, respectivamente; n= 3)
em linhagem de células endoteliais de aorta de coelho. Em conclusão, o uso
combinado de metodologias que envolvem experimentos funcionais e bioquímicos,
no presente estudo, foi capaz de demonstrar que a hipotensão e vasorrelaxamento
induzido pelo -terpineol são mediados em parte pelo endotélio e envolve a indução
do NO e a via NO-GMPc.

157

158

159

160

161

162

163
Estudo B: Avaliação das ações cardiovasculares do -terpineol em animais
hipertensos – Experimentos in vivo.
Artigo 2: α-Terpineol induces hypotension and improves baroreflex sensitivity in
spontaneously hypertensive rat
Revista: Journal Cardiovascular Pharmacology, to be submitted, 2012
RESUMO
Introdução: Os monoterpenos apresentam propriedades benéficas no sistema
cardiovascular, como efeitos protetores sobre a camada endotelial, vasorelaxante e
hipotensores (Bastos, 2009; Ribeiro, 2010). Objetivos: O presente estudo investigou
a resposta hipotensora ao tratamento intravenoso (i.v) com monoterpeno, α-
terpineol, em ratos espontaneamente hipertensos (SHR) e controles normotensos
(WKY). Resultados: Em ambos SHR e WKY, injeções de α-terpineol (1–20 mg/kg,
i.v) diminuiu a pressão arterial média (MAP) dependente da dose em WKY e SHR
(-103, -399, -5211, -6212mmHg, n=10 e -37 5, -577, -715, -844 mmHg,
n=9, respectivamente) associado a taquicardia. O tratamento com hexametônio (30
mg/kg), ou atropina (2 mg/kg), ou atenolol (20 mg/kg), ou prazosim (1 mg/kg), não
afetou a hipotensão induzida por α-terpineol. Em seguida, a injeção do L-NAME
(20mg/kg), um bloqueador da NOS, foi capaz de reduzir a hipotensão produzida pelo
α-terpineol em ratos SHR e WKY, tanto em porcentagem quanto em valores
absolutos. A sensibilidade do barorreflexo de animais hipertensos e normotensos foi
avaliada antes e após o tratamento intravenoso com o α-terpineol e observamos que
o -terpineol foi capaz de aumentar a sensibilidade do barorreflexo de animais SHR.
Este conjunto de dados demonstra que o tratamento intravenoso com α-terpineol
diminui a pressão arterial em ratos hipertensos e sugere que pode ser parcialmente
atribuído a ação vascular, associado ao aumento da sensibilidade do barorreflexo.

164
α-Terpineol induces hypotension and improves baroreflex sensitivity in
spontaneously hypertensive rat
Thaís P. Ribeiro (1); Aurylene C. Oliveira (1); Maria S. França-Silva (1); Leônidas G.
Mendes-Junior (1); Valdir A. Braga(1); Isac A. Medeiros(1).
(1) Centro de Biotecnologia, Universidade Federal da Paraíba, Cidade
Universitária, Campus I, João Pessoa, PB, Brazil;
Running title: α-terpineol induces hypotension in hypertensive rats.
Corresponding author and reprint requests to:
Isac Almeida de Medeiros, PhD
Biotechnology Center, Federal University of Paraiba
B.O. Box 5009, 58.051-970
João Pessoa, PB, Brazil.
Phone: (55) 83 3216 7366 or 3216 7177
FAX : (55) 83 3216 75 11 or 83 3216 73 65
E-mail: [email protected]

165
SUMMARY
Studies in animals have documented beneficial properties of monoterpenes in the
cardiovascular system such as endothelial protective, vasorelaxant and hypotensive
activities (Bastos, 2009; Ribeiro, 2010). The present study investigated the
hypotensive responses to intravenous (i.v.) treatment with α-terpineol in the
spontaneous hypertensive rats (SHR) and Wistar normotensive controls (WKY). In
both SHR and WKY (i.v.) bolus injections of α-terpineol (1–20 mg/kg) decreased
mean arterial pressure (MAP) in a dose-related manner [WKY -103, -399, -5211,
-6212 mmHg, n=10) and SHR -375, -577, -715, -844 mmHg, n=9] associated
with tachycardia following bradycardia [WKY: Time 0: 45±5, 64±11, 110±7, 113±22
bpm; Time 3 min: -3±5, -10±4, -73±4, -125±2 bpm, n=10; SHR: Time 0: 61±5, 75±9,
85±3, 72±8 bpm; Time 3 min: -33±12, -71±5, -126±16, -144±32 bpm, n=9]. In SHR
unaffected the enhancement of α-terpineol-induced hypotension likes
hexamethonium (30 mg/kg) or atropine (2 mg/kg) or atenolol (20 mg/kg), prazosin (1
mg/kg). Likewise, both maximal percentage and absolute decreases in MAP elicited
by i.v. injection of the L-NAME (20mg/kg), NOS blocker, were significantly greater in
SHR than in control. We observe the α-terpineol increased the baroreflex gain,
improving the sensitivity of this cardiovascular reflex. These results show that α-
terpineol (i.v.) decreases blood pressure in conscious SHR, and this action is greater
when compared with normotensive rats. The data further support our previous
hypothesis that hypotensive effects of α-terpineol are partially attributed to the
actions of NO formation, and associate to increases in baroreflex sensitivity.
Keywords: monoterpene, hypotension, nitric oxide

166
INTRODUCTION
The arterial pressure is regulated by feedback control systems, operating in
both short and long term, which rely on autonomic nerves and circulating hormones
as their effector mechanisms. The vascular resistance in any particular region is
influenced, to varying degrees depending on the region, by the activity of sympathetic
vasomotor nerves, the level of circulating vasoactive hormones and also by local
factors, including metabolites and endothelial factors (Thrasher et al. 2006). The
principal mechanism for regulating arterial pressure in the short term is the
baroreceptor reflex with the sympathetic nervous system that controls the distribution
of cardiac output to different vascular beds (Kirchheim 1976). That involves the
compensatory reflex mechanism that responds to changes in arterial pressure
(Taylor et al. 2010). Cardiovascular homeostasis in the longer term depends on an
interaction between hormones and the sympathetic nervous system and this involved
in the onset of hypertension and different animal models have been used to study
this pathology, such as the spontaneously hypertensive rats (SHR). In SHR is
characterized by increased peripheral vascular resistance, sympathetic overactivity
and increased heart rate (Valenti et al. 2011; Kawada et al. 2011; Krum et al. 2011).
A precise knowledge of early development of the cardiovascular diseases is
often target for the studies with these new drugs where the vascular and cardiac
parameters are investigated (Edris et al., 2007). Although many effective drugs for
the treatment of hypertension exist, there is great interest in the research of new
bioactive products to treat hypertension (Kwan et al. 1995), including from plants
such as monoterpenes essential oils derivative (Luo et al. 2010).
Studies in animals have demonstrated beneficial properties of monoterpenes
in the cardiovascular system such as endothelial protective, vasorelaxant and
hypotensive activities (Guedes et al. 2004, Bastos et al. 2009, Magalhães et al,
2008). In this context, -terpineol, a monoterpene, is able to induce a reversible and
concentration-dependent vasorelaxation that was reduced or abolished under
blockade of NOS by L-NAME isolated rat superior mesenteric artery rings and
consequent release of endothelium-derived relaxing factors (EDRFs), mainly NO
(Ribeiro et al., 2010).

167
Although some studies have been conducted, the cardiovascular effects of α-
terpineol needs further investigation. Of note, its effects on hypertension had not yet
been investigated. Since hypertension is often associated with an imbalance
between sympathetic and parasympathetic activity, and the dysfunction in
baroreceptor reflex, we aimed to evaluate the action of α-terpineol on the
cardiovascular parameter and baroreflex sensitivity in spontaneously hypertensive
rats (SHR) and its normotensive control (WKY).
METHODS
Animals
Male 14 to 16-week-old Wistar Kyoto (WKY) and spontaneously hypertensive
(SHR) rats, were used for all experiments. Animals were housed under controlled
conditions of temperature (21 1ºC), lighting cycle (lights on: 06:00-18:00 h), and
food (Labina®, PURINA, Brazil) and water ad libitum. Experimental protocols and
procedures were approved by the Institutional Animal Care and Use Committee of
the Biotechnology Center – Federal University of Paraiba (CEPA # 020207).
Drugs
The drugs used were: cremophor EL, dimethyl sulphoxide (DMSO), L-
phenylephrine chloride, sodium nitroprussiate, hexamethonium, atropine, prazosim,
atenolol, Nw-nitro-L-arginine methyl esther (L-NAME), all from Sigma Chemical Co.,
Saint Louis, MO, USA. Heparin sodium salt (Roche), sodium thiopental (Cristália)
and α-Terpineol 95.0% (GC) of purity (Sigma).
The α-terpineol stock solution was prepared in saline solution and kept at -4o
C. α-Terpineol was dissolved in a mixture of saline and chremophor and diluted to
the desired concentrations just before use. The other compounds were freely
dissolved in saline solution.

168
Arterial pressure (AP) and heart rate (HR) recordings in unanesthetized rats
For AP and HR recordings, procedures were similar to those previously
described (Oliveira et al. 1996). Briefly, under ketamin plus xilazin anesthesia (45
mg.Kg-1, i.p.), rats were fitted with polyethylene catheters inserted into the lower
abdominal aorta and inferior vena cava through left femoral artery and vein,
respectively. Both catheters were filled with heparinized saline, tunneled
subcutaneously, exteriorized and sutured at the dorsal surface of the neck. Twenty-
four hours after surgical procedures, experiments were performed in unanesthetized
rats. Blood pressure and heart rate were recorded in conscious rats using a pressure
transducer coupled to an acquisition system (LabTrax 2-24T, World Precision
Instruments, Sarasota, FL, USA) connected to a computer running the software
DataTrax 2 (World Precision Instruments, Sarasota, FL, USA)..
Experimental design and protocols
1. Effect of α-terpineol on blood pressure and heart rate in unanesthetized rats
Normotensive (WKY) and hypertensive (SHR) animals received a series of
increasing bolus doses (1, 5, 10 and 20 mg/kg) of α-terpineol via the i.v. catheter,
and time course of the changes in blood pressure and heart rate was recorded. The
injections were separated by a time sufficient to allow full recovery of arterial
pressure, usually 15 min. This series of experiments was carried out to establish a
dose–effect relationship and the ED50 of α-terpineol.
2. Effects of α-terpineol on the autonomic control in unanesthetized rats
After hemodynamic parameters had stabilized, ED50 doses of α-terpineol
(4.8 mg/kg, i.v.) were administered. Thirty minutes after administration of α-terpineol,
atropine (2 mg ⁄ kg; i.v.; 30 min.), a non-selective muscarinic receptor antagonist,
prazosin (1 mg/kg, i.v) alpha-adrenergic receptor antagonist, atenolol (20 mg ⁄ kg;
i.v.; 30 min), beta-adrenergic receptor antagonist, or hexamethonium (30 mg/kg, i.v.),
a nicotinic receptor antagonist and ganglionic blocker, were administered separately,

169
and 30 min later α-terpineol was repeated. Changes in MAP and HR induced by α-
terpineol were compared before and after blockers.
3. Systemic hemodynamic effects of α-terpineol before and after nitric oxide synthase
blockade in vivo
Different doses of α-terpineol (4.8 mg/Kg i.v.) were administered. Successive
injections were separated by a time sufficient to allow full recovery of arterial
pressure (usually 15 min). After a 30 min of baseline recording, L-NAME (20 mg.Kg-
1, i.v.) was administered and 30 min later α-terpineol was repeated. Changes in MAP
and HR induced by α-terpineol were compared before and after L-NAME treatment.
4. Effects of α-terpineol in the baroreflex sensitivity
For baroreflex sensitivity studies, animals were divided in six different groups:
WKY + vehicle; WKY + α-terpineol; SHR + vehicle; SHR + α-terpineol. Following
baseline blood pressure and heart rate recordings, baroreflex was activated using
classical vasoactive drugs (modified Oxford Method, Botelho-Ono, 2010) before and
after acute administration of drugs. Phenylephrine (8 μg/Kg) and sodium
nitroprusside (25 μg/Kg) were given as intravenous bolus injection before and after α-
terpineol (4.8 mg/Kg, i.v.) or vehicle depending on the group. A 15-minute interval
was allowed between phenylephrine and sodium nitroprusside injections. Reflex
changes in heart rate produced by vasoactive drugs administration were quantified
and plotted as changes in heart rate over changes in mean arterial pressure
(ΔHR/ΔMAP) as described by Braga et al. (2008).
Data analysis
Values were expressed as mean ± S.E.M. When appropriate, statistical
significance was determined by two-way ANOVA following Bonferroni’s post-test,
using GraphPad Prism© software, version 5.0 (GraphPad Software Inc., La Jolla,
CA, USA). Values of P<0.05 were considered statistically significant.

170
RESULTS
Effect of α-terpineol on blood pressure and heart rate in unanesthetized rats
Baseline values of mean arterial pressure WKY and heart rate were 105 ± 3
mmHg and 360 ± 3 bpm, respectively and 185 ± 5 mmHg and 380 ± 5 bpm for SHR.
α-Terpineol (1, 5, 10 and 20 mg/kg, i.v., randomly) induced hypotension in a dose-
dependent manner WKY: (-103, -399, -5211, -6212 mmHg, n=10) and SHR:
(-375, -577, -715, -844 mmHg, n=9) (Figure 1A, B), associated to an initial
tachycardia followed by a severe bradycardia in both animal groups (WKY: Time 0:
45±5, 64±11, 110±7, 113±22 bpm; Time 3 min: -3±5, -10±4, -73±4, -125±2 bpm,
n=10; SHR: Time 0: 61±5, 75±9, 85±3, 72±8 bpm; Time 3 min: -33±12, -71±5, -
126±16, -144±32 bpm, n=9; figure 1 C, D).

171
Figure 1. Changes in mean arterial pressure (MAP) and heart rate (HR) induced by the acute administration of different doses of α-terpineol (1- 20 mg/kg, i.v.) in conscious rats. (A and C) normotensive Wistar Kyoto rats; (B and D) spontaneously
hypertensive rats. Values are expressed as mean s.e.m. (n=6), *P0.05 vs. control (Two-way ANOVA followed by Bonferroni’s post-test).

172
Effects of α-terpineol on the autonomic control in unanesthetized rats
After evaluating the action of α-terpineol on the autonomic control we
observed that parasympathetic blockade with atropine (2 mg ⁄ kg; i.v.) did not cause
changes in the hypotensive response elicited by α-terpineol ED50: 4.8 mg ⁄ kg; i.v. in
both hypertensive and normotensive animals (Figure 4A). WKY: -515 mmHg, n=6
and after Atropine WKY: -546 mmHg, n=6 and SHR: -627 mmHg, n=6 and after
atropine SHR: -619 mmHg, n=5. In contrast, the tachycardia and bradycardia
response was significantly reduced after α-terpineol treatment [WKY: Time 0: 65±11
bpm; Time 3 min: -11±4 bpm, n=5; After atropine WKY: Time 0: 59±3 bpm; Time 3
min: -2±2 bpm, n=5; and SHR: Time 0: 89±5 bpm; Time 3 min: -125±6 bpm, n=5;
After atropine SHR: Time 0: 60±4 bpm; Time 3 min: -10±4 bpm, n=5; figure 2 C, D].
Figure 2. Changes in mean arterial pressure (MAP), and heart rate (HR) induced by the acute administration of different doses of α-terpineol (4.8 mg/kg, i.v.) in normotensive and hypertensive rats before and after administrations of atropine (2
mg ⁄ kg; i.v.). Values are expressed as mean s.e.m. (n=6), *P0.05.

173
Likewise, α-terpineol ED50: 4.8 mg ⁄ kg; i.v. in both hypertensive and
normotensive animals (Figure 4A) the blockade with atenolol (20 mg ⁄ kg; i.v.) or
hexametonium (30 mg ⁄ kg; i.v.) (Figure 5A,B) WKY: -535 mmHg, n=5 and after
atenolol WKY: -678 mmHg, n=6 and SHR: -643 mmHg, n=6 and after atenolol
SHR: -622 mmHg, n=4 or hexametonium WKY: -543 mmHg, n=5 and after
hexametonium WKY: -5110 mmHg, n=5 and SHR: -656 mmHg, n=6 and after
hexametonium SHR: -615 mmHg, n=5 (Figure 6A,B) significantly reduced the
tachycardic and bradycardic responses but not cause changes in the hypotensive
response to α-terpineol, in hypertensive and normotensive rats. WKY: Time 0: 73±6
bpm; Time 3 min: -26±7 bpm, n=5; After Atenolol WKY: Time 0: 42±6 bpm; Time 3
min: -16±8 bpm, n=5; and SHR: Time 0: 77±6 bpm; Time 3 min: -145±10 bpm, n=5;
After Atenolol SHR: Time 0: 45±7 bpm; Time 3 min: -73±22 bpm, n=5; figure 5 C, D)
and WKY: Time 0: 74±6 bpm; Time 3 min: -10±3 bpm, n=5; After hexametonium
WKY: Time 0: 0±0 bpm; Time 3 min: -16±2 bpm, n=5; and SHR: Time 0: 88±4 bpm;
Time 3 min: -120±34 bpm, n=5; After hexametonium SHR: Time 0: 5±1 bpm; Time 3
min: -22±10 bpm, n=5; figure 6 C, D).
Figure 3. Changes in mean arterial pressure (MAP), and heart rate (HR) induced by the acute administration of different doses of α-terpineol (4.8 mg/kg, i.v.) in

174
normotensive and hypertensive rats before and after administrations of atenolol (20
mg ⁄ kg; i.v.). Values are expressed as mean s.e.m. (n=6), *P0.05.
Figure 4. Changes in mean arterial pressure (MAP), and heart rate (HR) induced by the acute administration of different doses of α-terpineol (mg/kg, i.v.) in normotensive and hypertensive rats before and after administrations of hexamethonium (30 mg ⁄
kg; i.v.). Values are expressed as mean s.e.m. (n=6), *P0.05.

175
Prazosin (1 mg ⁄ kg; i.v.), in turn, showed no changes in blood pressure and
heart rate (Figure 7A,B). MAP (WKY): -594 mmHg, n=5 and after Prazosin WKY: -
569 mmHg, n=5 (SHR): -677 mmHg, n=5 and after Prazosin SHR: -656 mmHg,
n=5 (Figure 6A,B) HR(WKY): Time 0: 73±3 bpm; Time 3 min: -26±7 bpm, n=5; After
Prazosin WKY: Time 0: 78±8 bpm; Time 3 min: -36±3 bpm, n=5; (SHR): Time 0:
77±6 bpm; Time 3 min: -143±10 bpm, n=5; After Prazosin SHR: Time 0: 85±7 bpm;
Time 3 min: -173±12 bpm, n=5; figure 7 C, D).
Figure 5. Changes in mean arterial pressure (MAP), and heart rate (HR) induced by the acute administration of different doses of α-terpineol (4.8 mg/kg, i.v.) in normotensive and hypertensive rats before and after administrations of prazosin (1
mg⁄kg; i.v.). Values are expressed as mean s.e.m. (n=6), *P0.05.

176
Systemic hemodynamic effects of α-terpineol before and after nitric oxide synthase
blockade in vivo
The hypotensive response was attenuated after acute blockade of the NO-
synthase with L-NAME (20 mg/Kg) MAP (WKY): -499 mmHg, n=5 and after L-
NAME WKY: -292 mmHg, n=7 (SHR): -675 mmHg, n=8 and after L-NAME SHR: -
351 mmHg, n=7 (Figure 8 A, B). The heart rate was also significantly attenuated at
4.8 mg/kg, demonstrating the importance of the NOS-activation in the systemic
effects induced by α-terpineol (figure 8). Bradycardic response three minutes after
administration this monoterpene was reduced only in hypertensive rats. HR (WKY):
Time 0: 64±11 bpm; Time 3 min: -33±4 bpm, n=7; After L-NAME WKY: Time 0: 45±7
bpm; Time 3 min: -37±22 bpm, n=5; (SHR): Time 0: 78±8 bpm; Time 3 min: -163±21
bpm, n=7; After L-NAME SHR: Time 0: 45±8 bpm; Time 3 min: -87±22 bpm, n=7;
figure 8 C, D).
Figure 6. Changes in mean arterial pressure (MAP), and heart rate (HR) induced by the acute administration of different doses of α-terpineol (4.8 mg/kg, i.v.) in normotensive and hypertensive rats before and after administrations of L-NAME (20
mg ⁄ kg; i.v.). Values are expressed as mean s.e.m. (n=6), *P0.05

177
Effects of α-terpineol in the baroreflex sensitivity
Representative tracings showing the changes in heart rate in response to
baroreflex activation are illustrated in Fig. 8. Rats from the SHR group presented a
reduction in baroreflex gain when compared to the WKY group (−0.86±0.07 vs.
−2.51±0.2 bpm mm Hg−1, P>0.05) as shown in Fig. 9. In SHR rats, acute
administration of α-terpineol (4.8 mg/Kg, i.v.), a monoterpene, restored the
depressed baroreflex sensitivity to values that resembles to those presented by WKY
+ α-terpineol and SHR + α-terpineol group (−2.23±0.2 vs. −1.5±0.08 bpm mm Hg−1, P
>0.05, n=4). Of note, administration of vehicle (i.v.) before and after baroreflex
activation produced no changes in baroreflex gain in either SHR or vehicle groups
(Fig. 8).
Figure 7. Effects of α-terpineol (4.8 mg/kg,i.v.) on the baroreflex sensivity of
normotensive (WKY) and hypertensive (SHR) rats. Values are expressed as mean
s.e.m. (n=5), (*) SHR control versus SHR after α-terpineol, (#) WKY and SHR P0.05
DISCUSSION

178
In this report, we sought to clarify the underlying mechanisms by which α-
terpineol elicits its cardiovascular effects in rats. The major findings of this work were
that the monoterpene α-terpineol induces marked hypotension and improvement of
baroreflex sensitivity in spontaneously hypertensive unanesthetized rats, which could
be attributed, at least in part, to a decrease of peripheral vascular resistance
mediated by increases in NO release and consequently activation of the NO-GMPc
pathway.
Many kinds of animal models are being employed to understand potential
mechanisms of cardiovascular control in health and disease. Examples of some of
these animal models include spontaneously hypertensive rat (SHR), which is a
suitable model to study hypertension development as it mimics humans essential
hypertension. These similarities include a genetic predisposition to high blood
pressure with no specific etiology, increased total peripheral resistance without
volume expansion and its endothelial function is decreased in its early stage
(Grunfeld et al., 1995).
Baseline MAP and HR values of conscious normotensive rats (WKY) and
spontaneously hypertensive rat (SHR) were of the same order of magnitude as those
reported previously in the same preparation (Guimarães et al. 2012). In both groups,
i.v. administration with α-terpineol induced immediate and dose-dependent decrease
in MAP and tachycardic response. Recent studies from our laboratory have shown
that i.v. administration of α-terpineol decreased MAP in conscious normotensive rats
(Ribeiro et al. 2010). However, in the present study, this is the first time that such
cardiovascular effects of α-terpineol have been reported in SHR. We focused on the
initial hypotension that occurred concomitantly with initial reflex tachycardia followed
by bradycardia.
To examine the origin of the α-terpineol-induced initial hypotension and
tachycardia followed by bradycardia, we compared the cardiovascular responses to
pretreatment with i.v. atropine partially significantly decreased the bradycardic effects
of α-terpineol without affecting the hypotension in SHR and WKY rats.
To determine the role of the autonomic nervous system in α-terpineol -induced
cardiovascular effects in rats. The administration of α-terpineol was able to decrease
MAP in SHR and WKY rats, even when the central sympathetic nerve drive was
eliminated by ganglionic blockade with hexamethonium. The hypotensive effects of

179
α-terpineol are associated with a significant and dose-dependent bradycardia after 3
min its administration, which appears to be partly dependent upon the presence of an
operational autonomic drive to the heart, as demonstrated by its attenuation in
hexamethonium in SHR and WKY rats. This indicates that α-terpineol-induced
maximal hypotensive and tachycardic response was unaffected in SHR and WKY
rats and bradycardic responses to α-terpineol are mediated by a vagal reflex and an
efferent cholinergic mechanism.
In a separate group of animals SHR and WKY rats (n = 5), hypotensive
responses to α-terpineol ED50 4.8 mg/kg, i.v. also remained unaffected by i.v. The
lack of effect of atenolol on baroreflex-mediated bradycardia in SHR and WKY was
expected. We have demonstrated that attenuation of the HR response to
baroreceptor stimulation by cardiac autonomic blockade does not affect the reflex
decreases in BP. The baroreceptor reflex bradycardia during rapid increases in BP is
normally mediated by the parasympathetic nervous system in conscious rats. The
second important finding from the present study is that hypotensive responses to α-
terpineol also remained unaffected after treatment with prazosin, a selective α-1-
adrenoceptor antagonist, in SHR and WKY rats.
Impaired endothelial function and reduced baroreflex sensitivity (BRS) are
important predictors of cardiovascular morbidity, especially in SHR rats. Considering
that endothelium-derived NO plays a major role in the regulation of blood pressure
and vascular tone (Chowdhary; Townend, 1999) we hypothesized that the decrease
in blood pressure elicited by α-terpineol could be due to NO release from intact
vascular endothelium. Indeed, in the presence of NO synthase inhibition,
hypotension and tachycardia induced by α-terpineol were significantly attenuated
when compared to that induced by the α-terpineol given alone indicating that, the
hypotensive effect of the compound in conscious normotensive rats may be
dependent on NO release from vascular endothelium. It is most likely that the
vasorelaxation produced by α-terpineol evoked baroreflex-mediated tachycardia,
mainly in the lower doses. However, we cannot rule out a direct action of α-terpineol-
derived NO on the autonomic control of the heart as described earlier (Charkoudian
et al. 2009 and Kishi et al. 2003).
It is well documented in the literature that nitric oxide can act on brain areas
involved in the cardiovascular control (Kishi et al. 2003). In this way, Kishi et al.
(2003) demonstrated that overexpression of eNOS in the RVLM favors GABA

180
release and sympathoinhibition, reducing the sympathetic tone to the vessels and to
the heart causing hypotension and bradicardia (Garcıa et al. 2008).
Evidence from animal studies suggests that diminished baroreflex sensitivity is
caused by endothelial dysfunction (Fahim 2003; Chapleau 1989). In particular, in
experimentally induced endothelial dysfunction, the decreased prostacyclin and
increased thromboxane concentrations are associated with reduced baroreflex
impulses from the carotid artery (Chapleau et al. 1995). Evaluating alterations in the
balance of cardiovascular sympathetic/parasympathetic motor activity is important for
gaining insights into neural mechanisms of cardiovascular disease. In addition, many
diseases are associated with a change in baroreceptor reflex gain. For example,
essential hypertension is related to an increase in sympathetic tone (Grassi et al.
1998) and an attenuated cardiac baroreceptor reflex (Korner et al. 1995), which is an
important prognostic indicator of autonomic dysfunction (LaRovere et al. 2001).
Baroreceptor afferent sensitivity and baroreflex-mediated changes in heart rate (HR)
(Ohta et al. 1995) are consistently impaired in spontaneously hypertensive rats
(SHR) (Kawada et al. 2011). The new findings in the present study were that the
baroreflex sensitivity by α-terpineol was enhanced in SHR and WKY rats.
The reasons for the enhancement of the baroreflex sensitivity in SHR and
WKY rats α-terpineol-induced are complex. One possibility is that the cardiac
sympathetic afferent inputs increase in hypertension, which may be caused by α-
terpineol release in the myocardium stimulating the cardiac sympathetic afferents
and by the increased sensitivity of cardiac sympathetic afferents to the chemical
stimulus. Another possibility is that the central gain of the baroreflex sensitivity α-
terpineol-induced is increased in hypertension, which is supported by the present
findings that the baroreflex sensitivity responses induced by overexpression of eNOS
in the brain were greater in SHR and WKY rats (Guo et al. 2009).
The autonomic nervous system influences cardiovascular physiology, at least
partly, by the arterial baroreflex. Thus the impairment of endothelial function and
decrease of nitric oxide (NO) is seen very early in the development of hypertension.
Interestingly, the enhanced α-terpineol in SHR and WKY rats may possibly be
associated with preferential vasodilation in the mesenteric vascular bed (Magalhães
et al. 2008, Ribeiro et al. 2010).

181
Regardless of how it acts, by improving endothelial cell function, α-terpineol
could improve autonomic nervous system control through 2 mechanisms: indirectly,
by improving hemodynamics, or directly, by acting on subendothelial nerve endings
at the baroreceptor level (carotid, aortic, or cardiopulmonary). Possible support for a
direct action comes from the recent observation that endothelium-derived nitric oxide
increases vagal activity in SHR rats. However further chronic studies are needed to
explore the interactions between α-terpineol-induced NO release and their
consequent actions of sympathetic activity and baroreflex sensitivity.
In conclusion, we have demonstrated that α-terpineol produces hypotension in
vivo normotensive Wistar Kyoto (WKY) and spontaneously hypertensive rats (SHR)
and increases in baroreflex sensitivity.
ACKNOWLEDGEMENTS
The authors wish to express their sincere thanks to José Crispim Duarte and
collaborators for technical assistance. This work was funded by CAPES and CNPq-
Brazil.

182
REFERENCES
Castro, H. G.; Oliveira, L. O.; Barbosa, L. C. A.; Silva, D. J. H.; Nascimento, E. A.;
Teor e Composição do Óleo Essencial de Cinco Acessos de Mentrasto Quim.
Nova, 2004; 27 (1), 55-57. [Article in Portuguese]
Chapleau MW, Cunningham T, Sullivan MJ, Watchel RE, Abboud FM. Structural
versus functional modulation of the arterial baroreflex. Hypertension. 1995;
26:341–347
Chapleau MW, Hajduczok G, Abboud FM. Peripheral and central mechanisms of
baroreflex resetting. Clin Exp Pharmacol Physiol Suppl. 1989;15:31-43.
Charkoudian, N.; Rabbitts, J. A. Sympathetic neural mechanisms in human
cardiovascular health and disease. Mayo Clin. Proc. 2009; 84: 822–30.
Chowdhary S, Townend JN. Role of nitric oxide in the regulation of cardiovascular
autonomic control. Clin. Sci. 1999; 97: 5–17.
Edris AE, Pharmaceutical and therapeutic potentials of essential oils and their
individual volatile constituents: a review. Phytother. Res., 2007; 21: 308-323.
Fahim M. Cardiovascular sensory receptors and their regulatory mechanisms. Indian
J Physiol Pharmacol. 2003 47(2):124-46.
Garcıa DA, Vendrell I, Galofre M, Sunol C. GABA released from cultured cortical
neurons influences the modulation of t-[35S] butylbicyclophosphorothionate
binding at the GABAA receptor: Effects of thymol. Eur. J. Pharmacol. 2008; 600:
26–31.
Grassmann, J.; Hippeli, S.; Spitzenberger, R.; Elstner, E. F.; The monoterpene
terpinolene from the oil of Pinus mugo L. in concert with alpha-tocopherol and
beta-carotene effectively prevents oxidation of LDL. Phytomedicine. 12(6-7),
416-23 2005(b).
Grassmann, J.; Terpenoids as plant antioxidants. Vitam. Horm. 2005 a; 72, 505-35.
Grunfeld, S., C.A. Hamilton, S. Mesaros, S.W. McClain, A.F. Dominiczak, D.F. Bohr
and T. Malinski. Role of superoxide in the depressed nitric oxide production by

183
endothelium of genetically hypertensive rats. Hypertension 26(Part 1): 854–857,
1995.
Guimarães DD, Carvalho CC, Braga VA. Scavenging of NADPH Oxidase-derived
Superoxide Anions Improves Depressed Baroreflex Sensitivity in
Spontaneously Hypertensive Rats Clin Exp Pharmacol Physiol. 2012 Jan 27.
doi: 10.1111/j.1440-1681.2012.05679.x.
Guo ZL, Tjen-A-Looi SC, Fu LW, Longhurst JC. Nitric oxide in rostral ventrolateral
medulla regulates cardiac-sympathetic reflexes: role of synthase isoforms. Am J
Physiol Heart Circ Physiol. 2009; 297(4):H1478-86.
Kagiyama S, Tsuchihashi T, Abe I, Fujishima M. Enhanced depressor response to
nitric oxide in the rostral ventrolateral medulla of spontaneously hypertensive
rats. Hypertension. 1998. 31(4):1030-4
Kawada T, Shimizu S, Kamiya A, Sata Y, Uemura K, Sugimachi M.Dynamic
characteristics of baroreflex neural and peripheral arcs are preserved in
spontaneously hypertensive rats. Am J Physiol Regul Integr Comp Physiol.
2011 Jan;300(1):R155-65.
Kim, J; Marshall, M. R; Wei, C. Antibacterial Activity of Some Essential Oil
Components against Five Foodborne Pathogens? J. Agric. Food Chem. 1995,
43, 2839-2845.
Kishi T, Hirooka Y, Kimura Yet al. Overexpression of eNOS in RVLM improves
impaired baroreflex control of heart rate in SHRSP. Hypertension 2003; 41:
255–60.
Krum H, Sobotka P, Mahfoud F, Böhm M, Esler M, Schlaich M. Device-based
antihypertensive therapy: therapeutic modulation of the autonomic nervous
system. Circulation. 2011; 18;123(2):209-15
Lahlou, S; Leal-Cardoso, J. H; Magalhães, P. J. Essential oil of Croton nepetaefolius
decreases blood pressure through an action upon vascular smooth muscle:
studies in DOCAsalt hypertensive rats. Planta Med. 2000; 66: 138-143.
Magalhães PJC, Criddle DN, Tavares RA, Melo EM, Mota TL, Leal-Cardoso JH.
Intestinal myorelaxant and anti-spasmodic effects of the essential oil of Croton

184
nepetaefolius, and its constituents cineole, methyl-eugenol and terpineol.
Phytother. Res. 1998; 12: 172–177.
Magalhães PJC, Lahlou S, Juca DM, Coelho-de-Souza LN, Frota PTT, Costa AMG,
Leal-Cardoso JH. Vasorelaxation induced by the essential oil of Croton
nepetaefolius and its constituents in rat aorta are partially mediated by the
endothelium. Fund. Clin. Pharmacol. 2008; 22: 169–177
Ohta H, Talman WT. Alteration of baroreceptor and chemoreceptor reflexes in
spontaneously hypertensive rats. Clin Exp Pharmacol Physiol. 1995; 22: S60–
S61.
Oliveira EJ, Medeiros IA, Mukherjee R, Hypotensive and spasmolytic effects of
normacusine B from Strychnos atlantica roots. Phytomedicine 1996; 3: (1) 45–
49.
Parnas, M, et al. Carvacrol is a novel inhibitor of Drosophila TRPL and mammalian
TRPM7 channels. Cell Calcium 2009; 45: 300–309.
Ribeiro, TP; Porto, DL; Menezes, CP; Antunes, AA; Silva, DF; Souza, DP; Nakao,
LS; Braga, AV; Medeiros, IA. Unraveling the cardiovascular effects induced by
α-terpineol: a role for the NO-cGMP pathway. Clin. Exp. Phamacol. Physiol.,
2010; 37(8):811-6.
Saito, K. et al. The biological properties of monoterpenes hypotensive effects on rats
and antifungal activites on plant pathogenic fungi of monoterpenes. Mokuzai
Gakaishi., 1996. 42: (7) 677-680.
Santos, M. R.; Carvalho, A. A.; Medeiros, I. A.; Alves, P. B.; Marchioro, M.; Antoniolli,
A. R.; Cardiovascular effects of Hyptis fruticosa essential oil in rats Fitoterapia.
2007.
Sterner, O; Szallasi, A. Novel natural vanilloid receptor agonists: new therapeutic
targets for drug development. Trends Pharmacol. Sci. 1999; 20: 459– 465.
Taylor JG, Bisognano JD. Baroreflex stimulation in antihypertensive treatment. Curr
Hypertens Rep. 2010 Jun;12(3):176-81.
Thrasher TN. Arterial baroreceptor input contributes to long-term control of blood
pressure. Curr Hypertens Rep. 2006; 8(3):249-54.

185
Toda N, Okamura T. The pharmacology of nitric oxide in the peripheral nervous
system of bood vessels. Pharmacol. Rev. 2003; 55: 271–324.
Valenti VE, De Abreu LC, Colombari E, Sato MA, Ferreira C. The variability of
baroreflex sensitivity in juvenile, spontaneously hypertensive rats. Cardiovasc J
Afr. 2011 Jan-Feb;22(1):14-7.
Vogt-Eisele AK, Weber K, Sherkheli MA. et al., Monoterpenoid agonists of TRPV3.
Br. J. Pharmacol. 2007; 151: 530–540.

186
Estudo C: Mecanismos de sinalização celular envolvidos nos efeitos
vasculares induzidos pelo α-terpineol em animais hipertensos.
Artigo 3: Endothelial signaling mechanisms involved in vasodilation to α-terpineol in spontaneously
hypertensive rats.
Revista: Pharmacological Research, to be submitted, 2012
RESUMO
Introdução: O α-terpineol apresenta propriedades benéficas no sistema
cardiovascular, como efeitos vasorelaxante e hipotensores (Ribeiro et al. 2010) e
demonstrou em animais hipertensos produzir hipotensão e melhora da
sensibilidade do barorreflexo (Ribeiro et al. 2012). Objetivos: Este estudo teve o
objetivo de investigar os mecanismos de sinalização celular envolvidos no
vasorrelaxamento induzido pelo α-terpineol em ratos hipertensos. Resultados: Em
anéis de artéria mesentérica pré-contraídos com fenilefrina (10 µM), α-terpineol (10-
12 a 10-5 M) causa relaxamento dependente da concentração em ratos hipertensos
e controles normotensos (WKY resposta máxima a fenilefrina (10 µM) (Emax) = 60
4 ou SHR [Emax = 53.7 ± 3, n=9]. Após a remoção do endotélio vascular o
relaxamento induzido pelo -terpineol foi atenuado em WKY e SHR. Este efeito do
-terpineol foi atenuado também na presença de 100μM L-NAME, 30 μM
hidroxicobalamina ou ODQ 10 μM em ratos SHR e WKY. Em experimentos com
células endoteliais de coronária de porco observamos que -terpineol induz
ativação das vias PI3K/ATK e AMPK com aumento da fosforilação em Ser 1177 e
consequente ativação da eNOS e produção de NO. Em seguida, o efeito
vasorelaxante induzido pelo -terpineol foi atenuado na presença de 20 mM KCl,
modulador do efluxo de K+ ou diferentes bloqueadores de canais de potássio, como
TEA (1 mM); caribdotoxina (0.2 μM) + apamina (0.2 μM); glibenclamida (10µM) e 4-
AP. Em conclusão nos demonstramos que o vasorrelaxamento induzido pelo -
terpineol, em ambos, ratos SHR e WKY é mediado pela via de ativação da
PI3K/ATK e AMPK com aumento da fosforilação da eNOS e indução de NO, com
consequente ativação da via NO-cGMP, associado a produção do EDHF e
participação dos canais para potássio.

187
Endothelial signaling mechanisms involved in vasodilation to -terpineol in
spontaneously hypertensive rats
Thaís P. Ribeiro(1); Bruna P. V. Dantas (1); José George F. de Albuquerque (1) Lazare
Belamelaba (2); Valdir A. Braga(1); Valérie B. Schini-Kerth(2), Isac A. Medeiros(1).
(1) Centro de Biotecnologia, Universidade Federal da Paraíba, Cidade
Universitária, Campus I, João Pessoa, PB, Brazil;
(2) Laboratoire de Biophotonique e pharmacologie de la Faculté de Pharmacie,
l’Université de Strasbourg, UMR 7213, Illkirch, France.
Running title: -terpineol induces NO and EDHF in hypertensive rats
Corresponding author and requests for reprints:
Isac Almeida de Medeiros, PhD
Centro de Biotecnologia, Universidade Federal da Paraíba
Caixa Postal 5009, 58.051-970
João Pessoa, PB, Brazil.
E-mail: [email protected] Phone: (55) 83 3216 7366 or 3216 7177 FAX : (55) 83
3216 75 11 or 83 3216 73 65
SUMMARY

188
1. α-Terpineol is a monoterpene found in essential oils of several aromatic plant
species. Here we investigate the mechanisms underlying the cardiovascular
changes induced by -terpineol in SHR and WKY rats.
2. In phenylephrine (10 µM) pre-contracted mesenteric artery rings, α-terpineol
(10-12 to 10-5 M) caused a concentration-dependent relaxation [WKY maximum
response to PE (10 µM) = 60 4 or SHR maximum response to PE (10 µM) = 53.7
± 3, p<0.05, n=9]. After endothelium removal, the vasorelaxation elicited by -
terpineol was attenuated in WKY [maximum response to PE (10 µM) = 20.5 1*]
and in SHR [maximum response to PE (10 µM) 16.1 ± 3, p<0.05, n=8]. In addition,
vasorelaxation induced by -terpineol in rings pre-treated with L-NAME 100 µM or
hydroxocobalamin 30 µM or ODQ 10 M was attenuated in SHR and WKY [WKY
maximum response to PE (10 µM) = 18.1 ±3.8; 23.5 ± 7; 20.8 ± 1 and SHR
maximum response to PE (10 µM) = 20.1± 3 ; 17.3 ± 3; 18.1 ± 3 p<0.05, n=8]. In
experiments with endothelial cells we observed that -terpineol activates PI3K/ATK
and AMPK pathways with increase of Ser 1177 phosphorylation and consequently
eNOS activation and NO production.
3. Furthermore, the relaxant effect induced by -terpineol was attenuated in the
presence of KCl (20 mM), a modulator efflux K+ or different potassium channel
blockers such as TEA (1 mM); Charybdotoxin (0.2 μM) plus apamin (0.2 μM);
Glibenclamide (10µM) or 4-AP [WKY maximum response to PE (10 µM) = 23± 4;
37.5± 4; 28.6 ± 7; 33± 3; 38.7± 1 and SHR maximum response to PE (10 µM) =
36.4± 6; 38.5± 4; 35.1 ± 2; 24.2± 3; 42.5 ± 2, p<0.05, n=6].
4. In conclusion, we demonstrated that the -terpineol-induced vasorelaxation in
both SHR and WKY rats is, at least in part, mediated by the endothelium, most
likely via activation of PI3K/ATK and AMPK pathway with increase of eNOS
phosphorylation and NO release and consequently, activation of the NO-cGMP
pathway. Moreover, it seems to involve the EDHF production and potassium
channel activation.
Keywords: monoterpene, vasodilatation, nitric oxide, EDHF

189
INTRODUCTION
Vascular endothelial cells are exposed to numerous endogenous vasoactive
agents, these compounds bind to their respective membrane receptors and elicit a
rise in endothelial [Ca2+]i, which in turn enhances the production and release of a
number of vasodilators, including NO, prostacyclin, and endothelium-dependent
hyperpolarizing factors (EDHF) 1. New findings in the last decade have demonstrated
that the vascular endothelium is an important regulatory organ in maintaining
cardiovascular homeostasis and that endothelial dysfunction, involving alterations of
the L-arginine NO-synthase–soluble guanylyl cyclase pathway, eNOS uncoupling,
EDHF and enhanced production of contracting factors (prostanoids) which has been
associated with hypertension 2-3.
The endothelial nitric oxide synthase (eNOS) has been regarded as the
source of endothelial NO, Ca2+-activated calmodulin is important for the regulation of
eNOS activity. However, other proteins interact with eNOS and regulate its activity
(HSP90, Cav-1, AKT) 4. Proteins kinases, such AKT, AMPK, PKA, CAMKII, have
been proposed phosphorylate sites on eNOS that controlled activity were Ser 1177
as an activator. Further elucidation of therapeutic agents can promote eNOS
coupling and other potential avenues leading to the beneficial actions of NO in the
cardiovascular system 5.
Studies have demonstrated beneficial properties of essential oils in the
cardiovascular system such as antithrombotic, antiplatelet, endothelial protective,
vasorelaxant and hypotensive activities 6-7. Previous studies from Magalhães et.al
(2008) demonstrated that -terpineol induces relaxation in whole mesenteric vascular
bed preparation. Altogether, our preliminary studies indicate that -terpineol induces
endothelium-dependent relaxations in rat mesenteric artery rings by stimulating the
endothelial formation of NO, and is a potent hypotensive agent in vivo in the rat 9.
The major aim of this work is to elucidate the signal transduction pathway
endothelium-dependent relaxations in spontaneously hypertensive rats (SHR) in
response to this monoterpene, using approaches in vitro. We hypothesized the
vasodilator responses to α-terpineol, in SHR, may be involved mediators than NO as
well as K+ channels in small vessels.

190
Fig. 1 Structural formula of a-terpineol
METHODS
Animals
Male SHR and Wistar Kyoto rats (250-300 g) were used for all experiments.
Animals were housed under controlled conditions of temperature (21 1ºC) and
lighting cycle (lights on: 06:00-18:00 h). In addition, they had free access to food
(Labina®, PURINA, Brazil) and tap water. Experimental protocols and procedures
were approved by the Institutional Animal Care and Use Committee of the
Biotechnology Center – Federal University of Paraiba (CEPA # 010210).
Reagents
The drugs used were: cremophor EL, dimethyl sulphoxide (DMSO) L-
phenylephrine chloride, acetylcholine chloride, N-nitro-L-arginine methyl esther (L-
NAME), indomethacin, 1H-[1,2,4] oxadiazolo – [4,3-a] quinoxalin – 1 – one (ODQ),
tetraethylanmonium, glibenclaminde, 4-aminopyridin, carybdotoxin, apamin,
bradykinin all from Sigma Chemical Co., Saint Louis, MO, USA. Hydroxocobalamin
(Bristol-Myers Squibb),
-Terpineol stock solution was prepared in distilled water and kept at -4o C. -
Terpineol was dissolved in a mixture of distilled water and chremophor and diluted to
the desired concentrations with distilled water just before use. The final concentration
of cremophor in the bath never exceeded 0.01% and had no effect when tested in
control preparations (data not shown). Indomethacin was dissolved in 0.5% w/v
sodium bicarbonate and ODQ was dissolved in DMSO. The other compounds were
freely dissolved in distilled water. The composition of the Tyrode’s solution used was
(mM): NaCl, 158.3; KCl, 4.0; CaCl2, 2.0; MgCl2, 1.05; NaH2PO4, 0.42; NaHCO3, 10.0
and glucose, 5.6.

191
Cell culture
Porcine coronary artery segments were flushed with PBS without calcium to
remove remaining blood. Thereafter, endothelial cells were isolated by collagenase
treatment (type I, Worthington, 1 mg/ml for 12 min at 37 °C), and cultured in culture
dishes containing medium MCDB 131 (Invitrogen) and 15% fetal calf serum
supplemented with penicillin (100 U/ml), streptomycin (100 U/ml), fungizone (250
μg/ml), and L-glutamine (2mM) (all from Cambrex), and grown for 48–72 h, in 24-well
plates. All experiments were performed with confluent cultures of cells used at first
passage. Cells were exposed to serum-free culture medium in the presence of 0.1%
bovine serum albumin (QBiogene) for 6 h prior to treatment.
Western blot analysis
After treatment, cells were washed twice with PBS and then lysed in extraction
buffer (composition inmM: Tris/HCl 20 (pH 7.5; QBiogene), NaCl 150, Na3VO4 1,
sodium pyrophosphate 10, NaF 20, okadaic acid 0.01 (Sigma), a tablet of protease
inhibitor (Roche) and 1% Triton X-100 (QBiogen). Total proteins (20 μg) were
separated on 8% SDS-polyacrylamide (Sigma) gels at 70 V for 2.5 h. Separated
proteins were transferred electrophoretically onto polyvinylidine difluoride
membranes (Amersham) at 100 V for 120 min. Membranes were blocked with
blocking buffer containing 3% bovine serum albumin for p-AMPK, p-Akt and p-eNOS,
Tris buffered saline solution (Biorad) and 0.1% Tween 20 (Sigma) (TBS-T) for 1 h.
For detection of phosphorylated proteins, membranes were incubated with the
respective primary antibody (p-AMPKα Tyr172, p-Akt Ser473 and p-eNOS Ser1177,
Cell Signaling Technology; dilution of 1:1000) overnight at 4 °C. After washing,
membranes were incubated with the secondary antibody (peroxidase-labeled anti–
rabbit IgG, dilution of 1:5000; Cell Signaling Technology) at room temperature for 60
min. Prestained markers (Invitrogen) were used for molecular mass determinations.
Immunoreactive bands were detected by enhanced chemiluminescence
(Amersham). Ponceau staining was performed to verify the quality of the transfer and
equal amounts of proteins in each lane.

192
Determination of NO formation
Bioavailability of NO in the cultured endothelial cells was quantified exposing
cells to -terpineol (10-4 M) for 15 min after pre-incubation with 10 μM DAF-2DA for
30 min at 37 °C. The endothelial cells were also stimulated with bradikinin (BK) (10-5
μM for 15 min before DAF administration. Treatments were performed in triplicate.
The DAF-2DA used in the present study is a fluorescent indicator that enables direct
detection of NO under physiological conditions using flow cytometry 10.
In the present study, the low concentrations of NO released from endothelial
cells under basal conditions could be detected by DAF-2DA, evidenced as a small
increase of fluorescence intensity. To verify whether the fluorescent signal obtained
after the addition of DAF-2DA was dependent on the presence of NO, endothelial
cells were pre-incubated with L-NA (100 mol ⁄ L) for 30 min before the addition of
DAF-2DA and α-terpineol. Samples were analysed by cytometry using CeligoTM
adherent cell cytometer equipment (Cyntellect, San Diego, CA, USA). Data were
analysed by Celigo software. Thus, changes in [NO]i were expressed as F ⁄ F0,
where F is the fluorescence of the sample and F0 is the minimum (basal)
fluorescence. Results are expressed as the mean ± SEM of three independent
experiments performed in triplicate.
Vascular reactivity studies in isolated rat superior mesenteric rings
SHR and Wistar Kyoto rats were euthanized by stunning and bleeding. The
superior mesenteric artery was removed and cleaned from connective tissue and fat.
Whenever appropriated, the endothelium was removed by gently rubbing the intimal
surface of the vessels. Rings (1-2 mm) were obtained and placed in physiological
Tyrode’s solution, maintained to 37oC and gassed with carbogenic mixture (95 % O2
and 5 % CO2) and maintained at pH 7.4. All preparations were stabilized under a
resting tension of 0.75 g for 1 h. The solution was replaced every 15 min to prevent
the accumulation of metabolites11. The force of contraction was isometrically
recorded by a force transducer (Miobath-4, WPI, Sarasota, FL, USA) coupled to an
amplifier-recorder (Miobath-4, WPI, Sarasota, FL, USA) and to a computer equipped
with an analog–to–digital converter board.

193
The presence of functional endothelium was assessed by the ability of
acetylcholine (10 µM) to induce more than 85 % relaxation of vessels pre-contracted
with phenylephrine (10 µM) and the absence, less than 10% of relaxation to
acetylcholine was taken as an evidence that the vessel segments were functionally
denuded of endothelium12. The inhibitors were added 30 minutes before the
application of phenylephrine. In the tonic phase of the second contraction, α-terpineol
(10-12 to 10-5 M) was cumulatively added to preparations until a maximum response
for the addition was observed as indicated by a plateau response (approximately 2-3
minutes). Inhibition was calculated by comparing the response elicited by α-terpineol
before and after the inhibitors or antagonists were added to the preparation.
Experimental protocols
# Effect of α-terpineol on sustained contractions induced by phenylephrine (10 µM) in
isolated preparations of SHR rat mesenteric rings and control normotensive (WKY).
After a stabilization period, rings from SHR and WKY rats with or without
functional endothelium were used in these experiments. Two successive contractions
of similar magnitude were induced by phenylephrine 10 µM, separately. During the
tonic phase of the second contraction, α-terpineol (10-12 – 10-5 M) was cumulatively
added to preparations until a maximum response for the drug was observed as
indicated by a plateau response (approximately 2-3 minutes). The relaxation was
measured by comparing the developed tension before and after addition of α-
terpineol and Emax values were calculated as previously described.
# Influences of NO/cGMP signaling on the vasorelaxant effects of α-terpineol in SHR
and control normotensive (WKY).
The vasorelaxant responses to the test drugs are expressed as a percentage
of the tonic contraction induced by phenylephrine 10 µM. Preparations were exposed
to: a) L-NAME (100 M), a nitric oxide synthase (NOS) inhibitor [13] ; b)
hydroxocobalamin (30 M) a nitric oxide (NO) scavenger [14]; c) ODQ (10M), a

194
soluble guanylate cyclase (sCG) inhibitor [15]; and α-terpineol (10-12 to 10-5 M) was
cumulatively added to preparations until a maximum response.
# Investigation of the putative role of muscarinic receptors, cyclooxygenase, in
endothelial-dependent vasorelaxant effect induced by α-terpineol in SHR rats and
control normotensive.
PHE-induced sustained contractions were obtained in intact rings in both SHR
and WKY rats, previously incubated with atropine (1M) muscarinic receptors [16]
blocker or indomethacin (10 μM) a cyclooxygenase (COX) inhibitor [17], separately.
Then, concentration–response curves to α-terpineol (10-12 – 10-5 M) were obtained.
# K+ channels-Mediated Endothelium-Dependent Vasodilation α-terpineol-induced
PHE-induced sustained contractions were obtained in intact rings previously
incubated with KCl 20mM or TEA, a calcium-activated K+ channels (KCa) blocker [18]
Charybdotoxin (0.2 M) plus apamin (0.2 M) a calcium-activated K+ channels (IKCa
or SKca) blocker [19] Glibenclamide (10 M) KATP blocker, 4-Aminopyridine (1mM), a
voltage activated K+ channels (KV) blocker [20].
Data analysis
Values were expressed as mean ± S.E.M. When appropriate, statistical
significance was determined by one-way ANOVA following Bonferroni’s post-test,
using GraphPad Prism© software, version 5.0 (GraphPad Software Inc., La Jolla,
CA, USA). The maximal relaxation corresponds to the maximum response to PE (10
µM) of the highest concentration used. Values of P<0.05 were considered statistically
significant.

195
RESULTS
# Effect of α-terpineol on sustained contractions induced by phenylephrine (10 µM) in
isolated preparations of SHR rat mesenteric rings.
The chemical structure of α-terpineol is represented in Fig. 1. The effects of α-
terpineol on the cumulative concentration–response curves for phenylephrine on
isolated SHR and WKY rat mesenteric arteries are shown in Fig. 2 and Table 1 for
Emax values. The Emax values for phenylephrine in endothelium-intact or -denuded
rings were depressed in the presence of increasing concentrations α-terpineol (10-12
to 10-5 M) in isolated preparations of SHR rat mesenteric rings and WKY. α-Terpineol
induced vasorelaxation, in a concentration-dependent manner with endothelium-
intact (WKY maximum response to PE (10 µM) = 60 4 or SHR maximum response
to PE (10 µM) = 53.7 ± 3, p<0.05, n=9). After removal of vascular endothelium, the
relaxant response induced by α-terpineol was significantly attenuated for WKY
[maximum response to PE (10 µM) = 20.5 1*] and SHR [maximum response to PE
(10 µM) 16.1 ± 3*, p<0.05, n=8]
Figure 2. Concentration-response curves showing the relaxant effect of α-terpineol (10-12 to 10-5). The response is expressed as a percentage of relaxation in phenyephrine-induced contraction. Each data point represents the mean±s.e.m from
9 experiments. * P 0.05 indicates significant differences between maximum response to PE (10 µM) (one-way ANOVA following Bonferroni’s post-test). Values of
the (▲) WKY: Intact endothelium or ( ) Denuded endothelium; ( ), SHR: Intact
endothelium or ( ) Denuded endothelium. # Influences of NO/cGMP signaling on the vasorelaxant effects of α-terpineol in SHR.

196
Since α-terpineol induced endothelium-dependent relaxation in spontaneously
hypertensive rats or control normotensive isolated mesenteric arteries, an attempt
was made to investigate the endothelium-derived vasoactive factors implicated in this
relaxation. The vasorelaxant responses induced by increasing concentrations of α-
terpineol (10-12 to 10-5 M) were significantly rightward shifted in the presence of NO-
synthase inhibitor (L-NAME 100 M) in SHR and WKY rats. [WKY maximum
response to PE (10 µM) = 18.1 ±3.8 and SHR maximum response to PE (10 µM) =
20.1± 3, p>0.05] (Figure 2 and Table 1).
Figure 3. Concentration-response curves showing the relaxant effect of α-terpineol (10-12 to 10-5). The response is expressed as a percentage of relaxation in phenyephrine-induced contraction. Each data point represents the mean±S.E.M from
8 experiments. p 0.05 indicates significant differences between maximum response to PE (10 µM) (one-way ANOVA following Bonferroni’s post-test). Values of the Intact
endothelium ( ) or ( ) Denuded endothelium, L-NAME (), or Hydroxocobalamin () or ODQ ().
In the presence of hydroxocobalamin (30 μM) for WKY [maximum response to
PE (10 µM) = 23.5 ± 7 and SHR maximum response to PE (10 µM) = 17.3 ± 3 or

197
ODQ (10 μM) for WKY [maximum response to PE (10 µM)= 20.8 ± 1 and SHR
maximum response to PE (10 µM) = 18.1 ± 3*, the relaxation induced by increasing
concentrations of α-terpineol was significantly shifted to the right in a similar
proportion to that obtained in endothelium denuded or L-NAME pre-incubated rings
(Figure 2 and Table 1).
# Investigation of the putative role of muscarinic receptors, cyclooxygenase, in
endothelial-dependent vasorelaxant effect induced by α-terpineol in SHR.
Treatment with cyclooxygenase inhibitor indomethacin (10 μM) for WKY
[maximum response to PE (10 µM) = 61.1 ± 5] and SHR [maximum response to PE
(10 µM) = 53.1 ± 4, p<0.05] in isolated rat superior mesenteric rings with intact
endothelium pre-contracted with phenylephrine (10 μM), had no significant effect on
α-terpineol-induced relaxations. Furthermore, relaxing effect induced by the α-
terpineol was not altered (Figure 4 and Table 2) after pre-incubation of endothelium-
intact rings with atropine (1ηM) for WKY [maximum response to PE (10 µM) = 53.3 ±
8 and SHR maximum response to PE (10 µM) = 41.5 ± 2, a competitive antagonist
for the muscarinic acetylcholine receptor, suggesting muscarinic acetylcholine

198
receptor or that COX-derived products are not involved in the relaxation induced by
α-terpineol
Figure 4. Concentration-response curves showing the relaxant effect of α-terpineol (10-12 to 10-5). The response is expressed as a percentage of relaxation in phenyephrine-induced contraction. Each data point represents the mean±S.E.M from 6 experiments. * P<0.05 indicates significant differences between maximum response to PE (10 µM) (one-way ANOVA following Bonferroni’s post-test). Values of the Intact endothelium after pre-incubation of intact endothelium rings with atropine (1ηM) (), or indomethacin (10 μM) ().
# K+ channels-mediated endothelium-dependent vasodilation α-terpineol-induced

199
PHE-induced sustained contractions were obtained and observed that
vasorelaxant response induced by α-terpineol was reduced in preparations with
endothelium pre-treated with KCl 20mM (efflux modulate) [WKY MR to PE (10 µM) =
23± 4* and SHR MR to PE (10 µM) = 36.4± 6, p<0,05, n=6] or TEA, 1mM, at this
concentration TEA is a non-selective BKCa blocker [WKY [MR to PE (10 µM) = 37.5±
4 and SHR MR to PE (10 µM) = 38.5± 4].
In experiments with charybdotoxin (200M) plus apamin, a blocker of SKCa,
IKCa [WKY MR to PE (10 µM) = 28.6 ± 7 and SHR MR to PE (10 µM) = 35.1 ± 2,
p<0.05, n=6] or Glibenclamide (10 M) KATP blocker [WKY MR to PE (10 µM) = 33± 3
and SHR MR to PE (10 µM) = 24.2± 3*]; or 4-Aminopyridine (1mM), a voltage
activated K+ channels (KV) blocker [WKY MR to PE (10 µM) = 38.7± 1* and SHR MR
to PE (10 µM) = 42.5 ± 2*] the relaxant response induced by α-terpineol was
significantly attenuated (Figure 5 and table 3).

200
Figure 5 Concentration-response curves showing the relaxant effect of α-terpineol (10-12 to 10-5). Values of the Intact endothelium after pre-incubation of intact
endothelium rings with (), A. In the presence of KCl 20mM () or TEA (1mM) () WKY and SHR; or 4-AP (1mM) () or Glibenclamide (10 μM) () and SHR; or Charybdotoxin plus apamin () and SHR.
-12 -11 -10 -9 -8 -7 -6 -5
0
25
50
75
-Terpineol (Log M)
Intact endothelium KCl 20mM
Emax= 23 4
Intact endothelium - Phe 10 M
Emax= 60 4
WKY
TEA (1mM)
Emax=37.5 4
** *
**
%
of
maxim
al re
sp
on
se
-12 -11 -10 -9 -8 -7 -6 -5
0
25
50
75
-Terpineol (Log M)
Intact endothelium KCl 20mM
Emax= 36.4 6 *
Intact endothelium - Phe 10 M
Emax= 53.7 3
SHR
TEA (1mM)
Emax= 38.5 4*
**
*
*
%
of
maxim
al re
sp
on
se
-12 -11 -10 -9 -8 -7 -6 -5
0
20
40
60
-Terpineol (Log M)
4-AP 1mM
Emax= 38.7 1*
Intact endothelium - Phe 10M
Emax= 60 4
WKY
Glibenclamide 10 M
Emax = 33 3*
**
**
*
*
%
of
maxim
al re
sp
on
se
-12 -11 -10 -9 -8 -7 -6 -5
0
25
50
75
-Terpineol (Log M)
4-AP 1mM
Emax= 42.5 2*
Intact endothelium - Phe 10 M
Emax= 53.7 3
SHR
Glibenclamide 10 M
Emax= 24.2 3*
**
**
*
**
**
*
%
of
maxim
al re
sp
on
se
-12 -11 -10 -9 -8 -7 -6 -5
0
25
50
75
-Terpineol (Log M)
Charybdotoxin (0.2M) + Apamin (0.2M)
Emax= 28.6 7
Intact endothelium - Phe 10M
Emax= 60 4
WKY
* * * * **
*
%
of
maxim
al re
sp
on
se
-12 -11 -10 -9 -8 -7 -6 -5
0
25
50
75
-Terpineol (Log M)
Charybdotoxin (0.2M) + Apamin (0.2M)
Emax= 35.1 2 *
Intact endothelium - Phe 10 M
Emax= 53.7 3
SHR
**
**
*
*
%
of
maxim
al re
sp
on
se

201
# α-Terpineol and insulin causes the activation of eNOS
Experiments were performed to determine whether this signaling pathway is
also involved in α-terpineol-induced NO-mediated relaxations in mesenteric arteries
are critically dependent eNOS activation. Unstimulated endothelial cells had no
expression of p-eNOS, α-terpineol increased within 5 min signal of p-eNOS and,
thereafter, this signal evolved differentially, returned to baseline at 180 min. For
positive control we observed that insulin-stimulated conditions by p-eNOS Ser 1177
(Fig 6 Fig 7).
A
B
Figure 6. Insulin caused a time-dependent phosphorylation of eNOS at Ser1177 (A) and (B) dose-dependent phosphorylation of eNOS and pAKT.
Figure 7 α-Terpineol caused a time-dependent phosphorylation of eNOS at Ser1177 and total eNOS

202
# Role of protein kinase AKT in α-terpineol-induced eNOS activation
To better characterize the signaling pathway involved in eNOS activation in
response to α-terpineol, levels of p-Akt and p-eNOS were assessed in endothelial
cells by immunoblotting. α-Terpineol increased within 5 min signals of p-Akt and p-
eNOS and, thereafter, these signals evolved differentially. Compared to vehicle
stimulation, insulin-evoked robust increases in p-Akt S473 and p-eNOS S1177 5, 30,
60 and 180 min, associated the α-terpineol-induced effect.
Figure 8: α-Terpineol caused a time-dependent phosphorylation of eNOS and pAKT. Representative traces of 4 separate experiments performed in triplicate. Bar graphs showing the effects of α-terpineol (10-4 M) in time-course (5 min- 180 min).

203
In addition, was assessed dose-response to α-terpineol to eNOS activation in
response in endothelial cells by immunoblotting. Compared to vehicle stimulation,
insulin-evoked robust increases in levels of p-eNOS S1177 and p-AKT S473. α-
Terpineol increased within 30 min signals in concentration-dependents of p-Akt and
p-eNOS and, thereafter, these signals evolved differentially.
Figure 9: α-Terpineol caused a time-dependent phosphorylation of eNOS and pAKT. Representative traces of three separate experiments performed in triplicate. Bar graphs showing the effects of α-terpineol (10-4 M) in time-course (5 min- 180 min).

204
# Role of protein kinase AMPK in α-terpineol-induced eNOS activation
Indeed, phosphorylation of pAMPKα was an early and transient event, which
reached a peak value within 15 min and then returned to baseline at 30 min. In
contrast, the level of p-Akt and p-eNOS was detected after 5 min and then increased
steadily until 60 min. These data indicate that α-terpineol, act on upstream mediators
of the activation of the PI3-kinase/Akt pathway and AMPK leading to eNOS
phosphorylation.
Figure 9 α-Terpineol caused a time-dependent phosphorylation of eNOS and pAKT. Representative traces of three separate experiments performed in triplicate. Bar graphs showing the effects of α-terpineol (10-4 M) in time-course (5 min- 180 min).

205
# α-Terpineol stimulates the formation of NO in endothelial cells
Next, experiments were performed to provide direct evidence that α-terpineol
induces NO formation in porcine coronary artery endothelial cells using flow
cytometry. Exposure of cells to α-terpineol induced about a 1.5-fold increase in the
formation of NO (Fig. 10). The stimulatory effect was abolished by L-NA.
Figure 10: Nitric oxide (NO) generation by a rabbit aorta endothelial cell line (10-6 cells⁄mL) was estimated using diaminofluoresceindiacetate (DAF-2DA). Representative traces of three separate experiments performed in triplicate. Bar graphs showing the effects of BK (positive control), α-terpineol (10-4 M) alone, and in
the presence of 100μM L-NAME, p 0.05.
M-4
Bra
dikin
in 1
0M-4
-terp
ineo
l 10
M-4
-terp
ineo
l 10
L-NA +
0
20
40
60
NO
Rele
ase (
Flu
ore
sce
nce,
%)

206
DISCUSSION
In this report, we sought to clarify the underlying mechanisms by which α-
terpineol elicits its vasodilation in spontaneously hypertensive rats (SHR) and
normotensive control (WKY). The major findings of this work were that the
monoterpene α-terpineol induces decrease of peripheral vascular resistance
mediated by increases in NO release and consequently activation of the NO-GMPc
pathway, EDHF and K+ channels participation activation in spontaneously
hypertensive rats and their normotensive controls.
The vascular endothelium, releasing nitric oxide and endothelium- derived
hyperpolarizing factors (EDHFs), is known to play an important role in regulating the
tone of arterial resistance vessel. Essential hypertension is characterized by impaired
endothelium-dependent vasodilation as the result of a reduction in NO oxide
availability. Through the activation of NO synthase, α-terpineol enhances the release
of NO from the endothelium and induces a relaxation of the vascular smooth muscle
cell in normotensive rats [9].
Thus, we performed experiments in isolated superior mesenteric arteries of
the spontaneously hypertensive rats (SHR) and normotensive control (WKY). We
found that under this controlled conditions, α-terpineol induced vasorelaxation that
was significantly attenuated after removal of the functional endothelium.
In order to investigate whether the vasodilator effect of α-terpineol is
dependent on NO-cGMP and/or endothelium derived hyperpolarizing factor (EDHF)
pathways, in this way contribute to the relaxing effect verified in our experiment. The
present study suggests that the vasodilator effect of the α-terpineol partially depends
on the release of NO from the endothelial cells, in presence of a NOS inhibitor and a
NO scavenger the concentration-response curves to α-terpineol were shifted to the
right, suggesting that EDRFs (at least NO) play an important role in the α-terpineol-
induced vasorelaxant response. In contrast, infusion of the NOS inhibitor (L-NAME)
plus L-arginine decreased the vasorelaxation produced by α-terpineol, suggesting
that L-arginine, in the presence of a NOS inhibitor, improves NO-dependent
vasorelaxation in isolated superior mesenteric arteries of the spontaneously
hypertensive rats (SHR) and Wistar Kyoto normotensive control (WKY). Moreover,
the present findings provide also direct evidence that α-terpineol activates eNOS as
indicated by the L-NAME sensitive formation of NO and the enhanced

207
phosphorylation of eNOS at Ser1177 in endothelial cells. These data corroborate
with Ribeiro et al. (2010) with mesenteric arteries of Wistar rats and Magalhães et al.
(2008) where α-terpineol-evoked vasorelaxation were also significantly reduced by L-
NAME in rat mesenteric vascular bed preparations. The latter effect is a novel finding
that may be important to the understanding of monoterpenes biological activity.
Interestingly, α-terpineol induced p-eNOS S1177 to total eNOS increased
phosphorylation maximal between 30 and 60 min in cultured endothelial cells.
Additional eNOS phosphorylation sites that are specifically activated by AMPK and
AKT were also evaluated. These data suggest that in our experimental setting, eNOS
might be preferentially phosphorylated by AKT but not by AMPK mediated signalling.
These data demonstrated that signalling kinases are important upstream activators of
phosphorylation of eNOS S1177 α-terpineol-induced in endothelial cells.
Vascular NO dilates all types of blood vessels by stimulating soluble guanylyl
cyclase and increasing cGMP in smooth muscle cells22 and subsequent cGMP-
dependent protein kinase (PKG) activation23. However, NO has been proposed to
mediate a variety of effects via cGMP-independent mechanisms24. Therefore, in
order to verify the participation of NO/GMPc pathway, we incubated the preparations
with ODQ. Under this condition, the concentration-response curve to α-terpineol was
shifted to the right, suggesting that the relaxant response elicited by the α-terpineol
involves the NO/sGC/GMPc pathway (Figure 3 and Table 1).
Furthermore, after its synthesis and release, NO diffuses to adjacent smooth
muscle cells and causes them to relax22. Therefore, many studies have been
performed to directly measure vascular relaxation elicited by natural products and
found that the vasorelaxant effect is related to stimulation of NO release from
vascular tissues9,25-26.
Our results suggest that the cardiovascular effects induced by α-terpineol
could be partially mediated by activation of eNOS and consequently NO production.
To assess whether enhanced NO release by α-terpineol was associated to the
activation of muscarinic receptors, the effects of atropine on the endothelium-
dependent relaxation response to α-terpineol were investigated. Thus, pre-incubation
of the mesenteric rings with atropine did not affect the vasorelaxation induced by α-
terpineol. These findings indicated that the α-terpineol-induced vascular relaxation
does not involve the activation of muscarinic receptors in the vasculature. (Figure 4
and Table 2).

208
It is reported in the literature that the endothelium-dependent vasorelaxant
response may also involve the release of COX-derived products, such as PGI2, via
the COX pathway. To determine if the vasorelaxant effect induced by α-terpineol
involves COX metabolites, we incubated the preparations with 10 µM indomethacin.
In this condition the relaxation induced by increasing concentrations of α-terpineol
was not affected, suggesting that COX-products are not involved in the vasorelaxant
response induced by α-terpineol. (Figure 4 and Table 2).
The role of K+ channels in the nitric oxide-induced vasorelaxation has been
largely investigated in resistance vessels [27,28]. Moreover, K+ channels play an
important role in the regulation of contractility and vascular tone [18]. In most cases,
the vasorelaxation mediated by membrane hyperpolarization is attributed to the rise
in K+ permeability. Therefore, hyperpolarization of the endothelium membrane
elevates [Ca2+]i by an increase in Ca2+ influx that induces relaxation of the underlying
smooth muscle [29] through endothelium-derived hyperpolarizing factors (EDHFs) and
the generation of nitric oxide and prostacyclin. Several types of potassium channels
have been proposed to regulate endothelial membrane potential, including large
conductance, BKCa, Kir, SKCa and IKCa channels[18]. KATP, KV which can be blocked by
glibenclamide and 4-AP, respectively.
In this context, α-terpineol -induced vasorelaxation curve was right shifted in the
presence of KCl (20 mM), suggesting a role for K+ channels activation in
spontaneously hypertensive rats and normotensive control. Therefore, we further
investigated the effect of α-terpineol in spontaneously hypertensive rats and
normotensive control mesenteric rings with intact endothelium in the presence of
glibenclamide (10 µM), a potassium channel ATP-sensitive (KATP) blocker. Under this
experimental condition, glibenclamide attenuated the vasorelaxation induced by α-
terpineol. It has been reported in the literature that the subtype of K+ channels that
plays a role in NO-GMPc relaxation pathway is the KATP in most arteries [18].
In addition, the nitric oxide pathway has been shown to activate calcium-
activated K+ channels (KCa) in mesenteric arteries. The KCa channels are classified by
their conductances as follows: BKCa, IKCa and SKCa channel [32-33]. In the present
experiments, were used TEA, sensitive to all BKCa channels, apamin to SKCa
channels and charybdotoxin to IKCa channels. SKCa and IKCa channels in vascular
endothelium appear to have particularly prominent roles, since inhibition of these
channels prevents EDHF mediated vasodilation [1, 18, and 28]. In our experiments,

209
treatment with TEA (1 mM) and charybdotoxin plus apamin (0.2μM) produced a shift
to the right of the concentration–response curves for α-terpineol, suggesting a role for
BKCa, IKCa, SKCa channels endothelium-dependent in spontaneously hypertensive
rats and normotensive control (Figure 5; Table 3).
In conclusion, using combined functional and pharmacological approaches, we
have demonstrated that, α-terpineol produces vasorelaxation in both SHR and WKY
rats, mediated by the endothelium via activation of AKT and AMPK upstreams
pathway to eNOS phosphorylation and increase of NO levels and consequential NO-
GMPc pathway. In addition, we indicate that effect endothelium-dependent induced
by α-terpineol evokes, at least, EDHF production and potassium channel activation.
Altogether, these findings should provide convincing evidence that α-terpineol uses
several signal transduction pathways to enhance the endothelial formation of NO,
and hence to increase the protection of the vascular system. This vascular activation
has potential benefits including (1) improved endothelial function via greater
vasodilatation of resistance arteries and (2) analyses performed in cultured cell
systems must be validated in vivo models in order to more fully delineate the
endothelial dysfunction in normal physiology and in disease states, such
hypertension.
ACKNOWLEDGEMENTS
The authors wish to express their sincere thanks to José Crispim Duarte, Evelyne
Lacoffrette, Dr. Christian Müller and collaborators for technical assistance. This work
was funded by CAPES and CNPq-Brazil.

210
REFERENCES
1. Félétou, M. Vanhoutte, P.M., Endothelial dysfunction: a multifaceted disorder, Am.
J. Physiol., Heart Circ. Physiol. 2006. 291: H985–H1002
2. Török J. Participation of nitric oxide in different models of experimental
hypertension. Physiol Res. 2008;57(6):813-25.
3. Chang HR, Lee RP, Wu CY, Chen HI. Nitric oxide in mesenteric vascular
reactivity: a comparison between rats with normotension and hypertension. Clin
Exp Pharmacol Physiol. 2002 Apr;29(4):275-80
4. Fleming I. Molecular mechanisms underlying the activation of eNOS. Pflugers
Arch. 459, 793–806, 2010.
5. Edris, A. E.; Pharmaceutical and therapeutic potentials of essential oils and their
individual volatile constituents: a review. Phytother. Res.,21, 308-323, 2007.
6. Santos, M. R. V.; Moreira, F. V.; Fraga, B. P.; DE Sousa, D. P.; Bonjardim, L. R.;
Quintans-Junior, J. L. Cardiovascular effects of monoterpenes: a review. Braz. J.
Pharmacognosy, 21(4): 764-771, 2011.
7. Bastos JF, Moreira IJ, Ribeiro TP, Medeiros IA, Antoniolli AR, De Sousa DP,
Santos MR. Hypotensive and Vasorelaxant Effects of Citronellol, a Monoterpene
Alcohol, in Rats. Basic Clin. Pharmacol. Toxicol. 2010. 106 (4) 331 - 337.
doi.10.1111/j.1742-7843.2009.00492.x
8. Magalhães PJC, Criddle DN, Tavares RA, Melo EM, Mota TL, Leal-Cardoso JH.
Intestinal myorelaxant and anti-spasmodic effects of the essential oil of Croton
nepetaefolius, and its constituents cineole, methyl-eugenol and terpineol.
Phytother. Res. 1998; 12: 172–177.
9. Ribeiro TP, Porto DL, Menezes CP, Antunes AA, Silva DF, De Sousa DP et al.
Unraveling the cardiovascular effects induced by alpha-terpineol: a role for the
NO-cGMP pathway. Clin Exp Pharmacol Physiol. 2010; 37(8): 811-6. doi:
10.1111/j.1440-1681.2010.05383.x.
10. Nakatsuboa N, Kojimaa H, Kazuya K, Nagoshib H, Hiratab Y, Maedaa D, Imaia Y,
Irimuraa T, Naganoa T. Direct evidence of nitric oxide production from bovine
aortic endothelial cells using new fluorescence indicators: diaminofuoresceins.
FEBS Letters 1998; 427: 263–266
11. Altura BM, Altura BT. Differential effects of substrate on drug-induced
contractions of rabbit aorta. Am. J. Physiol., 1970; 219: 1698-705.

211
12. Furchgott FF, Zawadzki JV. The obligatory role of endothelial cells in the
relaxation of arterial smooth muscle by acetylcholine. Nature. 1980; 288: 373-376.
13. Moncada S, Higgs EA. The L-arginine - nitric oxide pathway. N. Engl. J. Med.
1993; 29: 2002 – 2012.
14. Kruszyna H, Magyar JS, Rochelle LG, Russel MA, Smith RPE, Wilcox DE.
Spectroscopic Studies of Nitric Oxide (NO) Interations with Cobalamins: Reaction
of NO with Supéroxocobalamin(III) Likely Accounts for Cobalamin Reversal of the
Biological Effects of NO. J. Phamacol. Exp. Ther. 1998; 285: (2) 665-671.
15. Garthwaite, J.; Southam, E.; Boulton, C.L.; Nielsen, E.B.; Schmidt, K.; Mayer, B.
Potent and selective inhibition of nitric oxide-sensitive guanylyl cyclase by 1H-
[1,2,4]oxadiazolo[4,3-a]quinoxalin-1-one. Mol. Pharmacol. 1995; 48: 184-188.
16. Caulfield MP, Birdsall NJ. International Union of Pharmacology. XVII.
Classification of muscarinic acetylcholine receptors. Pharmacol. Rev. 1998; 50:
(2) 279–90.
17. Vanhoutte PM. COX-1 and Vascular Disease. Clin. Pharmacol. Ther., 2009; 86:
(2) 212–215.
18. Zhou E, Qing D, Li J. Age-associated endothelial dysfunction in rat mesenteric
arteries: roles of calcium-activated K(+) channels (K(ca)). Physiol Res. 2010;
59(4):499-508.
19. Garland CJ. Compromised vascular endothelial cell SK(Ca) activity: a
fundamental aspect of hypertension? Br J Pharmacol. 2010;160(4):833-5.
20. Nelson MT, Quayle JM. Physiological roles and properties of potassium channels
in arterial smooth muscle. Am J Physiol 1995; 268, C799–C822.
21. Magalhães PJC, Lahlou S, Juca DM, Coelho-de-Souza LN, Frota PTT, Costa
AMG, Leal-Cardoso JH. Vasorelaxation induced by the essential oil of Croton
nepetaefolius and its constituents in rat aorta are partially mediated by the
endothelium. Fund. Clin. Pharmacol. 2008; 22: 169–177
22. Rajapakse N, Mattson DL. Role of L-arginine in nitric oxide production in health
and hypertension Clin. Exper. Pharmacol. Physiol. 2009; 36: 249–255.
23. Alioua A, Tanaka Y, Wallner M, Hofmann F, Ruth P, Meera P, Toro L. The large
conductance, voltage-dependent, and calcium-sensitive K+ channel, Also, is a
target of cGMP-dependent protein kinase phosphorylation in vivo. J. Biol. Chem.
1998; 273: 32950–32956.

212
24. Moncada S, Palmer R, Higgs EA. Nitric oxide: physiology, pathophysiology, and
pharmacology (Review). Pharmacol. Rev. 1991; 43: 109–142.
25. Luciano MN, Ribeiro TP, de França-Silva MD, do Nascimento RJ, de Jesus
Oliveira E, França KC, Antunes AA, Nakao LS, Aita CA, Braga VA, de Medeiros
IA. Uncovering the vasorelaxant effect induced by Vale do São Francisco red
wine: A role for nitric oxide. J Cardiovasc Pharmacol. 2011 Mar 9. doi:
10.1097/FJC.0b013e318217db1f.
26. Cavalcante, H.M., Ribeiro, T.P., Silva, D.F., Nunes, X.P., Barbosa-Filho, J.M.,
Diniz, M.F. Correia, NA, Braga, VA, Medeiros, IA. 2011. Cardiovascular Effects
Elicited by Milonine, a New 8,14-Dihydromorphinandienone Alkaloid. Basic Clin.
Pharmacol. Toxicol 108(2):122-30. doi: 10.1111/j.1742-7843.2010.00631.x..
27. Bolotina VM, Najibi S, Palacino JJ, Pagano PJ, Cohen RA. Nitric oxide directly
activates calcium-dependent potassium channels in vascular smooth muscle.
Nature 1994; 28, 850–853.
28. Mistry DI, Garland CJ. Nitric oxide (NO)-induced activation of large conductance
Ca2+ -dependent K+ channels (BKCa) in smooth muscle cells isolated from the
rat mesenteric artery. Br J Pharmacol 1998;124: 1131–1140.
29. Crane GJ, Gallagher N, Dora KA, Garland CJ. Small- and intermediate-
conductance calcium-activated K+ channels provide different facets of
endothelium-dependent hyperpolarization in rat mesenteric artery. J Physiol 553:
183–189, 2003.
30. Brayden JE, Nelson MT. Regulation of arterial tone by activation of calcium-
dependent potassium channels. Science 1992; 256: 532−535.