UNDB – Engenharia Civil Disciplina: Mecânica dos Solos II Prof. Jean Mark.
Mecânica Quântica Equação de Schrödinger - Autenticação · Equação de Schrödinger ......
Transcript of Mecânica Quântica Equação de Schrödinger - Autenticação · Equação de Schrödinger ......

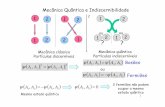
Dualidade onda-corpúsculo
Princípio de incertezade Heisenberg
Mecânica Quântica
Equação de Schrödinger
( )∂∂
∂∂
∂∂
π2
2
2
2
2
2
2
28
0Ψ Ψ Ψ
Ψx y z
mh
E V+ + + − =
H Ψ = E Ψ

EQU
AÇ
ÃO
DE
SCH
RÖ
DIN
GER
“Construção” da equação de SchrödingerMecânica ondulatória para partículas
( ) ( )txsenAtx v2, ±=Ψλπ
v = λ × ν
Equação de uma onda
( ) xsenAxλπ2
=Ψ
Onda estacionária
( )
( ) xsenAdx
xd
xcosAdx
xd
λπ
λπ
λπ
λπ
24
22
2
2
2
2
−=Ψ
=Ψ
( ) ( )xdx
xdΨ−=
Ψ2
2
2
2 4λπ
λ

EQU
AÇ
ÃO
DE
SCH
RÖ
DIN
GER
vmh
=λcomp. de onda de de Broglie(dualidade onda-corpúsculo)( )
Ψ−=Ψ
2
2
2
2 4λπ
dxxd
22
22
vmh
=λ ( )Ψ−=
Ψ2
222
2
2 v4hm
dxxd π
( )2
2
2
222 1
4v
dxxdhm Ψ
Ψ−=
π( )2
2
2
222 182
vdx
xdm
hm
m ΨΨ
−=π
mmmT2
vv21 22
2 ==( )2
2
2
2 18 dx
xdm
hT ΨΨ
−=π
E = T + V ( ) Vdx
xdm
hE +Ψ
Ψ−= 2
2
2
2 18π
( ) 018 2
2
2
2
=−+Ψ
ΨVE
dxxd
mhπ
( ) ( ) 082
2
2
2
=Ψ−+Ψ VE
hm
dxxd π

EQU
AÇ
ÃO
DE
SCH
RÖ
DIN
GER
Erwin Schrödinger,1887-1961
E = T + V
Ψ(x,y,z) Função de ondaE Energia total=Valor próprioV Operador Energia PotencialT Operador Energia CinéticaH = T + V Operador Hamiltoniano
H Ψ = E ΨH Ψ = E Ψ
( )∂∂
∂∂
∂∂
π2
2
2
2
2
2
2
28
0Ψ Ψ Ψ
Ψx y z
mh
E V+ + + − =
vmh
=λ ( ) xsenAxλπ2
=Ψ

Como o fenómeno em estudo tem simetria esférica, é mais adequado usar coordenadas polares esféricas do que coordenadas cartesianas
x = r senθ cosϕy = r senθ senϕ
z = r cosθ
x2 + y2 + z2 = r2
EQU
AÇ
ÃO
DE
SCH
RÖ
DIN
GER
X
Y
Z
x
y
z
θ
ϕ
r
αα
αα
sensen
coscos
⋅=→=
⋅=→=
cbcb
caca
αa
bc
r senθ
r senθ

( )∂∂
∂∂
∂∂
π2
2
2
2
2
2
2
28
0Ψ Ψ Ψ
Ψx y z
mh
E V+ + + − =Á
TOM
O d
e H
x,y,zΨ (x,y,z)
r,θ,ϕΨ (r,θ,ϕ)
reV
o
2
41επ
−=
04
18111 2
2
2
22
2
222
2 =Ψ⎟⎟⎠
⎞⎜⎜⎝
⎛++⎟⎟
⎠
⎞⎜⎜⎝
⎛ Ψ+
Ψ+⎟⎟
⎠
⎞⎜⎜⎝
⎛ ΨreE
hmsen
senrsenrrr
rr oπεπ
θ∂∂θ
∂θ∂
θϕ∂∂
θ∂∂
∂∂
Ψ (r,θ,ϕ) = R(r) Θ(θ) Φ(ϕ)

4444444 34444444 21
4444444 84444444 76
λ
λ
ϕθθθ
θθπεπ
=
=
ΦΦ
−⎟⎠⎞
⎜⎝⎛ Θ
Θ−=⎟⎟
⎠
⎞⎜⎜⎝
⎛++⎟
⎠⎞
⎜⎝⎛
cte
cte
o dd
senddsen
dd
senr
reE
hm
drdRr
drd
R 2
2
22
2
2
22 11
4181
1 8 14
22
2
22
Rddr
rdRdr
mh
Eer
ro
⎛⎝⎜
⎞⎠⎟ + +
⎛⎝⎜
⎞⎠⎟ =
ππε
λ R(r), função radial
− ⎛⎝⎜
⎞⎠⎟ − =
1 12
2
2ΘΘ
ΦΦ
send
dsen
dd sen
ddθ θ
θθ θ ϕ
λ
sen dd
sendd
dd
senθ
θθ
θ ϕλ θ
ΘΘ
ΦΦ⎛
⎝⎜⎞⎠⎟ + = −
1 2
22
sen dd
sendd
sendd
cte m cte m
θθ
θθ
λ θϕΘ
ΘΦ
Φ⎛⎝⎜
⎞⎠⎟ + = −
= =
22
2
2 2
1
1 244444 344444 1 24 34
sen dd
sendd
sen mθ
θθ
θλ θ
ΘΘ⎛
⎝⎜⎞⎠⎟ + =2 2
dd
m2
22ΦΦ
ϕ= −
Θ(θ)
− =1 2
22
ΦΦd
dm
ϕ
Φ(φ) Funções angulares

dd
m2
22ΦΦ
ϕ= −
ϕimek ⋅=Φ
ϕ
ϕimekmi
dd
=Φ
321Φ=
−=Φ ϕ
ϕimekm
dd 2
2
2
dd
m2
22ΦΦ
ϕ= −
Equa
ção
em Φ
( ) ( )πϕϕ 2+Φ=Φ
( )e eim imϕ ϕ π= +2
= e eim imϕ π2
m = ?
Condição limite:Φ unívoca
eim2 1π =
( ) ( )cos m isen m2 2 1π π+ =6 74444 84444
m = 0, ou nº inteiro!Número quântico!
X
Y
Z
x
y
z
θ
ϕ
r

1 8 14
22
2
22
Rddr
rdRdr
mh
Eer
ro
⎛⎝⎜
⎞⎠⎟ + +
⎛⎝⎜
⎞⎠⎟ =
ππε
λN
úmer
os q
uânt
icos
: n, ℓ
, me
s( )rR ln,
sen dd
sendd
sen mθ
θθ
θλ θ
ΘΘ⎛
⎝⎜⎞⎠⎟ + =2 2
dd
m2
22ΦΦ
ϕ= −
( )θml ,Θ
( )ϕmΦ
( ) ( ) ( ) ( )ϕθϕθ mmllnmln rRr Φ×Θ×=Ψ ,,,, ,,
( ) ( ) ( )ϕθϕθ ,,, ,,,, mllnmln YrRr ×=Ψ
n = 1,2,3, … ,n, … (principal)ℓ = 0,1,2, …, (n-1) (azimutal ou angular)m = - ℓ,(- ℓ+1), … ,0, … ,(ℓ-1),+ℓ (magnético)s = -½ ou +½ (spin)

Orb
itais
e p
roba
bilid
ade
Ψ2
( )ϕθ ,,,, rmlnΨ “Orbital”
ℓ = 0 1 2 3 4s p d f g
sharpprimary
diffusefundamental
( )∫ =Ψ 1,,,,2 dVrmln ϕθ
( )ϕθ ,,,,2 rmlnΨ probabilidade
normação
( )ϕθ ,,2 rΨ → “densidade” de probabilidade → num ponto: (r,θ,ϕ) ou (x,y,z)
( )dVr ϕθ ,,2Ψ → probabilidade → num elemento de volume dV

( ) 02
0
23
00,2 2
221 a
rZ
ea
rZaZrR
−
⎟⎟⎠
⎞⎜⎜⎝
⎛−⎟⎟
⎠
⎞⎜⎜⎝
⎛⎟⎠
⎞⎜⎝
⎛= ( ) 02
0
23
01,2 62
1 aZr
ea
rZaZrR
−
⎟⎟⎠
⎞⎜⎜⎝
⎛⎟⎠
⎞⎜⎝
⎛=
Å529,02
20
0 ==em
ha
πε
Funções radiais, Rn,l(r)
( ) 023
00,1 2 a
rZ
eaZrR
−
⎟⎟⎠
⎞⎜⎜⎝
⎛=
nodo(sup. nodal)
2s1s 2p

)(20,2 rR
)(0,2 rR
)(1,2 rR)(2
1,2 rR
Densidade de Probabilidade
Corrigir para o elemento de volume, dV
2s
2p

dr
dV
r
R2(r)dV = ?
drrdV
rdrdV
rV
2
2
3
4
4
34
π
π
π
=
=
=
R2(r)dV = 4 π r2 R2(r)dr
(coroa esférica)

)(20,2 rR)(0,2 rR
)(1,2 rR)(2
1,2 rR
)(4 20,2
2 rRrπ
)(4 21,2
2 rRrπ
2s
2p

)(0,1 rR)(4 2
0,12 rRrπ
Orbital 1s
Máximo de probabilidade == raio de Bohra0 = 0.529 Å

)(0,3 rR )(4 20,3
2 rRrπ
)(1,3 rR
)(2,3 rR
)(4 21,3
2 rRrπ
)(4 22,3
2 rRrπ
3s
3p
3d
n = 3
Número de nodos: n - ℓ - 1
“penetrabilidade” das orbitais:s > p > d

21
0,0 41
⎟⎠⎞
⎜⎝⎛=Υ
π
zp=⎟⎠⎞
⎜⎝⎛=Υ θ
πcos
43 2
1
0,1
ϕθπ
ie±± ⎟
⎠⎞
⎜⎝⎛=Υ sen
83 2
1
1,1
Função angular, Yl,m(θ,φ)
orbitais s orbitais p
ϕθπ
cossen43)(
21 2
1
1,11,1
21
⎟⎠⎞
⎜⎝⎛=+⎟
⎠⎞
⎜⎝⎛= −YYpx
ϕθπ
sensen43)(
21 2
1
1,11,1
21
⎟⎠⎞
⎜⎝⎛=−⎟
⎠⎞
⎜⎝⎛−= −YYipy
Forma e orientação das orbitais
Combinações lineares

21
0,0 41
⎟⎠⎞
⎜⎝⎛=Υ
π
orbitais s
Independentes de θ e de φ esféricas
X
Y
Z
x
y
z
θ
ϕ
r
x
yz
x
y
z

X
Y
Z
x
y
z
θ
ϕ
rθ
x
y
z
θπ
cos43 2
1
⎟⎠⎞
⎜⎝⎛=zp
orbitais p z
y
x
x
y
z
+-x
y
z
+-
x
y
z
+
-
x
y
z
+-x
y
z
+- x
y
z
+
-
px py pz

x
y z
− ++−
x
yz
−+
+−
x
yz
−+
+−
x
yz
− +
+ −
x
yz
−
+
+
x
yz
+−+
x
yz
++ −
−x
yz
++ −−
x
yz
+
+ −
−
x
yz
++ −−
dx2-y2 dxydyz dxz dz2
orbitais d

Representação gráfica de orbitaisNuvem electrónica
Contornos exteriores
Superfícies de isoprobabilidade1s 2s
2p2p
2p 3p
Representação esquemática
x
y
z
s px pypz
dz2 dx2-y2 dxy dxz dyz

A
B
x
y
z
+
+
A
B
x
y
z
+
-
z
x
A
B
B'
A'
-+
+-
antissimétricas (u)orbitais fsimétricas (g)orbitais dantissimétricas (u)orbitais psimétricas (g)orbitais s
Simetria das orbitais(centro de simetria)
geradeungerade

Energia das orbitais (átomo de H)
H Ψ = E Ψ
∫ ∫ Ψ=ΨΨ dVEdVH 2
∫∫
Ψ
ΨΨ=
dV
dVHE
2
20
2
24
2 81
ε−=
hZme
nE
= modelo de Bohr(só depende de n)