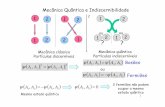
ESTRATÉGIAS TERAPÊUTICAS TOP-DOWN / STEP...
Transcript of ESTRATÉGIAS TERAPÊUTICAS TOP-DOWN / STEP...
Antivíricos
Exemplos da inibição da penetração nas células hospedeiras:amantidina (inibe a descapsulação do vírus da influenza), globulinas
γ, palivizumab (anti-RSV)
AntivíricosExemplos de inibidores da transcríptase reversa por análogos dos
nucleosídeos e nucleotídeos: abacavir, adefovir, didanosina, estavudina, lamivudina, tenofovir, zalcitabina, zidovudina
AntivíricosExemplos de inibidores da transcríptase reversa não-nucleosídicos:
delavirdina, efavirenz, nevirapina
Antivíricos
Exemplos de inibidores da polimérase do ADN: nucleosídicos (aciclovir; ganciclovir; vidarabina) e não-nucleosídicos (foscarnet)
AntivíricosExemplos de inibidores da protease do HIV: amprenavir, indinavir,
nelfinavir, ritonavir, saquinavir
Aciclovir
Análogo acíclico da guanosina Actividade limitada para a família dos Herpetoviridae
herpes simplex vírus (HSV) tipo 1 e 2 varicella-zoster (VZV)Epstein-Barr (In vitro)citomegalovirus (CMV) (In vitro)
Aciclovir
Aciclovir Aciclovir-MP
Aciclovir-DP
Aciclovir-TP
Timidina cínase víricacínase celular
cínase celular
Polimerase vírica Síntese do ADN vírico
Aciclovir
Resistência:Vírus deficientes em TKAlteração da afinidade para o substractoPolimerase do ADN
Virus resistentes:herpes simplex causadores de pneumonia, encefalite, infecções mucocutâneas em imunodeprimidos.
6% HSV em doentes HIV são resistentes
VZV resistentes em doentes infectados com HIV
Aciclovir
Resistências cruzadas com:ValaciclovirFanciclovirGanciclovir
Sem resistências :FoscarnetCidofovirTrifluridina
Aciclovir
Recomendações terapêuticas – toma oral :
primeiro episódio de herpes genital herpes genital recorrenterecorrência genital crónica (>6 episódios/ano)
proctite herpéticavaricelazona
Aciclovir
Recomendações terapêuticas – intravenoso:
HSV graveencefalite herpéticainfecção HSV neonatalvaricela e zona em imunodeprimidos
Aciclovir
Efeitos laterais:
Disfunção renal – 5-10%
Agitação, letargia, sonolência, alucinaçõestrémulo, psicoses, convulsões e coma
Aumento de enzimas hepáticas
Queimaduras, prurido e eritema
Valaciclovir
L-valil éster do aciclovir
Convertido em aciclovir (conversão enzimática)
Elevados níveis séricos de aciclovir
Indicações terapêuticas semelhantes às do aciclovir
Microangiopatia trombótica
Penciclovir
Análogo acíclico da guanosina
Mecanismo de acção semelhante ao do aciclovir
Semivida intracelular > aciclovir
Trifosfato de penciclovir < afinidade polimérase vírica que o trifosfato de aciclovir
Bem tolerado na aplicação tópica
Penciclovir
Resistência:
Vírus deficientes em timidina cínase (TK)Perda de afinidade da polimérase do ADN
Resistência cruzada com o aciclovir
Fanciclovir
Pró-fármaco do penciclovir
Mecanismo de acção semelhante ao do aciclovir
Indicações terapêuticas semelhantes às do aciclovir
Análogo acíclico da guanosina
Também requer trifosforilação para activaçãomas não depende da TK para a fosforilação inicial
Inibe a polimérase do ADN
Actividade contra CMV,HSV,VZV,EBV
Ganciclovir
Resistências:
mutações UL97 (perda de afinidade da fosfotransférase)
sem resistencia cruzada com o foscarnet ou o cidofovir
mutações UL54 (perda de afinidade da polimérase do ADN)
resistencia cruzada com cidofovir
Ganciclovir
Indicações terapêuticas:
Retinite CMV (indução e manutenção)ColiteEsofagitePneumonite em imunodeprimidos
Ganciclovir
Efeitos laterais:
Depressão da medula óssea NeutropeniaTrombocitopenia Anemia
Toxicidade SNCToxicidade hepática
Ganciclovir
Farmacocinética
Aciclovir/Valaciclovir Penciclovir/Fanciclovir Ganciclovir
Biodisponibilidade 15 /50% <5 /70% 3-7 %
Lig. às proteínas < 20% <20% 1-2%
Semivida 2,5 h 2 h 3 h
Eliminação renal 70% 90% 95%
Foscarnet
Ácido fosfonofórmico Tóxico para diversos alvos inibe não-
competitivamente, por exemplo, a polimérase do ADN dos herpesvírus e a transcríptase reversa do HIV
Actividade contra:HSV,VZV,CMV,EBV e HHV-6HSV e CMV resistentes ao aciclovirHIV
Resistência:Mutação das enzimas alvo
Toxicidade renal
Hipocalcemia, hipercalcemia,hipomagnesemia,hipocaliemia,hipo- e hiperfosfatemia
Anemia, neutropenia
Toxicidade hepática
Foscarnet
Cidofovir
Cidofovir Cidofovir-MP
Cidofovir-DP
cínase celularcínase celular
Polimerase vírica Síntese do ADN vírico
É um nucleosídeo acíclico derivado do fosfonato
Actividade contra: HSV,VZV,CMV,EBV e HHV-6 In vitro:adenovirus, poxvírus, virus do papiloma humano, virus resistentes ao aciclovir
Resistência:Mutações da polimerase
Cidofovir
Toxicidade renal (hidratação e probenecide)
Neutropenia, Anemia, Trombocitopenia
Toxicidade hepática
Hipotonia ocular
Cidofovir
Farmacocinética
Foscarnet Cidofovir
Biodisponibilidade 17% baixa
Semivida 4-6 h 2.6 h
Eleminação renal 80% 90%
Derivado da timidina
Incorporada no DNA vírico e celular
Activo sobre o HSV
Mielotoxicidade
Aplicação tópica (queratite HSV)
Idoxuridina
Vidarabina
Arabinosídeo de alanina
Encefalite HSV
HSV neonatal
HSV e VZV em doentes imunosuprimidos
Tratamento tópico (queratoconjuntivite)
Análogo pirimidínico nucleosídico fluorado
Inibe competitivamente a polimérase do ADN
HSV-1 e HSV-2 (inclui os resistentes ao aciclovir)
Fosforilação celular
Mielotoxicidade
Aplicação tópica (queratoconjuntivite)
Trifluridina
Análogo nucleosídico da citidina
Actividade contra: HBV , HIV
HBV DNA – diminui 97% após 2 semanas
HBV DNA – diminui 98% após 1 ano
Seroconversão do Ag HBe em 20%
Recorrência vírica de 80% após paragem do fármaco
Lamivudina
Aparecimento de estirpes resistentes do HBVMutação YMDDSensíveis ao Adefovir
8-9 meses após terapêutica
20% ano de estirpes resistentes/ano
Lamivudina
845 a.a.
Terminal Terminal ProteinProtein SpacerSpacer PolPol/RT/RT RNaseHRNaseH
A B C
1 183 349 692
YYMMDDDDD
GVGLSPFLLAI(G) II(F)
(rt1) (rt 344)
E
Lamivudine-resistant
mutations:
L528ML528M ** M552V/I*M552V/I*rtrt L180ML180M rtrt M204I/VM204I/V
* old nomenclature
WILD TYPEWILD TYPE MUTANTMUTANT
Modeling indicates mutation of M552L to V in HBV polymerase causes steric hindrance between the β-methyl branch on the side chain of valineand the sulphur atom in the L-oxathiolane ring of 3TCTP. *Das K, et al. J Virol. 2001;75:4771-4779.
WILD TYPEWILD TYPE MUTANTMUTANT
Modeling indicates HBV polymerase mutations M552V and L528M have no steric effects on the binding of adefovir diphosphate (ADVDP).
*Das K, et al. J Virol. 2001;75:4771-4779.
DNA-VHB (PCR)M
edia
n Se
rum
HB
V D
NA
Cha
nge
-4
-3
-2
-1
0
1
Baseline 4 8 12 16
(Log
10 c
opie
s/m
L)
LAMADVADV+LAM
Weeks
Biodisponibilidade 80%
Ligação às proteínas plasmáticas 36%
Semivida de 5-7h
Concentrações no LCR de 30% das do plasma
Lamivudina
Ribavirina
Nucleosídeo sintético de purina
Desenvolvido há dezenas de anos
Acção antivírica diversificada mas pouco potente contra vírus ADN e ARN
Até há pouco tempo usado praticamente apenas em pediatria pela sua acção sobre o vírus sincicial respiratótio(RSV)
Interesse recente adicional pela sua actividade sobre o vírus da hepatite C (HCV)
Mecanismo de actuação:
diminuição de trifosfato de guanosinadiminuição da síntese do ADNdiminuição da síntese proteica víricainibição da síntese do ARNm
Ribavirina
Efeitos laterais:
Anemia hemolítica
Leucopenia
Hiperuricemia
Hiperbilirrubinemia
Depressão, ansiedade e insónia
Teratogénica, mutagénica, gonodatóxica
Ribavirina
Citoquina produzido pelas células eucarióticas
Sem actividade antivírica directa
Modula a resposta imunológica – TH1
Tipo I – IFN-α ; IFN- β; Tipo II- IFN-γ
Interferon
Actividade antivírica:
Penetração, descapsulação, síntese do ARNm, transdução de proteínas víricas, libertação vírica
IFN- β – esclerose múltiplaIFN-α – VHB, VBC, papiloma virus, melanoma maligno, sarcoma de Kaposi, linfoma folicular
IFN-2a e 2b – ADN recombinante
INTERFERON
Administrados por via i.m, i.v, subcutânea, intralesional.Interferon peguilado – PEG (polietileno glicol)
Efeitos laterais: Síndrome gripalLeucopenia, trombocitopenia, Anemia
Sonolência, depressãoToxicidade hepática e tiroideia
Interferon
Interferon / ribavirina
0
10
20
30
40
50
60
70
80
90
100
% d
e re
spos
ta s
uste
ntad
a
IFN6m
IFN12m
IFNRIV6m
IFNRIV12m
PEG12M
PEGRIV12M
6
16
34
42 39
55
1986 1998 2001 2002
Interferon / ribavirina
0
10
20
30
40
50
60
70
80
90
100%
de
resp
osta
sus
tent
ada
Gen,1 Gen,1 Gen 2/3
16
41
78
46
61
77
Gen,1Gen,1 Gen 2/3Gen,1
Peg IFN + RIV
24 Sem. 48 Sem.
Inibidores da ligação e entrada na célula hospedeira
HIVHIV11
RNARNA
LinfLinfóócitocito TTgp120gp120 gp41gp41
CD4CD4
CXCR4 ou CCR5CXCR4 ou CCR5 gp41gp41
CD4CD4
INIBIDOR MECANISMO DE ACÇÃO FASE CLÍNICA
CD4 sr Inibição competitiva do receptor da gp120 Fase 1-2 (mostrou pouca actividade)
TNX-355 Atc monoclonal antiCD4 ... Fase 1-2 (dose-dependente após única adm EV)
PRO 542 CD4 tetramérico incorporado na γ-globulina Fase 1-2 (evidência preliminar de actividade)
Rec
epto
r C
D4
BMS-806 Ligação à gp120 para impedir a do CD4 Pré-clínica
SCH-C Antagonista RANTES (ligação competitiva ao CCR5) Fase 1-2 (actividade curta duração após adm PO)
PRO 140 Atc monoclonal anti-CCR5 Pré-clínica
Rec
epto
res d
as
quim
ioqu
inas
AMD3100 Inibidor do CXCR4 Fase 2 (actividade mínina após adm EV)
Sulfato dextrano Ligação à gp120 e inibe a interacção do CXCR4 Fase 1-2 (resultados mistos; elevada toxicidade)
PRO 2000 Ligação ao CD4 impedindo a da gp120 Fase 2 em curso (uso tópico)
Out
ros
Cianovirina-N Ligação à gp120 interferindo com a interacção do CD4 e CXCR4 Pré-clínica (uso tópico)
Enfuvirtide (T-20) Péptido que interfere na fusão mediada pela gp41 Fase 3 (actividade > 1A por adm SC; vantagem aos 6M
como TT de resgate; aprovado pelo FDA)
T-1249 Péptido que interfere na fusão mediada pela gp41 Fase 1-2 (actividade de curta duração por adm SC; interesse no TT de resgate em doentes portadores de vírus resistentes ao T-20
Fusã
o da
mem
bran
a
“Penta-hélix” Ligação à extremidade C da gp41 formando uma estrutura hexa-hélix estável, inibindo a fusão Pré-clínica
INFECÇÃO HIV Inibidores da entrada celular
INFECÇÃO HIV Inibidores da entrada celular
Já em uso clínico prático
Inibidores da ligação e entrada na célula hospedeira
HIVHIV11
RNARNA
LinfLinfóócitocito TTgp120gp120 gp41gp41
CD4CD4
CXCR4 ou CCR5CXCR4 ou CCR5 gp41gp41
CD4CD4
CdsrCdsr
Antivíricos
HIVHIV11
RNARNA
LinfLinfóócitocito TTgp120gp120 gp41gp41
CD4CD4
CXCR4 ou CCR5CXCR4 ou CCR5 gp41gp41
CD4CD4
BMSBMS--806806
Inibidores da ligação e entrada na célula hospedeira
HIVHIV11
RNARNA
LinfLinfóócitocito TTgp120gp120 gp41gp41
CD4CD4
CXCR4 ou CCR5CXCR4 ou CCR5 gp41gp41
CD4CD4
TNXTNX--355355
Enfuvirtide
Administrado por via subcutânea
Aumento de incidência da pneumonia bacteriana
Resistência por mutação HR1 da superfície gp41
Não inibe a CYP3A4
Reacção no local da injecção
Antivíricos
Inibidores da transcríptase reversa - Análogos nucleosídicos e nucleotídicosabacavir adefovir didanosina entricitabina lamivudina estavudina tenofovir zalcitabina zidovudina
Inibidores da transcriptase reversa - Análogos nucleosídicos
Estruturalmente semelhantes aos ácidos nucleicos
Diferem no radical hidroxilo na posição 3’
Impedem a ligação 5’-3’
Fosforilados pelas cínases celulares na posição 5’
Anti-HIV1 e anti-HIV 2
Nucleosídeos análogos da citidinazalcitabina,lamivudina,entricitabina
Nucleosídeos análogos da timidinazidovudina, estavudina
Nucleosídeos análogos da adenosina e inosinadidanosina
Nucleosídeo análogos da guanosinaabacavir
Nucleotídeos análogos do fosfato de adenosina adefovirtenofovir
Inibidores da transcríptase reversa - Análogos nucleosídicos
Inibidores da transcríptase reversa - Análogos nucleosídicos
1) maior actividade nas células em replicação
zidovudina, estavudina (análogos da timidina)
2) maior actividade nas células em repouso
didanosina, zalcitabina, lamivudina
Zidovudina
Análogo da timidina
Maior actividade sobre células em replicação
Biodisponibilidade de 65%
Ligação às proteínas plasmáticas 24-28%
Semivida intracelular > semivida plasmática
Concentrações no LCR 50% das concentrações plasmáticas
Zidovudina
Interacções medicamentosas:
probenecide – diminui a excreção
ribavirina – diminui a fosforilação intracelular
metadona – aumenta a concentração plasmática
Zidovudina
Efeitos laterais:
anemia
neutropenia
macrocitose
miopatia, miosite
hiperpigmentação da pele e unhas
Estavudina
É um análogo síntético da timidina
Similar à zidovudina
Biodisponibilidade 80%
Semivida intracelular > semivida plasmática
Concentrações no LCR 40% das concentrações plasmáticas
Estavudina
Efeitos laterais:
neuropatia periférica reversivel
macrocitose
pancreatite
toxicidade hepática
Didanosina
É um análogo síntético da purina
Maior actividade em células em “repouso”
Instável em meio ácido
Biodisponibilidade 30-40%
Semivida intracelular > semivida plasmática
Concentrações no LCR 20% das concentrações plasmáticas
Didanosina
Efeitos laterais:
neutropenia (30%)
pancreatite (5-10%)
rabdomiólise
despigmentação da retina
hipertrigliceridemia, hiperuricemia
Zalcitabina
É um análogo síntético da pirimidina
Maior actividade em células em “repouso”
Biodisponibilidade 80%
Concentrações no LCR 9-37% das concentrações plasmáticas
Zalcitabina
Efeitos laterais:
neutropenia reversivel
pancreatite (menos frequente)
úlceras orais ou penianas múltiplas (3%)
Zalcitabina
Interacções medicamentosas:
didanosina + zalcitabina
risco acrescido de neuropatia e pancreatite
Abacavir
É um análogo da guanosina
Convertido em carbovir trifosfato
Biodisponibilidade > 80%
Concentrações no LCR 27-33 % das concentrações plasmáticas
Correlação entre a frequência de alguns efeitos laterais dos inibidores nucleosídicos da transcríptase reversa do HIV e a
potência inibidora da polimerase do ADN do hospedeiro
Efeitos laterais:pancreatite, lipodistrofia, resistência à insulina, neuropatia, miopatia
Inibição da polimerase γ do ADN
zalcitabina>didanosina>estavudina>zidovudina>lamivudina=abacavir=tenofovir
Efeitos Laterais
Zido. Lami. Didano. Estav. Zalci. Abac.
Anemia +++ + + + + +
Leucopenia +++ + + + + +
Neuropatia periférica - + + + + ++ +
Pancreatite - + + ++ + + +
RESISTÊNCIA AOS NRTIRESISTÊNCIA AOS NRTI
↓ INCORPORAÇÃO DO TERMINADOR↓ INCORPORAÇÃO DO TERMINADOR REMOÇÃO DO TERMINADORREMOÇÃO DO TERMINADOR
M184VK65RComplexo Q151M
M184VK65RComplexo Q151M
Família análogos da TCodão 69Família análogos da TCodão 69
Resistência
Redução da incorporação do análogo terminador: exemplos
Mutação Consequência
M184V Resistência à lamivudina
Complexo Q151M Resistência a todos NRTI excepto lamivudina
K56R Resistência a todos NRTI excepto zidovudina
Resistência
Remoção do terminador (exemplo)
Consequência
Resistência de largo espectro que inclui o tenofovir
Antivíricos
Inibidores da transcriptase reversa – não-nucleosídicos
delavirdina efavirenz nevirapina
Farmacocinética
Nevirapina Delavirdina Efavirenz
Biodisponibilidade (%) 90 > 80 ?
Lig. às proteínas 60 98 99
Penetração LCR (%) 45 <1 0.26-1.19
Farmacocinética
Nevirapina Delavirdina Efavirenz
Efeitos laterais Rash cutâneo Rash cutâneo S N C
Interacção alimentos sem sem evitar gorduras
CYP 3A4 Indução Inibição Indução e inibição
Resistência
Mutação Nevirapina Delavirdina Efavirenz
K103N Resistência
Y181C Resistência
K103N Resistência Resistência Resistência
Antivíricos
Inibidores da protease
amprenavir atazanavir indinavir fosamprenavir lopinavir nelfinavir ritonavir saquinavir
Transcriptasereversa
Poliproteínasprecursoras
Proteínasfuncionais
ARN
ADN
cápside
matriz
? ? ?
nucleocápside
Farmacocinética
Saquinavir Ritonavir Indinavir Nelfinavir Amprenavir
Biodisponibilidade (%) 12 75 60 20-80 60-80
Lig. às proteínas 98 98-99 ? >98 90
Metabolização Hep Hep Hep Hep Hep
Eleminação renal (%) <5 <15 <20 <5 <5
Fosamprenavir
Pró-fármaco do amprenavir
As refeições não interferem na AUC
Inibidor / indutor da CYP3A4
Sem resistência cruzada ?
Atazanavir
As refeições aumentam a AUC
Inibidor da CYP3A4
Risco de bloqueio AV
Não causa dislipidemia?
Interacções medicamentosas
Ritonavir Indinavir Nelfinavir Saquinavir Amprenavir
Ritonavir 3,6 x 2.5x 20x 3.5x
Indinavir 1.8x 5-8x 1.6x
Nelfinavir 1.5x 4-6x 2.5x
Saquinavir 1.2x 30%
Amprenovir 38% 1.2x 18%
Interacções medicamentosas
Delavirdina Nevirapina Efavirenz
Ritonavir 1,7 x 41% 1.2x
Indinavir 1,4 x 30% 30%
Nelfinavir 2 x 1.1x 1.2x
Saquinavir 6 x 25% 60%
Amprenovir 35%
Interacções medicamentosas
Não interfere Refeições aumentam a AUC Refeições diminuem a AUC
Fosamprenavir Lopinavir AmprenavirAtazanavir IndinavirRitonavirNelfinavirSaquinavir
Interacções medicamentosas
Rifampicina Rifabutina
Delavirdina Não associar 96% não 80%
Nevirapina Talvez 20-58% Sim 16%
Efavirenz Talvez 25% Talvez 35% Rifab.
Interacções medicamentosas
Rifampicina Rifabutina
Indinavir Não associar 89% Sim x2
Nelfinavir Não 82% Sim x2
Amprenavir Não 82% Sim x2
Ritonavir Talvez 35% Talvez x4
Quem tratar?
1) Doentes com SIDA
2) Doentes assintomáticos com < 200 CD4+ /mm3
3) Doentes assintomáticos com 201-350 CD4+ /mm3
4) Doentes assintomáticos > 350 CD4+ /mm3 eRNA do HIV > 100.000/cópias /ml
Como tratar ?
inibidores da transcríptase reversa não-nucleosídicos (1) + nucleosídicos (2)
efavirenz + zidovudina (ou tenofovir) + lamivudina (ou entricitabina)
Como tratar ?
inibidores da transcríptase reversa não-nucleosídicos (1) + nucleosídicos (2)
efavirenz + didanosina (ou abacavir ou estavudina) + lamivudina (ou entricitabina)
nevirapina + didanosina (ou abacavir ou estavudina) + lamivudina (ou entricitabina)
nevirapina + zidovudina (ou tenofovir) + lamivudina (ou entracitabina)
Como tratar ?
inibidores da protease (1 ou 2) + inibidores nucleosídicos da transcríptase reversa (2)
lopinavir/ritonavir + zidovudina + lamivudina (ou entricitabina)
Como tratar ?
inibidores da protease (1 ou 2) + inibidores nucleosídicos da transcríptase reversa (2)
lopinavir/ritonavir + abacavir (ou estavudina ou tenofovir ou didanosina) + lamivudina (ou entricitabina)
Vantagens Desvantagens
NNRTI menor lipodistrofia resistênciaguarda dos inibidores da protease intervenção nas CYP
efavirenz potente antivírico teratogénicouma toma diária
nevirapina tomas com as refeições exantemashepatotoxicidade
Vantagens Desvantagens
Inibidores da protease aumento da sobrevivênvia lipodistrofiaguarda dos NNRTI acção sobre as CYP
lopinavir/ritonavir potente antivírico efeitos adversos gastrointestinais
atazanavir menos lipodistrofia aumento PRuma toma diária hiperbilirrubinemia
Como não tratar ?
1) monoterapia (excepto na gravidez – zidovudina)
2) amprenavir+fosamprenavir
3) atazanavir+indinavir (hepatotoxicidade)
4) didanosina+estavudina (neuropatia periférica, pancreatite, acidose láctica)
5) didanosina+zalcitabina ou estavudina + zalcitabina (neuropatia periférica)
Como não tratar ?
6) efavirenz durante a gravidez (teratogenicidade)
7) entricitabina+lamivudina (resistência cruzada)
8) lamivudina+zalcitabina (inibição da fosforilação celular mútua)
9) saquinavir como único inibidor da protease (biodisponibilidade)
10)estavudina+zidovudina (antagonismo in vitro e vivo)